субтотальное поражение желудка что
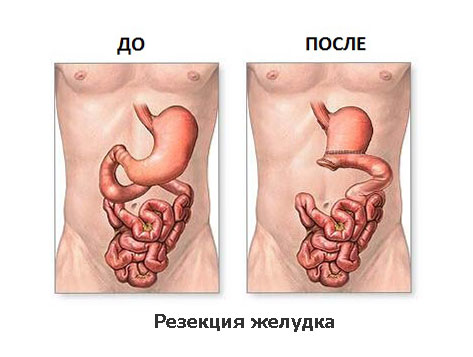
Операция резекции и гастрэктомии
29 января 1881 года Теодор Бильрот провел первую успешную операцию резекции желудка при локализации рака в его выходном отделе. Последующая и также успешная операция резекции была проведена через несколько месяцев ассистентом Бильрота. Успех заключался и в продолжительности жизни пациента, первого среди прооперированных по поводу рака желудка прожившего пять лет после операции.
Уважаемые пациенты! Обратите внимание на следующие материалы сайта:
Несмотря на то, что с момента выполнения первой успешной операции на желудке прошло более 130 лет и за прошедшее время медицина шагнула далеко вперед, основным методом лечения рака желудка остается операция. Никакие другие методы лечения не могут заменить хирургическое вмешательство.
Принципиально выделяют два вида радикальных операций по поводу рака желудка: субтотальная резекция желудка и гастрэктомия. Выбор объема операции зависит в первую очередь от локализации опухоли в желудке, уровня глубины проникновения опухоли в стенку желудка, а также её распространение на соседние органы и структуры.
Дистальная субтотальная резекция желудка
При распространении опухоли на соседние органы выполняется и их резекция. Операция завершается восстановлением непрерывности желудочно-кишечного тракта формированием анастомоза (соустья) между оставшейся частью желудка и тонкой кишкой.
Существует несколько десятков способов восстановления непрерывности желудочно-кишечного тракта, но наиболее часто применяемыми являются следующие: по Бильрот, Бальфуру, Ру, Райхелю—Полиа, Хофмейстеру—Финстереру, Мойнихену. Анастомозы формируются с помощью ручного шва, либо с помощью различных сшивающих аппаратов.
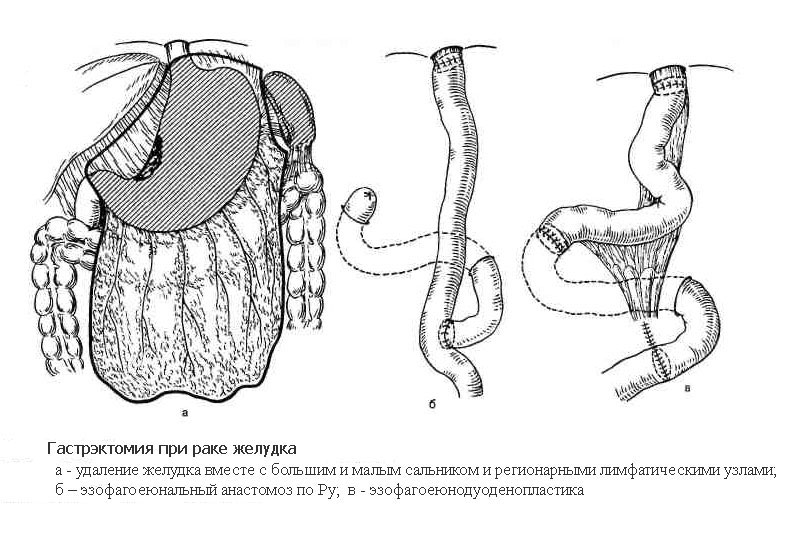
Гастрэктомия
Гастрэктомия – операция, выполняемая при локализации раковой опухоли в средней и верхней трети тела и кардиальном отделе желудка, а также при расположении опухоли в месте перехода желудка в пищевод (кардиоэзофагеальный рак). Объем операции включает удаление всего желудка, также с обязательным выполнением лимфодиссекции. В отдельных случаях дополнительно удаляются селезенка вместе с телом и хвостом поджелудочной железы. При распространении опухоли на соседние органы выполняется и их резекция. Операция завершается формированием анастомоза напрямую между пищеводом и тонкой кишкой, также либо с помощью ручного шва, либо с помощью специальных сшивающих аппаратов.
Изложенные операции могут выполняться традиционным (открытым) методом и с помощью высокотехнологичных малотравматичных методов (лапароскопическим или роботическим).
Традиционный (открытый) метод применяется у пациентов с местнораспространенными опухолями желудка требующие расширенных и комбинированных операций с резекцией соседних органов и структур, а также у пациентов с высоким индексом массы тела (ИМТ>30).
У пациентов с начальной (I-II) стадией заболевания и с ИМТ
Гладышев Дмитрий Владимирович:
Коваленко Сергей Алексеевич:
Городская больница №40, г.Сестрорецк, ул.Борисова, д.9, хирургический корпус (№4), кабинет №19.
Часы приёма: понедельник, среда, пятница с 15.00 до 17.00. По направлению онкологов поликлиник.
Запись по телефону: 8-911-235-21-80.
Информационно-справочная служба: +7 (812) 437-40-75 и +7 (812) 437-31-11
Отдел платных услуг: +7 (812) 437-11-00 и +7 (911) 766-97-70
Информация по отборочной комиссии: +7 (812) 437-09-07
Отдел госпитализации: +7 (812) 437-03-68 и +7 (812) 434-32-13
Запись на МРТ, КТ, ПЭТ КТ : +7 (812) 437-35-13 и +7 (911) 171-06-04
Маммография: +7 (812) 200-16-88.
Вы можете выбрать удобную для Вас дату исследования соответственно с периодом менструального цикла.
Кроме того, Вы можете оставить свой вопрос в рубрике «Вопрос-ответ» и сотрудники отдела платных услуг обязательно свяжутся с Вами или ответят по указанному Вами адресу электронной почты.
Лечение рака желудка
О заболевании
Рак желудка – это новообразование в слизистой желудка. По мере разрастания опухоли она прорастает глубже в слои желудка, а также в ближайшие органы и лимфатические узлы.
Симптомы отличаются в зависимости от стадии онкологии. Чтобы подтвердить наличие опухоли, ее вид и ее стадию, пациент направляется на дополнительные исследования терапевтом или гастроэнтерологом.
При лечении проводится операция с последующей химиотерапией. Прогноз на выздоровление зависит от стадии рака, его вида и тактики проводимого лечения.
Виды рака желудка
В зависимости от гистологического строения, рак желудка делится на:
При раке желудка проводится иммуногистохимия для выявления HER/2 нео рецепторов. Эта опухоль отличается более агрессивным течением, но, вместе с тем, наличие данных рецепторов позволяет использовать в лечении высокоэффективный таргетный препарат (например, герцептин).
Симптомы рака желудка и первые признаки
Диагностика рака желудка на ранних стадиях происходит очень редко. Если вы следите за своим самочувствием и не пренебрегаете появившимися «малыми признаками», то лучше обратиться к врачу. В нашей клинике принимают онконастороженные терапевты и гастроэнтерологи, то есть они учитывают возможность наличия онкологии и, при малейшем подозрении, направляют таких пациентов на диагностику, которая позволяет исключить или выявить ранний рак.
Клиническое проявление онкологии напрямую зависит от стадии. Для начальных стадий характерно полное отсутствие симптомов или незначительное проявление:
К симптомам второй стадии относятся:
К симптомам третьей стадии относятся:
К симптомам четвертой стадии относятся:
Диагностика рака желудка
Установить верный диагноз можно только с помощью инструментальной диагностики. Но перед ее назначением предположительный диагноз должен подтвердиться другими диагностическими методами.
Для этого терапевтом или гастроэнтерологом проводится тщательный сбор и анализ жалоб пациента при подозрении на наличие онкологии. В зависимости от полученных данных назначается подходящая диагностика.
После всего этого проводятся лабораторные исследования:
Инструментальная диагностика рака предусматривает:
Стадии рака желудка и прогноз
1 стадия
Опухоль небольшого размера (до 2 см), занимает слизистый и подслизистый слой стенки желудка. Ближайшие лимфоузлы не поражены или поражены точечно, метастазов нет. Прогноз при данной стадии благоприятный и составляет 60-80% выживаемости.
2 стадия
Опухоль уже прорастает глубже в стенку желудка и поражает больше регионарных узлов (до 15), при этом метастазов нет. Прогноз при данной стадии составляет 50% выживаемости.
3 стадия
Происходит полное поражение всей стенки желудка и более отдаленных лимфоузлов, но нет метастазов в отдаленных органах. Возможно поражение опухолью соседних органов, но без поражения лимфоузлов. Прогноз при данной стадии составляет 20% выживаемости.
4 стадия
Характеризуется распространением рака на соседние органы или наличием хотя бы одного метастаза в отдаленные органы. Прогноз при данной стадии составляет 10% выживаемости.
Очень важно отметить, что при 4 стадии наша задача состоит в том, чтобы перевести заболевание в хроническую форму, что позволяет продлить жизнь пациента в 3 и более раз.
Не зависимо от стадии вы получите лечение европейского уровня, которое намного эффективнее, чем протоколы Минздрава, принятые в России и странах СНГ.
Метастазы при раке желудка
При раке желудка метастазы распространяются либо по лимфатическим путям, либо по системе кровоснабжения. Наиболее часто происходит метастазирование печени, поджелудочной, кишечника и брюшной стенки.
Лечение рака желудка
Рак желудка почти всегда лечится хирургически. Объем операции напрямую зависит от стадии заболевания. Если опухоль не успела прорасти вглубь стенки желудка, то проводят эндоскопическую резекцию при помощи гастроскопа.
При субтотальной гастрэктомии удаляется часть желудка, пораженную онкологией.
На более поздних стадиях желудок удаляется целиком с захватом окружающих тканей. Пищевод при этом сшивают с тонким кишечником. При наличии пораженных лимфоузлов, они также подлежат удалению.
В тяжелых случаях, когда полное излечение невозможно, проводится паллиативная операция. Хирург удаляет пораженную часть желудка, чтобы облегчить состояние пациента и перевести рак в хроническую форму.
Химиотерапия при раке желудка
Химиотерапия бывает адъювантной и неоадъювантной. То есть до операции и после нее. При некоторых видах онкологии ее совмещают с лучевой терапией. Сочетание химиотерапии и лучевой терапии может быть основной тактикой при метастазировании на поздних стадиях, когда полное излечение невозможно.
В отдельных случаях эффективны таргетные препараты: трастузумаб, рамуцирумаб, иматиниб, сунитиниб, регорафениб. Но их применение возможно только когда раковые клетки обладают нужными молекулярно-генетическими характеристиками.
Материалы конгрессов и конференций
V РОССИЙСКАЯ ОНКОЛОГИЧЕСКАЯ КОНФЕРЕНЦИЯ
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ РАКА ПРОКСИМАЛЬНОГО ОТДЕЛА ЖЕЛУДКА: ЭВОЛЮЦИЯ СТАНДАРТОВ
М.И. Давыдов, Тер-Ованесов М.Д., Стилиди И.С., А.Н. Абдихакимов, В.А. Марчук
ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России, Москва
Основу настоящего исследования составляет анализ результатов лечения 1209 больных раком проксимального отдела желудка, находившихся в отделении торако-абдоминальной онкологии ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России с января 1975 года по декабрь 1996 года включительно.
В течение двадцатидвухлетнего периода в клинике торакальной онкологии ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России совершенствовалась техника хирургических вмешательств, изменялась концепция хирургического лечения рака проксимального отдела желудка, совершенствовались методы предоперационной подготовки и послеоперационного ведения больных. В последнее десятилетие летальность после операций значительно уменьшилась, несмотря на то, что с 1988 года абсолютному большинству больных стандартно выполняются расширенные и расширенно-комбинированные операции. Расширение объема вмешательства требует детальной отработки каждого компонента, учитывая общее повышение риска выполнения подобных вмешательств в плане развития послеоперационных осложнений. Длительное время наиболее сложным и коварным элементом любого вмешательства на органах желудочно-кишечного тракта считались анастомозы, в особенности пищеводные соустья, характеризовавшиеся высокой частотой развития несостоятельности и связанной с этим осложнением летальности. В настоящее время, благодаря детальной отработке техники формирования пищеводных соустий, характеризующихся относительной простотой исполнения, универсальностью применения, а также высокой надежностью, недостаточность швов анастомоза стала казуистически редким осложнением.
Различия в показателях послеоперационной летальности в разные периоды работы клиники статистически достоверны и составляют 27,0±5,6%, 12,8±1,9% и 5,2±0,9% соответственно. Абсолютное большинство расширенных и расширенно-комбинированных операций выполнены в последний период и сопровождались послеоперационной летальностью, не превышающей 5%.
Частота хирургических осложнений после резекций в I, II и III периоды работы клиники составила соответственно 61,9±6,1%, 36,2±2,8% и 19,2±1,6% (различия статистически достоверны). В то же время частота терапевтических осложнений практически не изменилась: 15,9±4,6%, 17,2±2,2% и 19,3±1,9% соответственно.
Таким образом, анализ непосредственных результатов хирургического лечения больных раком проксимального отдела желудка в разные периоды работы клиники торакальной онкологии ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России свидетельствует о существенном снижении показателей летальности и частоты хирургических осложнений вследствие совершенствования техники оперативных вмешательств.
Из всей группы пациентов, перенесших хирургическое вмешательство и выписанных из клиники, прослежена судьба 500 больных (84,2%): 5 и более лет после операции без рецидива и отдаленных метастазов прожили 118 больных, т.е. пятилетняя выживаемость составила 23,6%.
Важным фактором, определяющим прогноз у больных, оперированных по поводу рака проксимального отдела желудка, является распространение опухоли на пищевод. При этом большая распространенность опухоли в желудке усиливает влияние этого фактора.
Пятилетняя выживаемость у больных с распространением опухоли на пищевод была в два раза ниже, чем у больных без вовлечения пищевода в опухолевый процесс: 21,9±1,9% и 44,7±8,1% соответственно(t=2,7).
При вовлечении в опухолевый процесс верхней трети и тела желудка различия в показателях пятилетней выживаемости в зависимости от распространения опухоли на пищевод были выражены в наибольшей степени: 13,6±2,7% и 40,7±9,6% соответственно (t=2,7). Эти данные коррелируют с частотой метастатического поражения регионарных лимфатических узлов: при распространении опухолевой инфильтрации до уровня диафрагмального сегмента пищевода частота лимфогенного метастазирования составляет 81,6%.
Таким образом, изучение отдаленных результатов хирургического лечения рака проксимального отдела желудка показало, что пятилетняя выживаемость в целом составляет 23,6%. Этот показатель остается весьма низким по сравнению с пятилетней выживаемостью больных, оперированных по поводу рака дистальных отделов желудка. Распространение опухоли на пищевод, несомненно, является важнейшим прогностическим фактором, поскольку, как было показано выше, сочетается с более высокой частотой метастатического поражения лимфатических узлов и с вовлечением лимфоколлекторов средостения.
При проксимальных резекциях показатели пятилетней выживаемости мало отличались друг от друга при расширенных (32,8±6,0%) и стандартных (30,2±3,9%) операциях. При гастрэктомиях показатель пятилетней выживаемости после расширенных операций был более чем в три раза выше, чем после стандартных (34,3±8,0% и 10,1±3,6% соответственно, t=2,8). Наибольшие различия в показателях пятилетней выживаемости отмечены после гастрэктомий у больных с вовлечением в опухолевый процесс пищевода и кардии, а также при вовлечении в процесс серозной оболочки (27,8±10,9% и 6,6±3,2% соответственно, t=2,1).
Таким образом, расширенные гастрэктомии имеют несомненные преимущества перед стандартными и сопровождаются более высокими показателями пятилетней выживаемости.
Другим фактором, определяющим противопоказания к выполнению проксимальной субтотальной резекции желудка, являются метастазы в лимфатические узлы, расположенные вдоль правой половины большой кривизны желудка, а также супра- и субпилорические. Эти группы лимфоколлекторов следует рассматривать как второй этап лимфогенного метастазирования, подлежащий удалению. Поэтому пальпаторное обнаружение увеличенных лимфатических узлов этих групп при интраоперационной ревизии требует выполнения расширенной гастрэктомии.
Таким образом, расширенные лимфодиссекции позволяют улучшить отдаленные результаты у больных раком проксимального отдела желудка. Преимущества расширенной лимфодиссекции выявлены лишь у тех больных, которым по онкологическим показаниям выполнены гастрэктомии. Данные, представленные выше, позволяют прийти к заключению, что по онкологическим критериям при раке проксимального отдела желудка с размером опухоли более 4 см и выходом процесса на серозную оболочку операцией выбора является гастрэктомия D2, а при поражении лимфатических узлов второго этапа метастазирования целесообразно увеличить объем лимфодиссекции до D3 с обязательным удалением верхних парааортальных лимфатических узлов (16а1).
Оценивая значение расширенной лимфодиссекции у больных раком проксимального отдела желудка в целом, необходимо отметить следующее:
1 Wright C., Mathisen D., Wain J., Grillo H. et al. //Evolution of treatment strategies for adeno-carcinoma of the esophagus and GE junction.// Ann Thorac Surg 1994; 58: 1574-1579.
2 Двойрин В.В., Аксель Е.М., Трапезников Н.Н. Заболеваемость злокачественными новообразованиями и смертность от них населения стран СНГ. Москва-1996;
3 Lerut T., Coosemans W., DE Leyn P., Deneffe G., Topal B., Van de Ven C., Van Raemdonc D. // Reflections on three Field Lymphadenectomy in Carcinoma of the Esophagus and Gastro-Esophageal Junction.// Hepato-Gastroenterology 1999; 46: 717-725.
4 Siewert JR, Roder JD //Lymphadenectomy in esophageal cancer surgery.// Dis Esophagus 1992; 64: 45-60.
5 Holscher AH, Schuler M, Siewert JR. //Surgical treatment of adenocarcinomas of the gastroesophageal junction.// Dis of Esophagus 1989; 1: 35-50.
6 Steup WH, De Leyn P., Deneffe G., Van Raemdonck D., Coosemans W., Lerut T. //Tumors of the esophago-gastric junction. Long-term survival in relation to pattern of lymph node metastasis and a critical analysis of the accuracy or inaccuracy of pTNM classification.// J Thorac Cardiovasc Surg, 1996; 111: 85-95.
7 Lerut T., De Leyn P., Coosemans W., Van Raemdonck D. //What is the optimal extent of lymphadenectomy in tumors of the GE-junction. The role of cervical lymphadenectomy.// 2nd International Gastric Cancer Congress, Munich, Germany, 27-30 Apr 1997 in Manduzzi Editore, pp 1223-1227.
8 Давыдов М.И., Тер-Ованесов М.Д. //Современная стратегия хирургического лечения рака желудка.//Современная онкология; 2000; Том 2, №1: стр. 4-12.
9 Maruyama K, Sasako M, Kinoshita T, Okajima K Effectiveness of Systemic Lymph Node Dissection in Gastric Cancer Surgery. In Nishi M., Ichikawa H., Nakajima T., Maruyama K., Tahara E. Gastric cancer. Springer-Verlag; 1993: 293-306
Рак желудка
Общая информация
Краткое описание
Рак желудка – это злокачественное новообразование желудка. [1,2,3,4] (УД-А)
Название протокола: Рак желудка
Код протокола:
Код (ы) МКБ-10:
C 16 Злокачественное новообразование желудка.
Сокращения, используемые в протоколе:
Дата разработки/пересмотра протокола: 2015 г.
Категория пациентов: взрослые.
Пользователи протокола: онкологи (онкохирурги, химиотерапевты, радиологи), общие хирурги, гастроэнтерологи, врачи общей практики, врачи скорой и неотложной помощи, патологоанатомы, морфологи, диетологи.
Оценка на степень доказательности приводимых рекомендаций.
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с не высоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). Результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++или+), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование, или мнение экспертов. |
| GPP | Наилучшая фармацевтическая практика. |
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Международная классификация TNM:
Последний пересмотр этой классификации состоялся в 2009г. – 7-е издание, и она была одобрена всеми национальными комитетами по классификациям заболеваний.
Классификация применима только для рака желудка, при гистологическом подтверждение диагноза.
Анатомические области
· Кардиальный отдел;
· Дно;
· Тело;
· Антральный и пилорический отделы.
Регионарные лимфатические узлы 
Регионарными лимфатическими узлами для желудка являются лимфатические узлы, расположенные вдоль малой (1, 3, 5) и большой (2, 4а, 4б, 6) кривизны, вдоль левой желудочной (7), общей печеночной (8), селезеночной (10, 11) и чревной (9) артерий, а также гепатодуоденальные узлы (12). Поражение других внутрибрюшинных лимфатических узлов, таких как ретропанкреатические, мезентериальные и парааортальные, классифицируются как отдаленные метастазы.
Примечание:
1 Опухоль, которая распространяется на желудочно-ободочную или желудочно-печёночную связку, большой или малый сальник, но не прорастает в висцеральную брюшину, классифицируют как Т3.
2 Соседними структурами для желудка являются селезёнка, поперечная ободочная кишка, печень, диафрагма, поджелудочная железа, брюшная стенка, надпочечники, почки, тонкая кишка, забрюшинное пространство.
N – Региональные лимфатические узлы;
NX – Региональные лимфатические узлы не могут быть оценены;
N0 – Нет метастазов в региональных лимфатических узлах;
N1 –Метастазы в 1 – 2 региональных лимфатических узлах;
N2 – Метастазы в 3—6 региональных лимфатических узлах;
N3 – Метастазы в 7 и более региональных лимфатических узлах.
М – Отдаленные метастазы;
М0 – Нет отдаленных метастазов;
М1 – Есть отдаленные метастазы или наличие опухолевых клеток в асцитической жидкости.
N – Региональные лимфатические узлы;
NX – Региональные лимфатические узлы не могут быть оценены;*
N0 –Нет метастазов в региональных лимфатических узлах;
N1 – Есть метастазы в региональных лимфатических узлах.
*При GIST региональные лимфатические узлы вовлекаются редко, поэтому те случаи, когда статус лимфатических узлов не может быть оценен клинически или морфологически, рассматривают как N0 вместо NX или pNX.
М – Отдаленные метастазы;
М0 – Нет отдаленных метастазов;
М1 – Есть отдаленные метастазы.
Патогистологическая классификация pTNM:
Требования к определению категорий pT, pN, pM соответствуют требованиям к определению категорий T, N, M.
Примечание: pN0 гистологическое исследование включает обычно 15 и более регионарных лимфатических узлов.
| Группировка по стадиям: | |||
| Стадия | T | N | M |
| СТАДИЯ 0 | Tis | N0 | М0 |
| СТАДИЯ IА | Т1 | N0 | М0 |
| СТАДИЯ IB | Т1 | N1 | М0 |
| Т2 | N0 | М0 | |
| СТАДИЯ IIA | Т1 | N2 | М0 |
| Т2 | N1 | М0 | |
| Т3 | N0 | М0 | |
| СТАДИЯ IIB | Т1 | N3 | М0 |
| Т2 | N2 | М0 | |
| Т3 | N1 | М0 | |
| Т4a | N0 | М0 | |
| СТАДИЯ IIIА | Т2 | N3 | М0 |
| Т3 | N2 | М0 | |
| Т4a | N1 | М0 | |
| СТАДИЯ IIIB | Т3 | N3 | М0 |
| Т4a | N2 | М0 | |
| Т4b | N0-1 | М1 | |
| СТАДИЯ IIIC | Т4a | N3 | М0 |
| Т4b | N2-3 | М0 | |
| СТАДИЯ IV | Любая Т | Любая N | М1 |
Диагностика
Перечень основных и дополнительных диагностических мероприятий:
Основные (обязательные) диагностические обследования, проводимые на амбулаторном уровне:
· Сбор жалоб и анамнеза;
· Общее физикальное обследование;
· Рентгенография органов грудной клетки в двух проекциях;
· Фиброэзофагогастродуоденоскопия с биопсией опухоли и морфологическим исследованием биопсийного материала;
· Рентгеноскопическое исследование желудка с контрастированием;
· Ультразвуковая диагностика комплексная (печень, желчный пузырь, поджелудочная железа, селезенка, почек);
· Цитологическое исследование;
· Гистологическое исследование.
Минимальный перечень обследования, который необходимо провести при направлении на плановую госпитализацию: согласно внутреннему регламенту стационара с учетом действующего приказа уполномоченного органа в области здравоохранения.
Основные (обязательные) диагностические обследования, проводимые на стационарном уровне (при плановой госпитализации проводятся диагностические обследования, не проведенные на амбулаторном уровне):
· ОАК;
· Биохимический анализ крови (белок, креатинин, мочевина, билирубин, АЛТ, АСТ, глюкоза крови);
· Коагулограмма (протромбиновый индекс, фибриноген, фибринолитическая активность, тромботест);
· ОАМ;
· Рентгенография органов грудной клетки (2 проекции);
· Компьютерная томография органов грудной клетки и средостения;
· УЗИ надключичных, подмышечных лимфатических узлов;
· Спирография;
· Электрокардиографическое исследование;
· ЭХО КГ (пациентам 50 лет и старше, так же пациенты моложе 50 лет при наличии сопутствующей патологии ССС).
Дополнительные диагностические обследования, проводимые на стационарном уровне (по показаниям):
· Магниторезонансная томография органов средостения с контрастированием;
· УЗИ надключичных и шейных лимфатических узлов;
· УЗИ плевры и плевральной полости;
· Ультразвуковая диагностика комплексная (печень, желчный пузырь, поджелудочная железа, селезенка, почек);
· МРТ головного мозга;
· Колоноскопия;
· Ирригоскопия;
· Фиброэзофагоскопия;
· Отрытая биопсия увеличенных надключичных и шейных лимфатических узлов (при наличии увеличенных лимфоузлов);
· Цитологическое исследование;
· Гистологическое исследование;
· КТ органов грудной клетки;
· КТ органов брюшной полости с контрастированием;
· Сцинтиграфия костей скелета;
· ИГХ исследование биопсийного материала.
Диагностические мероприятия, проводимые на этапе скорой неотложной помощи: нет.
Диагностические критерии постановки диагноза:
Жалобы и анамнез:
Патогномоничных симптомов рака желудка не установлено. Жалобы больного могут соответствовать проявлениям различных заболеваний желудка (хронический гастрит, язвенная болезнь желудка и т.д.).
· Боли в эпигастральной области;
· Дисфагию;
· Тошноту;
· Рвоту (в том числе «кофейной гущей»);
· Потеря аппетита;
· Снижение веса.
Физикальное обследование:
· Положение больного при поздних стадиях рака желудка, чаще вынужденное с выраженной адинамией.
· При осмотре лица – может встречаться уменьшение блеска и живости глаз.
· Бледность кожных покровов может быть указанием на желудочно-кишечное кровотечение. Восковидный или землистый оттенок приобретают кожные покровы у больных с поздними стадиями рака желудка.
· В некоторых случаях при развитии метастазов в симпатические узлы брюшной полости можно наблюдать и выраженную диффузную гиперпигментацию кожных покровов.
· В далеко зашедших стадиях рака желудка отмечаются также сухость кожи и снижение ее тургора.
· Выраженное похудание, достигающее степени кахексии, встречается при раке дистального отдела желудка. В таких случаях у больных появляются и безбелковые отеки.
· В поздних стадиях в надключичной области слева между ножками грудиноключично-сосцевидной мышцы иногда удается определить плотный лимфатический узел с неровной поверхностью, не спаянный с прилегающей кожей (метастаз Вирхова).
· При осмотре полости рта у больных раком желудка может появиться зловонный запах изо рта – признак распада злокачественной опухоли желудка.
· Выбухание стенки живота в подложечной области наблюдается при запущенных формах рака желудка. При резком похудании в ряде случаев удается визуально определить контуры желудка, его малую и большую кривизну.
· При развитии опухолевого стеноза привратника у некоторых больных определяются периодические волнообразные движения, приподнимающие в ограниченных участках переднюю брюшную стенку, которые становятся более отчетливыми после предварительного легкого поколачивания брюшной стенки в эпигастральной области.
· При пальпации передней брюшной стенки опухоли желудка отчетливо пальпируются в тех случаях, если они располагаются преимущественно в дистальных отделах желудка (антральном, пилорическом) и достигают нескольких сантиметров в диаметре.
· При перкуссии можно уточнить положение нижней границы желудка, обнаружить изменение пространства Траубе (при раке субкардиального отдела желудка).
Лабораторные исследования:
Цитологическое исследование (увеличение размеров клетки вплоть до гигантских, изменение формы и количества внутриклеточных элементов, увеличение размеров ядра, его контуров, разная степень зрелости ядра и других элементов клетки, изменение количества и формы ядрышек);
Гистологическое исследование (крупные полигональные или шиповидные клетки с хорошо выраженной цитоплазмой, округлыми ядрами с четкими ядрышками, с наличием митозов, клетки располагаются в виде ячеек и тяжей с или без образования кератина, наличие опухолевых эмболов в сосудах, выраженность лимфоцитарно-плазмоцитарной инфильтрации, митотическая активность опухолевых клеток).
Инструментальные исследования:
· фиброэзофагогастродуоденоскопия (позволяет увидеть дефект слизистой, определить его размеры и характер, взять кусочек ткани для гистологического исследования);
· рентгеноскопическое исследование пищевода с контрастированием, рентгеноскопическое исследование желудка с контрастированием (двойное контрастирование) (позволяет определить распространенность и протяженность ЗНО желудка, а так же определить тактику хирургического вмешательства);
· ультразвуковая диагностика комплексная (печень, желчный пузырь, поджелудочная железа, селезенка, почек, надключичных л/узлов) (эхогенное наличие увеличенных л/узлов брюшной полости и забрюшинного пространства, наличие метастазов в брюшной полости, а так же прорастание ЗНО желудка в соседние структуры);
· компьютерная томография органов брюшной полости и забрюшинного пространства (более четка визуализация наличий увеличенных л/узлов брюшной полости и забрюшинного пространства, наличий метастазов в брюшной полости, а так же прорастание ЗНО желудка в соседние структуры).
· морфологическое исследование – основной метод дифференциальной диагностики рака пищевода с другими заболеваниями. Обнаружение в биоптате злокачественных клеток однозначно свидетельствует о раке пищевода, хотя отсутствие признаков опухоли в однократно полученном материале не исключает это заболевание. Только при многократных отрицательных результатах наряду с динамическим наблюдением можно считать патологический процесс доброкачественным.
Показания для консультации специалистов:
· консультация кардиолога (пациентам 50 лет и старше, так же пациенты моложе 50 лет при наличии сопутствующей патологии со стороны ССС или патологических изменении на ЭКГ);
· консультация невропатолога (при сосудистых мозговых нарушениях, в том числе инсультах, травмах головного и спинного мозга, эпилепсии, миастении, нейроинфекционных заболеваниях, а также во всех случаях потери сознания);
· консультация нейрохирурга (при наличии метастазов головной мозг, позвоночник);
· консультация эндокринолога (при наличии сопутствующей патологии эндокринных органов, например – сахарный диабет).
· Консультация других специалистов по поводу наличия сопутствующих патологий: гинеколога (острые и хронические заболевания женских половых органов), фтизиатра (туберкулез в анамнезе), инфекционист (хронический гепатиты) и др.
Дифференциальный диагноз
| Язвенная болезнь | Полипы желудка | Лимфома желудка | Саркома желудка |
| Для исключения злокачественного характера язвы необходима множественная биопсия по краям дефекта и из дна язвы. | Лишь аденоматозные полипы обладают высоким потенциалом к злокачественной трансформации. | Часто связана с инфекцией Helicobacter pylori. | Наиболее часто представлена лейомиосаркомой, занимающей переднюю или заднюю стенку желудка. |
| обязательно выполняют ФЭГДС и биопсию через 8— 12 нед после установления диагноза язвенной болезни. | Размер полипов варьирует от небольшого выбухания до крупных полипоидных масс, имитирующих рак желудка. | Характерны выраженная общая слабость, быстрая утомляемость, боли в эпигастральной области, чувство быстрого насыщения, анорексия. | Характеризуется медленным ростом, изъязвлением и кровоточивостью; поражение лимфатических узлов не характерно. |
| Необходимо помнить о возможности заживления язвенной формы рака желудка на фоне противоязвенной терапии. | Полипы, как правило, бывают случайной находкой при ФЭГДС или рентгеновском обследовании. | Для верификации и типирования необходима глубокая биопсия с иммуно- гистохимическим исследованием, наиболее часто речь идёт о В-клеточной лимфоме. | |
| Рекомендуют эндоскопическое удаление с гистологическим исследованием |
Лечение
Цели лечения:
· полное или частичное удаление органа со злокачественным новообразованием;
достижение полной или частичной регрессии, стабилизации опухолевого процесса
Тактика лечения**:
Выбор методов лечения рака желудка зависит от многих факторов, в том числе размеров самой опухоли, вовлечения в процесс других органов, тканей, лимфатических узлов. Важным моментом является наличие у пациента сопутствующих заболеваний (тяжелые болезни сердца, легких, почек). Специалисты учитывают все эти факторы. Для пациента разрабатывают индивидуальный план, который может состоять из хирургического лечения и/или химиотерапии.
Лечение в зависимости от стадии;
Стадии 0, I А, I В, IIА, IIВ:
· Дистальная субтотальная гастрэктомия.
· Проксимальная субтотальная гастрэктомия.
· Лапароскопическая гастрэктомия (при условии овладения техникой вмешательства и наличию соответствующего оборудования)
· Гастрэктомия (тотальная).
· Эндоскопическая мукозэктомия (Tis или T1а) при условии овладения техники проведения операций).
· Обязательным компонентом стандартных операций является лимфодиссекция в объеме D2. Стадии заболевания Т3, N1-2 предполагают курсы адъювантной полихимиотерапии.
Стадии IIIА, IIIВ, IIIС
· Гастрэктомия.
· Обязательным компонентом стандартных операций является лимфодиссекция в объеме D2. Установление до операции местнораспространенной формы (Т3-Т4), наличие метастазов в регионарных (N1-N2), а также низкодифференцированные гистологические формы опухолевого процесса предполагает проведение курсов (2-3) неоадъювантной лекарственной терапии при условии согласия пациентов на проведение лекарственной терапии в предоперационном режиме, а также отсутствием противопоказаний к ней (опухолевые стенозы, кровотечения и др.).
· Адъювантные курсы полихимиотерапии с учетом ответа опухоли на проводимую предоперационную лекарственную терапию.
Стадия IV
· Оперативное лечение с паллиативной целью, например при опухолевой обструкции, перфорации или сильного кровотечения. Может быть выполнена циторедуктивная гастрэктомия, гастро-энтероанастомоз. Лимфодиссекция не выполняется. Могут рассматриваться варианты гастростомии и/или еюностомии, а также стентирование при желудочной обструкции.
· Адъювантные курсы полихимиотерапии;
· Самостоятельные курсы паллиативной полихимиотерапии.
Рецидив
Хирургические вмешательства (индивидуализированно):
· различные по объему радикальные и паллиативные оперативные вмешательства;
· эндоскопическое разрушение опухоли;
· установка стентов.
Паллиативная химиотерапия (индивидуализированно).
Критерии эффективности лечения
Эффект от проведенного лечения оценивается по критериям ВОЗ:
Полный эффект – исчезновение всех очагов поражения на срок не менее 4х недель.
Частичный эффект – большее или равное 50% уменьшение всех или отдельных опухолей при отсутствии прогрессирования других очагов.
Стабилизация – (без изменений) уменьшение менее чем на 50% или увеличение менее чем на 25% при отсутствии новых очагов поражения.
Прогрессирование – увеличение размеров одной или более опухолей более 25% либо появление новых очагов поражения.
Медикаментозное лечение:
Химиотерапия – это медикаментозное лечение злокачественных раковых опухолей, направленное на уничтожение или замедление роста раковых клеток с помощью специальных препаратов, цитостатиков. Лечение рака химиотерапией происходит систематически по определенной схеме, которая подбирается индивидуально. Как правило, схемы химиотерапии опухолей состоят из нескольких курсов приема определенных комбинаций препаратов с паузами между приемами, для восстановления поврежденных тканей организма.
Существует несколько видов химиотерапии, которые отличаются по цели назначения:
· неоадъювантная химиотерапия опухолей назначается до операции, с целью уменьшения неоперабельной опухоли для проведения операции, а так же для выявления чувствительности раковых клеток к препаратам для дальнейшего назначения после операции.
· адъювантная химиотерапия назначается после хирургического лечения для предотвращения метастазирования и снижения риска рецидивов.
· лечебная химиотерапия назначается для уменьшения метастатических раковых опухолей.
В зависимости от локализации и вида опухоли химиотерапия назначается по разным схемам и имеет свои особенности.
Показания к химиотерапии:
· гистологически верифицированные ЗНО желудка;
· при лечении нерезектабельных опухолей;
· отдаленные метастазы или отдаленных лимфатических узлах;
· рецидив опухоли;
· удовлетворительная картина крови у пациента: нормальные показатели гемоглобина и гемокрита;
· сохраненная функция печени, почек, дыхательной системы и ССС;
· возможность перевода неоперабельного опухолевого процесса в операбельный;
· отказ пациента от операции;
· улучшение отдаленных результатов лечения при неблагоприятных гистотипах опухоли (низкодифференцированный, недифференцированный).
Противопоказания к химиотерапии:
Противопоказания к химиотерапии можно разделить на две группы: абсолютные и относительные.
Абсолютные противопоказания:
· гипертермия >38 градусов;
· заболевание в стадии декомпенсации (сердечно – сосудистой системы, дыхательной системы печени, почек);
· наличие острых инфекционных заболеваний;
· психические заболевания;
· неэффективность данного вида лечения, подтвержденная одним или несколькими специалистами;
· распад опухоли (угроза кровотечения);
· тяжелое состояние больного по шкале Карновского (таблица см. приложение 1) 50% и меньше.
11. FOLFOX
Оксалиплатин 100мг/м2 в/в 1-й день+кальция фолинат 200мг/м 2 2-час. инфузия 1-2 день +5Fu 400мг/м 2 болюсно 1-2 день +5Fu 600мг/м 2 22-час.инфузия в 1-2 день, каждые 2 недели;
13. CapOX(XELOX): оксалиплатин 130мг/м 2 в/в в 1-й день + кабецитабин по 1000мг/м 2 2 раза в день с 1 по14-й день, каждые 3 недели;
Функционирующие НЭО G1-G3: аналоги соматостатина (симптоматическая терапия).
Октреотид 0,1 мг п/к 3 раза в сутки в течение короткого периода времени (примерно 2 недели) с целью оценки его эффективности и общей переносимости,
затем Октреотид 20 мг внутримышечно 1раз/28 дней
Если в течение 3 месяцев обеспечивается адекватный контроль клинических проявлений и биологических маркеров заболевания – октреотид 10 мг внутримышечно 1раз/28 дней.
Если в течение 3 месяцев обеспечивается только частичный контроль клинических проявлений и биологических маркеров заболевания – октреотид 30 мг внутримышечно каждые 4 недели.
Распространенные нейроэндокринные опухоли толстой кишки или с неизвестной локализацией первичной опухоли – октреотид 30 мг внутримышечно 1раз/28 дней до прогрессирования.
Нефункционирующие НЭО
Ki67 20%, G3:
1) карбоплатин/цисплаин+этопозид,
2) темозоломид+бевацизумаб,
3) темозоломид+капецитабин+бевацизумаб,
4) аналоги соматостатина
Особый раздел неэпителиальных опухолей представляют GIST- недавно выделенная самостоятельная нозологическая единица, имеющая индивидуальные гистологические, иммуногистохимические и молекулярно-генетические признаки. Подавляющее большинство GIST (>90%) являются злокачественными. Подтверждением диагноза стромальных опухолей служит выявление в опухолевых клетках экспрессии рецептора Kit (CD117) иммуногистохимическим методом. В случаях первично операбельных GIST показано радикальное удаление опухоли. Использование иматиниба с адъювантной целью 400мг/сут внутрь в течение 1 года или до прогрессирования
При резистентности к иматинибу целесообразно увеличение дозы препарата до 800мг/сут. Получены обнадеживающие результаты использования после прогрессирования на фоне лечения иматинибом во второй линии терапии сунитиниба (в монорежиме или в комбинации с иматинибом).
Сунитиниб применяют в дозе 50мг/сут перорально ежедневно в течение 4 нед, затем следует 2-недельный перерыв с возобновлением терапии.
Другие виды лечения: нет.
Хирургическое вмешательство:
Хирургическое вмешательство, оказываемое в амбулаторных условиях: нет.
Хирургическое вмешательство, оказываемое в стационарных условиях:
Виды хирургических вмешательств:
· комбинированная расширенная гастрэктомия с лимфодиссекцией D-2;
· проксимальная субтотальная гастрэктомия;
· дистальная субтотальная гастрэктомия;
· лапароскопическая гастрэктомия.
Показания к хирургическому лечению:
· гистологически верифицированные операбельные ЗНО желудка;
· при отсутствии противопоказании к хирургическому лечению.
Противопоказания к хирургическому лечению при ЗНО желудка:
· наличие у больного признаков неоперабельности и тяжелой сопутствующей патологии;
· при отделенных метастазах (в печень, легкие, головной мозг и т.д.);
· при отделенных метастазах в лимфатические узлы шеи;
· при наличии опухолевых клеток в асцитической жидкости;
· обширные гематогенные метастазирования, диссеминированного опухолевого процесса;
· хронические декомпенсированные и/или острые функциональные нарушения дыхательной, сердечно-сосудистой, мочевыделительной системы;
· аллергия на препараты, используемые при общей анестезии.
Паллиативная помощь:
· При выраженном болевом синдроме лечение осуществляется в соответствии с рекомендациями протокола «Паллиативная помощь больным с хроническими прогрессирующими заболеваниями в инкурабельной стадии, сопровождающимися хроническим болевым синдромом», утвержден протоколом заседания Экспертной комиссии по вопросам развития здравоохранения МЗ РК №23 от «12» декабря 2013 года.
· При наличии кровотечения лечение осуществляется в соответствии с рекомендациями протокола «Паллиативная помощь больным с хроническими прогрессирующими заболеваниями в инкурабельной стадии, сопровождающимися кровотечением», утвержден протоколом заседания Экспертной комиссии по вопросам развития здравоохранения МЗ РК №23 от «12» декабря 2013 года.
Препараты (действующие вещества), применяющиеся при лечении
| Бевацизумаб (Bevacizumab) |
| Дакарбазин (Dacarbazine) |
| Доцетаксел (Docetaxel) |
| Иматиниб (Imatinib) |
| Интерферон альфа (Interferon alfa) |
| Иринотекан (Irinotecan) |
| Кальция фолинат (Calcium folinate) |
| Капецитабин (Capecitabine) |
| Карбоплатин (Carboplatin) |
| Натрия фолинат (Sodium folinate) |
| Оксалиплатин (Oxaliplatin) |
| Октреотид (Octreotide) |
| Сунитиниб (Sunitinib) |
| Темозоломид (Temozolomide) |
| Трастузумаб (Trastuzumab) |
| Фторурацил (Fluorouracil) |
| Цисплатин (Cisplatin) |
| Эверолимус (Everolimus) |
| Эпирубицин (Epirubicin) |
| Этопозид (Etoposide) |
Группы препаратов согласно АТХ, применяющиеся при лечении
Госпитализация
Показания для госпитализации с указанием типа госпитализации:**
Показания для плановой госпитализации:
Наличие у больного морфологически верифицированного ЗНО желудка, подлежащего специализированному лечению.
Показания для экстренной госпитализации: нет.
Профилактика
Информация
Источники и литература
Информация
Список разработчиков протокола с указание квалификационных данных:
1. Абзалбек Естай Шайхибекулы – кандидат медицинских наук, РГП на ПХВ «Казахский научно – исследовательский институт онкологии и радиологии», врач центра торакальной онкологии;
2. Туманова Асель Кадырбековна – кандидат медицинских наук, РГП на ПХВ «Казахский научно – исследовательский институт онкологии и радиологии», руководитель центра дневного стационара химиотерапии – 1;
3. Табаров Адлет Берикболович – клинический фармаколог, РГП на ПХВ «Больница медицинского центра Управление делами Президента Республики Казахстан», начальник отдела инновационного менеджмента.
Указание на отсутствие конфликта интересов: нет.
Рецензенты: Ижанов Ерген Бахчанович – доктор медицинских наук, главный научный сотрудник отдела хирургии желудочно-кишечного тракта и эндокринных органов «Национальный научный центр хирургии».
Указание условий пересмотра протокола: пересмотр протокола через 3 года после его опубликования и с даты его вступления в действие или при наличии новых методов с уровнем доказательности.
Приложение 1
Шкала Карновского