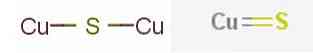Готовые домашние задания, готовые задачи по химии и биологии
Свойства и получение сульфидов
Задача 851.
Почему сульфид цинка растворяется в соляной кислоте, а сульфид меди нет? В какой кислоте можно растворить сульфид меди?
Решение:
Взаимодействие сульфида цинка с соляной кислотой выражается уравнением:
ZnS(к) + 2HCl ↔ ZnCl2 + H2S(г)
ZnS + 2H + ↔ Zn 2+ + H2S
S 2- + Zn 2+ ↔ ZnS(к);
S 2- + 2Н + ↔ Н 2 S(г).
S 2- +Cu 2+ ↔ CuS(к);
S 2- + 2Н + ↔ Н2S(г).
Задача 852.
Каковы продукты реакции взаимодействия хлорида железа (III): а) с сероводородом; б) с сульфидом аммония?
Решение:
а) Хлорид железа (III) и сероводород реагируют с образованием хлорида железа (II), серы и хлороводорода:
Данная реакция протекает по окислительно-восстановительному механизму, где роль окислителя играет FeCl3, а восстановителя – H2S.
б) Между хлоридом железа (III) и сульфидом аммония протекает реакция по обменному механизму с образованием сульфида железа (III) и хлорида аммония:
Задача 853.
Объяснить, почему ZnS и РbS можно получить обменной реакцией в водном растворе, а Al2S3 и Cr2S3 нельзя. Указать способ получения Al2S3 и Cr2S3.
Решение:
Малорастворимые сульфиды металлов можно осадить из растворов солей действием сероводорода или сульфида аммония:
Являясь солями слабой кислоты, растворимые сульфиды подвергаются гидролизу. Гидролиз сульфидов, содержащих элементы в высоких степенях окисления Al2S3 и Cr2S3 и др.), часто идет до конца, он необратим. Поэтому Al2S3 и Cr2S3 нельзя получить обменной реакцией в водном растворе. Обычно для их получения используют сплавление метала с серой в отсутствие кислорода и влаги:
2Al + 3S 
2Cr + 3S 
Сульфид хрома поучают:
Сплавление оксида хрома(III) с сероводородом:
2Cr2O3 + 9S 
Пропускание сероводорода через нагретый оксид хрома(III):
Cr2O3 + 3H2S 
Задача 854.
Какова реакция среды в растворах: а) Na2S; 6) (NH4)2S; в) NaНS?
Решение:
а) Na2S – соль сильного основания и слабой кислоты, гидролизующаяся по аниону:
Na2S ↔ 2Na + + S 2- ;
S 2- + H2O ↔ HS — + OH — (ионно-молекулярная форма);
Na2S + H2O ↔ NaHS + NaOH (молекулярная форма).
б) (NH4)2S – соль слабого однокислотного основания и слабой двухосновной кислоты, гидролизуется как по катиону, так и по аниону:
(NH4)2S ↔ 2NH4 + + S 2- ;
NH4 + + H2O ↔ NH4OH + H + (ионно-молекулярная форма);
S 2- + H2O ↔ HS — + NH4OH (ионно-молекулярная форма).
Н + + ОН — ↔ Н2О
в) NaНS – кислая соль слабой кислоты и сильного основания, которая будет гидролизоваться по аниону:
NaHS ↔ Na + + HS — ;
HS — + H2O ↔ H2S + OH — (ионно-молекулярная форма);
NaHS + H2O ↔ H2S + NaOH (молекулярная форма).
Сульфид меди свойства, риски и использование
сульфиды меди описать семейство химических соединений и минералов с формулой CuхSи. Эти соединения включают в себя экономически важные минералы и синтетические материалы.
Наиболее известные минералы сульфида меди включают сульфид меди (I) или сульфид меди химической формулы.2S содержится в минерале калькозин и сульфид меди (II) или сульфид меди формулы CuS, обнаруженной в минерале ковелита.
Калькозин добывался веками и является одной из самых прибыльных медных руд. Причины этого обусловлены его высоким содержанием меди (атомное соотношение 67% и почти 80% по массе) и легкостью, с которой медь можно отделить от серы.
Тем не менее, это не основной минерал меди из-за его дефицита. Хотя самые богатые залежи кальцизина были добыты, он, вероятно, все еще разрабатывается и, несомненно, будет добываться в будущем (МИНЕРАЛЬНЫЙ ХАЛКОЦИТ, 2014).
Ковелит не является распределенным минералом, но его радужные чары могут очаровывать восхищение любого, кто видит синие кристаллы индиго. Хотя хорошие кристаллы редки, именно блеск и цвет этого минерала делают его замечательным (THE MINERAL COVELLITE, 2014).
В горнодобывающей промышленности минералы борнита или халькопирита, которые состоят из смешанных сульфидов меди и железа, часто называют «сульфидами меди»..
Физико-химические свойства сульфидов меди
Сульфид меди (I) и (II) имеют одинаковый внешний вид, оба являются кристаллами темного, серого или черного цвета..
Эти соединения могут быть дифференцированы по их кристаллической структуре. Сульфид меди (I) имеет моноклинную структуру, а сульфид меди (II) имеет гексагональную структуру (Национальный центр биотехнологической информации, S.F.).
Они имеют молекулярную массу 159,16 г / моль и 95 611 г / моль и плотность 5,6 г / мл и 4,76 г / мл для случая сульфида меди (I) и (II) соответственно (Национальный центр Биотехнология Информация, SF).
Сульфид меди (I) имеет температуру плавления 1100 ° C и нерастворим в воде и уксусной кислоте, частично растворим в гидроксиде аммония (Royal Society of Chemistry, 2015).
Сульфид меди (II) имеет температуру плавления 220 ° C, где он разлагается, нерастворим в воде, соляной и серной кислотах и растворим в азотной кислоте, гидроксиде аммония и цианиде калия (Royal Society of Chemistry, 2015 ).
Перекись водорода активно реагирует с сульфидом меди (II) и взрывается при контакте с концентрированным раствором хлористой кислоты или хлоратов кадмия, магния или цинка.
Реактивность и опасности
Сульфиды меди (I) и (II) не классифицируются как опасные, однако они могут быть токсичными при попадании в организм вследствие образования сероводорода. Симптомы включают в себя рвоту, желудочную боль и головокружение, могут вызвать раздражение кожи и глаз, а вдыхание может вызвать раздражение дыхательных путей (ПАСПОРТ БЕЗОПАСНОСТИ МАТЕРИАЛА Copper Sulfide, 1995).
В случае воздействия тепла он может выделять токсичные пары серы или оксида меди, которые могут быть вредными для здоровья..
В случае попадания в глаза их следует немедленно промыть достаточным количеством воды в течение 15 минут, периодически поднимая нижнее и верхнее веко..
В случае попадания на кожу немедленно промыть большим количеством воды в течение 15 минут, снимая загрязненную одежду..
В случае проглатывания следует немедленно вызвать токсикологический центр. Прополоскать рот холодной водой и дать пострадавшему 1-2 стакана воды или молока для питья. Рвота должна быть вызвана немедленно.
В случае вдыхания пострадавшего следует доставить в прохладное место. Если не дышите, сделайте искусственное дыхание (Copper (II) Sulfide, 2009).
приложений
Сульфид меди (I) используется в качестве полупроводника и в фотографических целях (americanelements, 1998-2017). Его применение также включает использование в солнечных элементах, светящихся красках, электродах и некоторых разновидностях твердых смазочных материалов (Britannica, 2013)..
С другой стороны, сульфид меди (II) находит применение в солнечных элементах, суперионных проводниках, фотоприемниках, электропроводящих электродах, фототермических преобразовательных устройствах, микроволновых защитных покрытиях, активных поглотителях радиоволн, газовых сенсорах и поляризаторах излучения. инфракрасный (азом, 2013).
Также сульфид меди (II) (ковелит) используется при исследовании наночастиц:
В работе Geng Ku (2012) было продемонстрировано использование полупроводниковых наночастиц сульфида меди (НЧ CuS) для визуализации фотоакустических томографий на Nd: YAG-лазере на длине волны 1064 нм..
CuS NP позволил визуализировать