Актуальные вопросы тяжелой герпетической инфекции у взрослых
В настоящее время неуклонно увеличивается число больных рецидивирующей герпетической инфекцией, вызванной вирусами простого герпеса (ВПГ) 1 и 2 типа различной локализации. Наиболее распространенная локализация у взрослых лиц — аногенитальная и лабиальная
В настоящее время неуклонно увеличивается число больных рецидивирующей герпетической инфекцией, вызванной вирусами простого герпеса (ВПГ) 1 и 2 типа различной локализации. Наиболее распространенная локализация у взрослых лиц — аногенитальная и лабиальная. Многие вопросы патогенеза и терапии тяжелого и крайне-тяжелого течения герпесвирусной инфекции по-прежнему не решены.
Вид ВПГ относится к семейству Herpesviridae, подсемейству L-Herpesviridae, виду ВПГ. Различают два основных типа вируса — ВПГ 1 и ВПГ 2. Инфицирование возможно как одним, так и двумя типами возбудителя. ВПГ способен внедряться в различные клетки организма человека: в клетки кожи, слизистых оболочек урогенитального и желудочно-кишечного трактов (ЖКТ), дыхательных путей, центральной и периферической нервной системы, печени, эндотелия сосудов, а также в клетки крови — лимфоциты и др. [1]. Место постоянного обитания (пожизненного персистирования) ВПГ — паравертебральные сенсорные ганглии. ВПГ передается прямым контактным путем, возможна передача возбудителя контактно-бытовым и вертикальным путем (от матери к плоду), а также трансфузионным и парентеральным путями через инструменты при оперативных вмешательствах, стоматологических процедурах и т. д.
Как известно, большинство людей инфицированы ВПГ. Первичный иммунный ответ на инфекцию протекает латентно или с герпетическими высыпаниями с местной и общей воспалительной реакцией. У лиц с нормальным иммунным ответом размножение (репликация) ВПГ находится под иммунологическим контролем, и рецидивы бывают крайне редко или не возникают в течение всей жизни. В противовирусной защите организма участвуют факторы неспецифической защиты, уничтожающие или блокирующие вирусы: макрофаги и другие клетки-продуценты интерферонов (ИФН) α, β и γ, ряд интерлейкинов (ИЛ) (фактор некроза опухоли (ФНО), ИЛ-6 и др.), естественные киллеры и факторы, формирующие специфический иммунный ответ против конкретного вируса: цитотоксические Т-лимфоциты (ЦТЛ) (CD 8+ Т-лимфоциты) и В-лимфоциты, ответственные за продукцию специфических антител, блокирующих репликацию вируса и расположенные вне клетки вирусы. Для адекватного функционирования этих клеток и поддержания иммунного ответа необходима соответствующая продукция ИФН и ИЛ.
Под влиянием различных экзогенных и эндогенных факторов, повреждающих иммунную систему, возможно ослабление контроля над репликацией вируса и соответственно развитие рецидива. Рецидив ВПГ-инфекции могут спровоцировать другие инфекционные заболевания, переохлаждение, чрезмерная инсоляция, психические или физические стрессы, интоксикации различного генеза, в том числе употребление алкоголя, циклические изменения гормонального статуса (менструации), особенно при дисбалансе уровня гормонов у женщин, резкая смена климатических поясов и др.
При длительной хронической инфекции вирусы оказывают многостороннее неблагоприятное действие на иммунную систему человека. ВПГ прямо повреждают клетки иммунной системы (лимфоциты, макрофаги и естественные киллеры). Синтезируя белки-супрессоры и химерные белки, вирусы угнетают многие реакции иммунитета: ВПГ могут блокировать действие ИФН, нарушать распознавания инфицированных клеток и другие защитные реакции. Кроме того, высокая мутационная активность вирусного генома также способствует ускользанию вируса от иммунологического контроля.
Хроническая, часто рецидивирующая ВПГ-инфекция может провоцировать развитие аутоиммунных состояний (антифосфолипидный синдром, аутоиммунный тиреоидит, аутоиммунные васкулиты и др.). Кроме того, при интеграции ВПГ в генетический аппарат клеток возможна неопластическая трансформация клеток. Так, ВПГ является одним из факторов повышенного риска развития рака тела и шейки матки и других онкологических заболеваний. Также ВПГ-инфекция является одной из ведущих причин самопроизвольных абортов, преждевременных родов, рождения детей с патологией центральной нервной системы и внутренних органов. ВПГИ ассоциирована со многими «болезнями цивилизации» — атеросклерозом, ишемической болезнью сердца у лиц моложе 50 лет и др. Тяжелое течение ВПГИ может быть маркером онкологических заболеваний и СПИДа [7].
В зависимости от числа и выраженности рецидивов, выделяют легкое, среднетяжелое и тяжелое течение болезни (табл. 1).
При тяжелом течении ВПГ-инфекции возможно одновременное появление нескольких очагов поражения (например, в области половых органов, губ, крыльев носа), а также последовательное возникновение высыпаний разной локализации (один рецидив на фоне другого), продолжительность обострения при этом может достигать 16–20 дней. В месте высыпания больные ощущают жар, жжение, боль, напряжение и/или зуд кожи. На инфильтрированной коже появляется группа пузырьков, заполненных прозрачным содержимым. Пузырьки могут сливаться в сплошной многокамерный элемент. Прозрачное их содержимое затем мутнеет. Пузырьки в дальнейшем вскрываются, образуя мелкие эрозии, или подсыхают и превращаются в корочки. Возможно наслоение вторичной бактериальной инфекции. При рецидивах ВПГ часто поражает одни и те же участки кожи. Как правило, при тяжелом течении инфекции значительно ухудшается физическое и психическое состояние больных. У части пациентов в период рецидива увеличиваются или появляются слабость, лихорадка, озноб, миалгии, цефалгии, артралгии, раздражительность, нарушение сна, эмоциональная лабильность, также могут развиваться тяжелые депрессивные состояния, требующие медикаментозной коррекции. По данным органов здравоохранения США, ВПГ-инфекция аногенитальной локализации является примерно в 10% случаев причиной депрессий и суицидов. Тяжелое течение генитальной формы ВПГ-инфекции с частыми рецидивами приводит к нарушению нормальной половой функции пациента, болезнь нередко создает конфликтные ситуации в семье, на работе. Лечение больных с тяжелым течением ВПГ-инфекции представляет собой сложную задачу и должно включать как медикаментозную терапию, так и психологическую адаптацию пациента.
У больных с тяжелой ВПГ-инфекцией в большинстве случаев не наблюдается стойкого и значимого клинического эффекта в ответ на эпизодические курсы комбинированной терапии (противовирусные и иммунотропные средства, общеукрепляющие препараты). Как правило, такие больные меняют много лечебных учреждений в поисках адекватной помощи.
С течением заболевания появляется много побочных реакций на медикаменты или их непереносимость, в ряде случаев развивается устойчивость ВПГ к ацикловиру, ИФН a, другим средствам. Иммуностимуляторы, используемые эмпирически, могут приносить облегчение в период их приема, но во многих случаях они оказываются неэффективными и даже ухудшают клиническое течение болезни. Усугубляются проявления вторичного иммунодефицита, присоединяются другие инфекции, субдепрессивные состояния переходят в стойкие нарушения психики, теряется вера больных в выздоровление, в возможность современной медицины им помочь.
Для разработки современных подходов к лечению и контролю над ВПГ-инфекцией и более углубленного понимания патогенеза заболевания нами было изучено состояние различных звеньев противовирусной защиты и системы цитокинов у больных с тяжелым и крайне тяжелым течением ВПГ-инфекции аногенитальной и лабиальной локализации, а также степень инфицированности (системности заболевания) и частота сочетания с другими герпесвирусными инфекциями.
Обследовано 102 больных, страдающих тяжелой ВПГ-инфекцией более 2 лет (28 мужчин и 74 женщины, средний возраст — 34 ± 1,5 года) и имеющих частоту рецидивов более шести в год.
При этом у 60 больных наблюдалось от 6 до 11 рецидивов ВПГ-инфекции в год, а у 42 больных — от 12 до 20 рецидивов. У большинства пациентов преобладала аногенительная или смешанная локализация герпеса. Средняя длительность тяжелого течения заболевания составила 9,3 ± 1,2 года. Группу контроля составили 32 практически здоровых добровольца (14 мужчин и 18 женщин, средний возраст — 32 ± 1,6 года). Анализ ряда изучаемых параметров включал результаты обследования пациентов с легким течением заболевания (36 человек — 10 мужчин, 26 женщин, средний возраст — 33,4 ± 2,1 года, с частотой рецидивов 2,9 ± 0,8 в год). При рецидивах жалобы больных были характерными. Часто встречались депрессия, раздражительность, снижение памяти и другие нарушения физического и психического состояния и познавательных функций.
У многих больных в анамнезе были указания на повторные курсы противовирусной и/или иммунотропной терапии, оказывавшей неоднозначное влияние: или кратковременное положительное влияние на течение ВПГ-инфекции, или ухудшение и развитие рецидива на фоне или после отмены иммунокоррекции. Такие анамнестические данные отражают тяжесть иммунной недостаточности и неадекватность проводимой эмпирической терапии без оценки иммунного статуса и индивидуального подбора иммунокорректоров, а также восстановительной терапии — иммунореабилитации [5].
При обследовании больных с тяжелым течением ВПГ-инфекции выявлялись многие маркеры вторичного иммунодефицита в виде хронических инфекционно-воспалительных заболеваний различной локализации, со смешанным характером микрофлоры и в большинстве случаев ее устойчивостью к повторным курсам антибиотикотерапии. Из 102 больных хронической ВПГ-инфекцией тяжелого течения выявлены:
Эти данные свидетельствуют о необходимости комплексного подхода к лечению ВПГ-инфекции тяжелого течения с учетом осложнений вторичного иммунодефицита.
Кроме того, проводили ПЦР-исследование биологических материалов на наличие ДНК ВПГ 1 и 2 типа и других вирусов герпес-группы: цитомегаловируса, вируса герпеса человека (ВГЧ) 6 типа, вируса Эпштейна–Барр. Используемые нами программы амплификации позволяли выявлять ДНК вирусов на уровне, соответствующем активной их репликации. Наличие активной репликации вирусов подтверждали полуколичественным ПЦР-исследованием и серологическими тестами.
В результате исследования у больных с тяжелым течением ВПГ-инфекции обнаружены лабораторные признаки вторичного иммунодефицита.
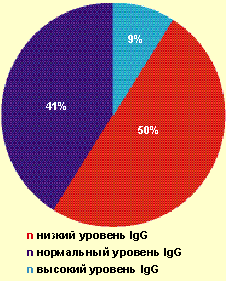 |
| Рисунок 1. Частота выявления различных значений IgG у больных с тяжелым течением ВПГ-инфекции |
Так, у большинства пациентов (91%) отсутствовало адекватное повышение продукции IgG в ответ на рецидив ВПГ-инфекции (рис. 1). При частоте рецидивов ВПГ-инфекции 6–11 рецидивов в год низкий уровень IgG выявлялся у 25% больных, при частоте — 12–20 рецидивов в месяц — уже у 64,3% больных. Более чем у 70% больных был повышен уровень ЦИК в 1,5–2,0 раза от показателей нормы. Известно, что длительная циркуляция ЦИК может приводить к отложению их на эндотелии сосудов и служить одним из факторов формирования аутоиммунной патологии.
У большинства больных с ВПГ-инфекцией тяжелого течения (70%) были обнаружены нарушения в системе естественной и/или специфической цитотоксичности (рис. 2) — снижение содержания зрелых активированных естественных киллеров CD16 + (менее 11%), Т-киллеров и/или ЦТЛ CD8 + (менее 27%). Важно отметить, что выраженное снижение уровня CD8 + (в состав которых входят также и супрессорные клетки) в большинстве случаев сочеталось с повышением уровня CD4 + и иммунорегуляторного индекса, что является фактором риска в отношении формирования аутоиммунных процессов. Как известно, системы естественной и специфической цитотоксичности играют ведущую роль в противовирусной защите.
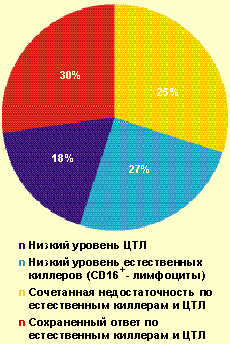 |
| Рисунок 2. Частота выявления нарушений в системе естественной и специфической цитотоксичности у больных с тяжелым течением ВПГ-инфекции (n = 102) |
Обнаруженные нарушения в системах цитотоксичности и их активационных маркерах при ВПГ-инфекции косвенно свидетельствуют о недостаточном уровне продукции Т-хелперами 1 типа ИЛ-2 — одного из важнейших звеньев цитокиновой сети, необходимого для полноценного противовирусного иммунного ответа.
При исследовании функционального состояния нейтрофилов у больных с тяжелым течением ВПГ-инфекции повышение спонтанного НСТ-теста было выявлено почти в половине случаев. Однако показатели стимулированного НСТ-теста и индекса стимуляции, напротив, были существенно снижены у большинства больных, что свидетельствует об истощении у них резервных способностей нейтрофилов.
Н. А. Дидковский, доктор медицинских наук, профессор
И. К. Малашенкова, кандидат медицинских наук
Ж. Ш. Сарсания, кандидат биологических наук
А. Н. Танасова, И. Н. Зуйкова, И. А. Зуйков, Н. М. Хитрик
НИИ физико-химической медицины, ММА им. И. М. Сеченова, Москва
Герпес: что это и какие препараты применять?
Герпес в переводе с греческого «ползущий». На данный момент актуальность этого заболевания не уменьшилась. Оно встречается более чем у 90% населения.
Что такое герпес
Как понять, что это именно герпес?
Но для достоверного подтверждения диагноза необходим анализ крови на наличие специфической реакции организма на вирус (IgM) он будет говорить о том, что на момент сдачи крови у вас протекает острый период болезни.
При генитальном герпесе, также берут на исследование выделения из половых путей и уретры. Обязательна консультация специалиста (дерматовенеролога).
Стоит обратить внимание, что вирус не выводится из организма после перенесенной ветрянки, а остается «жить» в определенном отделе нашей нервной системы, поэтому сдавать анализ на Ig G не имеет смысла.
Как можно заразиться
Заражение происходит через слизистые:
То есть чаще всего заражение происходит при несоблюдении гигиены и защиты при половом акте. Так же при расчесывании уже появившихся пузырьков происходит занос на новые участки кожи и слизистых.
Отдельный путь заражения от матери к плоду, на данный момент является обязательным обследование на ВПГ-1,2 у планирующих беременность и беременных женщин.
Инфекция поражает нервную систему и опасна своими последствиями для организма.
Как себя вести при герпесе

Препараты
Рассмотрим подробно группы препаратов для лечения
Данная группа препаратов воздействуют непосредственно на причину, сам вирус. Курс и схему приема назначает после комплексного обследования.
Переносимость препаратов достаточно хорошая, противопоказаны при беременности и кормлении грудью. Так же осторожно и под контролем врача применение у лиц с почечной и печеночной недостаточностью. Детям дозу определяет педиатр исходя из расчета по весу.
2. Препараты интерферона:
Противопоказаний у данной группы практически нет. Она является основным способом лечения такой уязвимой группы как беременные и кормящие женщины.
Используют для стимуляции выработки собственного интерферона и избежания усугубления течения и распространения инфекции. Переносится достаточно хорошо. Противопоказания у каждого препарата определенный возраст указанный в инструкции.
Данные препараты применяются при герпетических поражения слизистой рта, обладают антибактериальным, противовирусным действием, а также снимают воспаление и обезболивают.
Обладают местным противовирусным действием, Зовиракс Дуо Актив в сочетании с гормоном гидрокортизоном дает быстрое снятие воспаления и соответственно боли, также не дает образоваться новым пузырькам. Но так как в составе гормональная составляющая, очень внимательно необходимо прочитать инструкцию. Только с 12 лет. Перед применением любых мазей и гелей необходимо очистить кожу от косметики и загрязнений.
Только под контролем иммунолога.
Снимают боль, воспаление и так же при необходимости температуру.
Помогают избежать отечности.
Также отдельно можно выделить вакцину против герпеса. Показана она взрослым, которые болеют герпесом более 3 раз в год и высоким титром антител, пожилым лицам, ВИЧ-инфицированным. Также детям которые не переболели ветрянкой.
Лечение беременных женщин выбирается в зависимости от срока беременности, строго акушером-гинекологом и зависит от степени тяжести течения!
Герпес-является комплексной проблемой. Причиной повторяющегося или впервые возникшего герпеса является снижение иммунитета, гормональные изменения.
Главной профилактикой является поддержание работы иммунитета:
Федеральные клинические рекомендации по ведению больных генитальным герпесом- Москва 2015; Клинические рекомендации простой герпес у взрослых-2014 год;
Современный взгляд на клиническое течение, диагностику и терапию генитального герпеса у женщин
Среди вирусных заболеваний инфекция, обусловленная вирусами простого герпеса (ВПГ), занимает одно из ведущих мест, что определяется повсеместным распространением вируса: 90% инфицированием ими человеческой популяции, пожизненной персистенцией ВПГ в органи
Среди вирусных заболеваний инфекция, обусловленная вирусами простого герпеса (ВПГ), занимает одно из ведущих мест, что определяется повсеместным распространением вируса: 90% инфицированием ими человеческой популяции, пожизненной персистенцией ВПГ в организме инфицированных, значительным полиморфизмом клинических проявлений герпетической инфекции, торпидностью к существующим методам лечения.
Генитальный герпес (ГГ), являясь частным случаем ВПГ-инфекции, относится к одному из наиболее распространенных заболеваний, передаваемых половым путем, и отличается от других болезней этой группы пожизненным носительством возбудителя в организме человека (латенцией), что обуславливает высокий процент формирования рецидивирующих форм болезни.
Заболеваемость ГГ во всем мире и в России постоянно растет, что в значительной мере связано с распространением бессимптомной и недиагностированной форм болезни, но этот объективный процесс, к сожалению, не сопровождается радикальным изменением отношения к этому заболеванию как врачей, так и населения.
Этиология. Патогенез
Различают две основные антигенные группы ВПГ: 1 и 2 типа. При этом штаммы, относящиеся к одному и тому же антигенному типу, могут отличаться по иммуногенности, вирулентности, устойчивости к воздействию различных химических и физических факторов, что, в конечном итоге, определяет особенности клинических проявлений болезни. Штаммы ВПГ-1 чаще удается выделить при поражении кожи лица, верхних конечностей, штаммы ВПГ-2 — при генитальной локализации очагов, хотя прямой связи между антигенной специфичностью и локализацией клинических проявлений герпеса не обнаруживается.
Источником ВПГ-инфекции является больной или вирусоноситель. Вирус передается воздушно-капельным, контактным, трансфузионным путями и при трансплантации органов. Во время беременности инфицирование плода может происходить трансплацентарным и трансцервикальным (восходящим) путями.
Установлено, что в 40% случаев первичное инфицирование ВПГ происходит воздушно-капельным путем в раннем детском возрасте, при этом источником инфекции, как правило, являются члены семьи, имеющие активные признаки герпетической инфекции (ГИ).
Основными звеньями патогенеза ГИ являются:
1) инфицирование сенсорных ганглиев вегетативной нервной системы и пожизненная персистенция ВПГ в них;
2) поражение иммунокомпетентных клеток, ведущее к вторичному иммунодефициту;
3) тропизм ВПГ к эпителиальным и нервным клеткам, обуславливающий полиморфизм клинических проявлений ГИ.
Вирус начинает размножаться в месте инокуляции — «входных воротах» инфекции (кожа, красная кайма губ, слизистые оболочки полости рта, половых органов, конъюктива), где появляются типичные пузырьковые высыпания, и проникает в кровяное русло и лимфатическую систему. На ранних этапах ГИ вирусные частицы внедряются также в нервные окончания кожи или слизистой оболочки, продвигаются центростремительно по аксоплазме, достигают периферических, затем сегментарных и регионарных чувствительных ганглиев центральной нервной системы, где они пожизненно сохраняются в латентном состоянии в нервных клетках.
Инфицирование сенсорных ганглиев является одним из важных этапов в патогенезе ГИ. При герпесе лица — это чувствительные ганглии тройничного нерва, при герпесе гениталий — ганглии люмбосакрального отдела позвоночника, служащие резервуаром вируса для его половой передачи. Распространение ВПГ в центробежном направлении во время рецидива определяет анатомическую фиксацию очагов поражения при рецидивах простого герпеса.
Рецидивирующее течение инфекции наблюдается у 30–50% населения, инфицированного ВПГ. Рецидивирующим герпесом (РГ) страдают представители всех возрастных групп.
Прогредиентное течение ВПГ-инфекции заключается в появлении более тяжелых клинических симптомов с увеличением длительности заболевания, а также вовлечении в инфекционный процесс органов и систем.
Обострения ГИ могут быть спровоцированы переохлаждением, инсоляцией, физической или психической травмой, приемом алкоголя, гормональными циклами.
Частота и интенсивность обострений при РГ варьируют в широких пределах и зависят от вирулентности и патогенности возбудителя, а также сопротивляемости организма человека. Заболевание чаще протекает как локальный процесс, высыпания обычно носят ограниченный, реже распространенный характер.
Таким образом, особенностями ГИ являются пожизненное носительство ВПГ в организме, рецидивирующий характер и прогредиентное течение заболевания.
Простой герпес может протекать в локальной и распространенной формах. Распространенная форма РГ встречается несколько реже локальной и характеризуется одновременным появлением нескольких очагов поражения на отдаленных участках кожно-слизистого покрова или вовлечением в патологический процесс прилежащих к очагу поражения тканей.
Появление у больных во время рецидивов наряду с герпетическими высыпаниями симптомов интоксикации, обусловленных вирусемией (общая слабость, недомогание, субфебрильная температура тела, увеличение и болезненность периферических лимфатических узлов) указывают на диссеминацию инфекционного процесса, на неспособность иммунной системы локализовать процесс, что может встречаться как при локальной, так и при распространенной формах РГ.
Рецидивирующие формы герпеса оказывают негативное воздействие на иммунную систему больного. ВПГ, развивающийся в иммунокомпетентных клетках крови, ведет к вторичному иммунодефициту, что клинически проявляется в частых простудных заболеваниях, снижении работоспособности, появлении субфебрильной температуры тела, лимфоаденопатии, психоастении. Рецидивирующий ГГ, нарушая нормальную половую жизнь пациентов, нередко является причиной нервно-психических расстройств, приводит к семейным неурядицам.
Вирусемия у женщин во время беременности может явиться причиной гибели плода, мертворождения: герпес-вирусы вызывают до 30% спонтанных абортов на ранних сроках беременности и свыше 50% поздних выкидышей, занимают второе место после вируса краснухи по тератогенности.
К настоящему времени получены доказательства, что ВПГ нередко является этиологическим фактором воспалительных заболеваний центральной нервной системы (менингоэнцефалит, ганглионеврит), ЛОР-органов, легких (хронический бронхит), сердечно-сосудистой системы (пери- и миокардит, возможно, ишемическая болезнь сердца), желудочно-кишечного тракта, мочеполовой системы. Поражение кожи и слизистых оболочек — самое распространенное клиническое проявление ГИ, а поражение ВПГ гениталий относится к одному из наиболее частых заболеваний, передающихся половым путем (ЗППП).
Клиника ГГ
Согласно существующей международной классификации различают первичный и рецидивирующий ГГ; последний, в свою очередь, подразделяется на типичную и атипичную клинические формы и бессимптомное вирусовыделение.
Термин «генитальный герпес» предполагает наличие очага поражения на коже и слизистых оболочках наружных половых органов. С развитием вирусологических методов исследований стали появляться сведения о «бессимптомных» и «атипичных» формах болезни. Диагноз «бессимптомная форма генитального герпеса» ставится на основании результатов вирусологического обследования при выделении ВПГ из отделяемого урогенитального тракта, при этом симптомы поражения кожи и видимых слизистых оболочек гениталий отсутствуют.
Диагноз «атипичная форма генитального герпеса» ставится гинекологами для обозначения хронического воспалительного процесса внутренних гениталий (кольпит, вульвовагинит, эндоцервицит и т. д.) при наличии лабораторно подтвержденной герпетической природы заболевания, в отличие от «типичной» картины болезни, при которой на слизистой оболочке этих органов имеются очаги поражения с везикулезно-эрозивными элементами. Вместе с тем из этой группы выпадают герпетические поражения уретры, анальной области и ампулы прямой кишки, хотя эти органы анатомически и функционально тесно связаны с половой сферой.
Инфицирование гениталий у взрослых обычно происходит в результате половых контактов. Самая высокая заболеваемость ГГ зарегистрирована в возрастной группе 20–29 лет. Повышенному риску развития ГГ подвергаются лица, начинающие половую жизнь в раннем возрасте и имеющие много половых партнеров.
Клинические проявления ГГ более выражены у серонегативных лиц, чем у серопозитивных, что свидетельствует о влиянии иммунного ответа, сформировавшегося на ГИ ВПГ-1 в детском возрасте, на тяжесть клинических проявлений герпеса при инфицировании гениталий ВПГ-2.
В большинстве случаев первичное инфицирование гениталий протекает бессимптомно, впоследствии превращаясь в латентное носительство герпес-вируса или в рецидивирующую форму ГГ. Однако в случаях клинически выраженного дебюта первичный ГГ обычно проявляется после 1–10-дневного инкубационного периода и отличается от последующих рецидивов более тяжелым и продолжительным течением.
Типичная клиническая картина первичного ГГ характеризуется появлением на слизистых оболочках половых органов и прилежащих участках кожи сгруппированных везикулезных элементов, возникающих на эритематозном фоне. Через 2–4 дня везикулы вскрываются, образуя мокнущие эрозии, реже — язвочки, эпителизирующиеся под коркой или без ее образования. Субъективно больных беспокоят зуд, жжение, болезненность в области очага поражения. У части больных отмечается повышение температуры тела до 38 °С, болезненное увеличение паховых лимфоузлов. Длительность острого периода при первичном ГГ может достигать 3–5 недель.
Рецидивирующий генитальный герпес (РГГ) является одним из самых распространенных инфекционных заболеваний мочеполовой системы.
Болезнь трудно поддается терапии, характеризуется хроническим течением, нарушением половой функции пациента, что нередко приводит к развитию неврастении. У женщин герпетические высыпания могут появляться на больших и малых половых губах, слизистой оболочке влагалища, шейки матки, в промежности и анальной области, нередко поражается кожа ягодиц и бедер. Заболевание сопровождается появлением и развитием симптомов интоксикации (субфебрильная температура, общая слабость и недомогание), увеличением и болезненностью паховых лимфатических узлов (чаще с одной стороны).
Для РГГ характерно раннее вскрытие везикул с образованием эрозивных поверхностей, выраженной субъективной симптоматикой (боль, зуд, жжение в очаге). РГГ отличается тяжелым течением; часто рецидивирующие формы болезни встречаются у 50–75% пациентов.
Типичная форма РГГ наружных гениталий характеризуется ярко выраженными симптомами болезни, классическим развитием очага поражения (эритема, образование везикул, развитие эрозивно-язвенных элементов, эпителизация) и субъективными ощущениями, проявляется повторяющимися пузырьковыми высыпаниями. Очаги поражения обычно носят ограниченный, реже распространенный характер и локализуются на одном и том же участке кожи или слизистой оболочки. Частые обострения РГГ нередко сопровождаются нарушением общего состояния больных. За 12–48 часов могут появляться местные и общие продромальные явления: зуд, чувство жжения, болезненность в местах будущих высыпаний, региональный лимфаденит, симптомы интоксикации, обусловленные вирусемией (головная боль, озноб, недомогание, субфебрильная температура).
Наличие везикулярных или эрозивных высыпаний на коже и слизистой гениталий, выраженная субъективная симптоматика (зуд, жжение) позволяет врачам визуально поставить диагноз РГГ, своевременно назначить лечение и информировать больного об инфекционном характере заболевания и опасности заражения полового партнера.
Необходимо отметить, что под воздействием проводимой терапии типично протекающий РГГ может значительно видоизменяться и приобретать абортивное течение. При этом элементы в очаге поражения минуют отдельные стадии развития. В этих случаях очаг поражения может быть представлен папулезным элементом, микроэрозией, отечным пятном на эритематозном фоне. Помощь в постановке диагноза при обращении больного с абортивно протекающим РГГ может оказать правильно собранный анамнез, в котором имеются указание на наличие у пациента в прошлом типичных для герпеса высыпаний.
Атипичные формы РГГ, в значительной мере осложняющие постановку диагноза, обусловлены рядом факторов:
1) изменением цикла развития герпетических элементов в очаге поражения;
2) необычной локализацией очага и анатомическими особенностями подлежащих тканей;
3) преобладанием субъективных ощущений в очаге.
При атипичных формах РГГ преобладает какая-либо из стадий развития воспалительного процесса в очаге (эритема, образование пузырей), либо один из компонентов воспаления (отек, геморрагия, некроз), или субъективная симптоматика (зуд), которые и дают соответствующее название атипичной форме РГГ (эритематозная, буллезная, геморрагическая, некротическая, зудящая). По интенсивности клинических проявлений атипичные формы могут протекать бурно как манифестные (буллезная, язвенно-некротическая) или как субклинические (микротрещины). И если при атипичных формах РГГ, проявляющихся образованием везикул и эрозий, в которые могут трансформироваться пузыри и язвы с присоединением, например, некротического компонента, можно заподозрить ГГ, то при клинических формах, которые не сопровождаются нарушением кожно-слизистого покрова или очаг поражения имеет непривычную форму, диагноз устанавливается с большим трудом.
Атипичные формы герпеса наружных гениталий у женщин встречаются чаще, чем у мужчин.
При отечной форме РГГ очаг поражения на слизистой оболочке вульвы представлен гиперемией и диффузным отеком.
Для «зудящей» формы РГГ характерно периодическое локальное появление выраженного зуда и (или) жжения в области наружных гениталий при незначительной гиперемии слизистой оболочки вульвы в очаге.
К атипичным формам РГГ относится и ВПГ-инфекция, проявляющаяся единичными глубокими рецидивирующими трещинами слизистой оболочки и подлежащих тканей малых и больших половых губ, сопровождающимися резкой болезненностью.
Субклиническая (малосимптомная) форма РГГ проявляется микросимптоматикой: кратковременным (менее суток) появлением одной или нескольких микротрещин, сопровождающихся незначительным зудом. Иногда субъективные ощущения отсутствуют, что снижает обращаемость больных в лечебные учреждения и затрудняет диагностику.
Субклиническая форма выявляется обычно при вирусологическом обследовании половых партнеров пациентов с каким-либо ЗППП или при обследовании супружеских пар с нарушением фертильности.
Клинический диагноз при абортивном течении, атипичной и субклинических формах рецидивирующего ГГ затруднен и может быть поставлен только при использовании вирусологических методов исследования.
В эпидемиологическом аспекте именно эти клинические формы ГГ являются наиболее опасными для распространения ГИ, когда на фоне минимальных клинических проявлений болезни происходит выделение ВПГ в окружающую среду, а отсутствие выраженной симптоматики позволяет больным вести активную половую жизнь и инфицировать половых партнеров.
Особенностью ГГ женских половых органов является многоочаговость. В патологический процесс нередко вовлекаются нижний отдел мочеиспускательного канала, слизистая оболочка ануса и прямой кишки. Вовлечение в инфекционный процесс этих органов может происходить вторично, вслед за возникновением герпеса наружных гениталий, а может протекать как изолированное поражение.
ГИ органов малого таза
По особенностям клинических проявлений герпетические поражения органов малого таза целесообразно разделить на:
1) герпес нижнего отдела урогенитального тракта, анальной области и ампулы прямой кишки;
2) герпес верхнего отдела полового тракта.
Герпес нижнего отдела урогенитального тракта, анальной области и ампулы прямой кишки. Поражение слизистых оболочек входа во влагалище, влагалищной части шейки матки, цервикального канала, уретры, мочевого пузыря, анальной области и ампулы прямой кишки. Проявляется в двух клинических формах: очаговой, характеризующейся появлением типичных для простого герпеса слизистых оболочек везикулезно-эрозивных элементов, и диффузной, при которой патологический процесс протекает по типу неспецифического воспаления.
Герпес уретры и мочевого пузыря. Герпетический уретрит субъективно проявляется болями и резями в начале мочеиспускания, дизурическими явлениями. При осмотре наблюдается гиперемия наружного отверстия уретры, наличие скудных слизистых выделений; при уретроскопии в передней части уретры иногда удается обнаружить мелкие поверхностные эрозии, катаральное воспаление. Ведущими симптомами герпетического цистита являются цисталгия, появление болей в конце мочеиспускания, дизурические явления.
Герпес анальной области и прямой кишки. Очаг поражения в анальной области обычно представляет собой рецидивирующую трещину, что нередко является поводом для диагностических ошибок. Такие больные с ошибочным диагнозом «трещина заднего прохода» попадают к хирургам. Зудящая форма герпеса ануса и герпетическое поражение геморроидальных узлов также трудны для диагностики.
Поражение анальной области может возникнуть первично, как самостоятельное заболевание, или вторично, в результате затекания отделяемого влагалища и мацерации слизистой оболочки ануса при наличии у пациентки герпетического кольпита, сопровождающегося обильной экссудацией.
При поражении сфинктера и слизистой оболочки ампулы прямой кишки (герпетический проктит) больных беспокоят зуд, чувство жжения и болезненность в очаге поражения, возникают мелкие эрозии в виде поверхностных трещин с фиксированной локализацией, кровоточащие при дефекации. При ректоскопии определяется катаральное воспаление, иногда эрозии.
Диагностировать герпетический проктит бывает особенно трудно. Мы наблюдали больных с рецидивирующим герпесом анальной области, у которых начало заболевания было связано с периодическим появлением скудных слизистых, иногда сукровичных выделений из прямой кишки, которые по времени совпадали с резкими распирающими болями в области сигмы и метеоризмом, сопровождавшимися сильным зудом в анальной области. В дальнейшем у этих пациенток стали появляться кровоточащие трещины в анальной области. На основании данных ретро- и колоноскопии (в ряде случаев с биопсией) и результатов вирусологического обследования этим больным был поставлен диагноз «герпетический проктит, рецидивирующий герпес анальной области».
Герпес верхнего отдела полового тракта (поражение матки, маточных труб). Типичная клиническая картина герпетических поражений органов верхнего отдела мочеполового тракта проявляется симптомами неспецифического воспаления. Обычно больные предъявляют жалобы на выделения из влагалища, периодически появляющиеся боли в малом тазу, области проекции матки, яичников. Эти пациентки длительное время без эффекта лечатся у гинекологов антибактериальными и противогрибковыми препаратами. При этом значительное число женщин, у которых отсутствуют выделения и субъективная симптоматика, вообще не обращаются к врачу и длительное время остаются источником распространения инфекции.
Такие диагнозы, как «ВПГ-эндометрит», «ВПГ-сальпингоофорит», врачами практически не ставятся. В то же время восходящие формы герпетического поражения внутренних половых органов у женщин подтверждаются обнаружением ВПГ в эндометрии, маточных трубах и крестцово-маточных связках. Установить реальную частоту поражения внутренних половых органов очень сложно, так как у 25–40%, а по некоторым данным, у почти 60% женщин заболевание протекает бессимптомно. Можно предположить, что эта патология встречается значительно чаще, чем диагностируется.
Для субклинической формы герпеса внутренних гениталий типично отсутствие у пациентки жалоб, иногда имеются указания на периодически появляющиеся необильные слизистые выделения из влагалища. При гинекологическом осмотре симптомы воспаления не выявляются. При динамическом лабораторном исследовании мазков отделяемого канала шейки матки, влагалища и уретры периодически выявляется повышенное количество лейкоцитов (до 200–250 и выше в поле зрения), свидетельствующее о наличии воспалительного процесса. При вирусологическом исследовании мазков методом иммунофлюоресценции в лейкоцитах определяется антиген ВПГ.
Бессимптомная форма герпеса внутренних гениталий характеризуется отсутствием у больных каких-либо жалоб на половую сферу, объективных клинических данных, подтверждающих воспаление. При лабораторном исследовании отделяемого урогенитального тракта выделяется ВПГ, в то время как в мазках признаков воспаления (лейкоцитоза) нет.
Бессимптомная форма герпеса внутренних гениталий выявляется у 20–40% женщин, страдающих РГ ягодицы и бедра. Это важное обстоятельство необходимо учитывать при планировании беременности у женщин с этой формой РГ в связи с существующей вероятностью развития во время беременности осложнений ВПГ-инфекции.
Осложнения ГГ
У каждой четвертой пациентки, страдающей РГГ, развиваются осложненные формы болезни. Осложнения могут быть локальные и системные.
К локальным осложнениям ГГ относится комплекс симптомов, состоящий из повышенного травматизма, сухости и образования болезненных кровоточащих трещин на слизистых оболочках наружных половых органов, возникающих при механическом раздражении. Эти симптомы появляются через несколько лет после начала заболевания и затрудняют половую жизнь пациенток. Наиболее часто поражается область задней спайки и слизистая оболочка входа во влагалище.
Вовлечение в инфекционный процесс нервной системы встречается у каждой третьей пациентки, страдающей ГГ, что обусловлено нейротропизмом ВПГ и тем фактом, что именно ганглии вегетативной нервной системы являются депо ВПГ в организме человека. Необходимо отметить, что болевой синдром при РГГ занимает особое место. При гинекологическом обследовании обращает на себя внимание частое отсутствие объективных данных, свидетельствующих о воспалении внутренних половых органов. При этом пациентки предъявляют жалобы на периодически возникающие тянущие боли внизу живота, в области проекции яичников, иррадиирующие в поясничную область и прямую кишку, боли в промежности. В ряде случаев болевой синдром может имитировать клинику «острого живота». Длительно существующий болевой синдром вызывает у пациентов снижение половой потенции и либидо.
Этот феномен, как правило, связан с имеющейся у больных специфической герпетической невралгией тазового нервного сплетения.
Особенности болевого синдрома при РГГ определяются свойствами нервных образований, вовлеченных в инфекционный процесс. Раздражение парасимпатических волокон вызывает у больных субъективные ощущения в виде жжения, являющегося патогномоничным симптомом при рецидивах ГГ. При герпесе бедер и ягодиц нередко встречается повышение поверхностной болевой чувствительности кожи (гиперестезия), субъективно воспринимаемое больным как покалывания, ощущение «ползания мурашек». Клинические проявления ганглиорадикулита проявляются тянущими болями по задней поверхности бедра, что обусловлено вовлечением в патологический процесс седалищного нерва.
Диагностика
Достоверно поставить диагноз ВПГ-инфекции позволяет только вирусологическое исследование.
Существующие методы лабораторной диагностики простого герпеса принципиально делятся на две группы:
1) выделение и идентификация ВПГ или выявление антигена возбудителя из инфицированного материала;
2) выявление вирусспецифических антител в сыворотке крови.
Материалом для лабораторного анализа может служить содержимое везикул, соскоб со дна эрозии, слизистой уретры, стенок влагалища, канала шейки матки, ануса, отделяемое урогенитального тракта, ампулы прямой кишки.
Частота выявления ВПГ в биоматериалах из различных отделов урогенитального тракта у женщин варьирует. Чаще вирус удается выделить из отделяемого канала шейки матки, реже из влагалища и уретры. Вирус редко определяется одновременно во всех образцах, полученных от больной, поэтому для уменьшения диагностических ошибок необходимо исследовать максимальное число образцов от одной пациентки.
Частота выделения ВПГ у женщин в значительной мере зависит от фазы менструального цикла. Более чем у 70% пациенток, страдающих простым герпесом, ВПГ выделяется в начале лютеиновой фазы. В это же время отмечается усиление клинических проявлений ВПГ-инфекции у основного числа больных. Реже ВПГ выделяется в пред- и постменструальном периодах (у 12–30% больных). Частота выявления ВПГ у больных в остальные дни менструального цикла снижается до 5–8%. Значительный разброс в выявлении антигена ВПГ у женщин в различные дни менструального цикла показывает, что отрицательный результат однократного вирусологического исследования не может исключить полностью диагноз ГГ. При подозрении на ВПГ-инфекцию необходимо проводить повторное (1 раз в 7 дней, 2–4 раза в течение месяца) вирусологическое исследование отделяемого мочеполовой системы у пациенток.
Выделение ВПГ на культуре клеток. При выделении вируса в культуре клеток диагноз ставится на основании характерного цитопатического действия, которое оказывает ВПГ на клетки. Для выделения ВПГ in vivo можно использовать 12–13-дневные куриные эмбрионы и лабораторных животных, у которых развиваются типичные для ВПГ-инфекции симптомы инфекции.
Серологические методы. Диагностическая ценность серологических методов при простом герпесе различна и зависит от формы инфекции (первичная, рецидивирующая), состояния реактивности организма больного, длительности заболевания и ряда других факторов.
В ответ на внедрение ВПГ в организме начинается продукция специфических иммуноглобулинов класса М (IgM), которые определяются на 4–6 день после инфицирования и достигают максимального значения на 15–20 сутки. С 10–14 дня начинается продукция специфических IgG, несколько позднее — IgA. IgM и IgA сохраняются в организме человека недолго (1–2 месяца), IgG — в течение всей жизни (серопозитивность).
Диагностическое значение при первичной ГИ имеет выявление IgM и/или четырехкратное увеличение титров специфических иммуноглобулинов G (IgG) в парных сыворотках крови, полученных от больной с интервалом 10–12 дней.
РГ обычно протекает на фоне высоких показателей IgG, свидетельствующих о постоянной антигенной стимуляции организма больного. Появление IgM у такой пациентки говорит об обострении болезни.
Для установления ВПГ-инфекции в диагностически сложных случаях необходимо комплексное вирусологическое обследование больных, включающее обнаружение антигена и анализ серологических показателей в динамике. Постановка диагноза ВПГ-инфекций только на основании серологического исследования может повлечь за собой диагностическую ошибку, так как низкие титры противогерпетических IgG не всегда доказывают отсутствие активной ГИ. Выявление же титров IgG выше средних является показанием к дополнительному обследованию пациентки с целью подтверждения или исключения диагноза ВПГ-инфекции.
Лечение генитального герпеса
Современная медицина не располагает методами лечения, позволяющими элиминировать ВПГ из организма человека. Поэтому методы лечения простого герпеса направлены на предотвращение или восстановление тех нарушений, которые вызывает активация ВПГ в организме.
В настоящее время существуют два основных направления в лечении простого герпеса:
а) использование этиопатогенетической противовирусной терапии, основное место в которой отводится ациклическим нуклеозидам — ацикловиру, валацикловиру, фамцикловиру;
б) комплексный метод лечения, включающий иммунотерапию (специфическую и неспецифическую) в сочетании с противовирусной терапией.
Ациклические нуклеозиды. Этиопатогенетическая терапия основывается на способности химиотерапевтических препаратов избирательно нарушать процесс взаимодействия ВПГ и клетки, включаться в цикл развития только ВПГ на стадиях синтеза вирусной ДНК и сборки вирусных частиц, тормозя их репродукцию, что приводит в конечном итоге к вирусостатическому эффекту. Химиотерапия занимает ведущее место при острой ГИ, протекающей с поражением ЦНС и других систем и органов, при герпесе новорожденных. Велико значение противовирусных средств при лечении рецидивирующих форм простого герпеса с поражением кожи, слизистых оболочек.
Схемы их назначения: ацикловир 0,2 г внутрь 5 раз в день 5 дней; валацикловир 0,5 г внутрь 2 раза в день 5 дней; фамцикловир 0,25 г внутрь 2 раза в день 5 дней.
Ацикловир нашел свое применение для лечения всех форм ГИ. Наличие нескольких лекарственных форм (мазь, таблетки, крем, суспензия, раствор для внутривенного введения) позволяют широко и эффективно использовать препарат в медицинской практике.
На основе ацикловира разработан более эффективный противогерпетический препарат валацикловир (L-валиновый эфир ацикловира). Именно это позволяет пациенту уменьшить число приемов препарата при рецидиве до двух раз в день (в отличие от ацикловира, который принимают 5 раз в день) и принимать валацикловир 1 раз в день при супрессивной терапии.
Иммунотерапия ГГ. Нарушение иммунного ответа — важнейшее звено в патогенезе простого герпеса. Как правило, заболевание протекает на фоне подавления иммунных реакций: отмечаются снижение общего количества Т- и В-клеток, изменение их функциональной активности, нарушения в макрофагальном звене иммунитета, в системе интерферона. Коррекция нарушений неспецифического и специфического звеньев иммунитета — одно из направлений в комплексной терапии простого герпеса.
Неспецифическая иммунотерапия включает в себя использование:
1) иммуноглобулина;
2) интерферонов и препаратов индукторов интерферона;
3) препаратов, стимулирующих Т- и В-звенья клеточного иммунитета и фагоцитоз.
Для лечения РГ применяют иммуноглобулин человеческий нормальный. Препарат содержит достаточное для достижения терапевтического эффекта количество специфических противогерпетических антител.
Первым препаратом, обладающим противовирусным действием, стал интерферон. Широкий спектр противовирусной активности, отсутствие резистентных к интерферону (ИФН) штаммов вирусов предопределили перспективу использования интерферона как средства этиопатогенетической терапии простого герпеса.
Свое развитие идея интерферонотерапии нашла в использовании индукторов эндогенного интерферона и создании генно-инженерных ИФН.
Способностью индуцировать ИФН обладает большая группа природных и синтетических соединений. Индуцируют выработку ИФН иммуномодулятор — левамизол, Дибазол, В12, Пирогенал, Продигиозан, являющиеся препаратами выбора при лечении герпеса.
Изучение ряда препаратов растительного происхождения, относящихся к классу полифенолов: Алпизарина, Флакозида, Хелепина-Д выявило их противовирусный эффект и интерферониндуцирующую активность.
Именно индукцией ИФН объясняется положительный терапевтический эффект, оказываемый описываемыми препаратами на многие вирусные заболевания (РГ, грипп, аденовирусная инфекция), что позволяет рекомендовать их как для монотерапии в неосложненных случаях РГ, так и в комплексном лечении ГИ, особенно у больных, страдающих частыми простудными заболеваниями и ОРВИ.
К середине 80-х годов в результате достижений генной инженерии была создана целая серия рекомбинантных интерферонов, представляющих собой различные субтипы альфа-2 интерферонов. Для лечения различных форм РГ используется отечественный рекомбинантный альфа-2 интерферон — Реаферон, который выпускается в инъекционной форме.
Для стимуляции Т- и В-звеньев клеточного иммунитета у больных РГ успешно применяются препараты «Тактивин», «Тималин», «Тимоген», «Миелопид».
Анализ многолетних наблюдений за больными, страдающими рецидивирующим ГГ, показывает, что наиболее выраженный терапевтический эффект достигается при комплексном подходе к терапии, который должен включать в себя несколько этапов:
1) противовирусная терапия в сочетании с иммунокоррекцией и интерферонотерапией, с учетом данных иммунологического обследования и изучения интерферонового статуса;
2) противорецидивное лечение противогерпетической вакциной в сочетании с иммуномодуляторами и симптоматическое использование противовирусных препаратов;
3) применение адаптогенов, повторные курсы вакцинотерапии (ревакцинация), симптоматическое использование противовирусных препаратов.
Вместе с тем даже при таком комплексном подходе встречаются случаи с низкой терапевтической эффективностью, проявляющиеся:
1) торпидностью к проводимой терапии, когда, несмотря на проводимое противовирусное и иммунокорригирующее лечение, включающее вакцинотерапию, частота и интенсивность рецидивов герпеса у больных остается прежней;
2) сохранением симптомов стойкого нарушения общего самочувствия (слабость, недомогание, психоастения) и снижения трудоспособности на фоне достигнутого в результате лечения выраженного улучшения в клиническом течении РГ (уменьшение частоты и длительности рецидивов).
Таким образом, тактика врача акушера-гинеколога и смежных специалистов, основанная на применении комплекса лечебно-профилактических мероприятий по диагностике и лечению ГИ, позволяет снизить частоту осложнений, улучшить репродуктивную функцию у женщин и обеспечить рождение здоровых детей.
Литература
В. Н. Кузьмин, доктор медицинских наук, профессор
МГМСУ, Москва



