Бишофитовые ванны в Волгограде
Ванна лекарственная с бишофитом
Бишофитовые ванны – это один из действенных и полезных методов физиотерапевтического лечения. Лекарственные ванны с бишофитом обладают огромной целебной силой и применяются не только с целью оздоровления, но и для профилактики заболеваний. В медицинском центре “Волжская Здравница” Вы можете заказать курс лечения бишофитными ваннами и получить не только эффект оздоровления но и удовольствие от лечения.
Как и любые физиопроцедуры ванны с бишофитом имеют свои показания и противопоказания. Перед тем, как принять решение о применении данного курса лечения необходимо провести консультацию с врачом физиотерапевтом, так как, бишофит имеет очень мощное воздействие на организм. Обратившись в медицинский центр “Волжская Здравница”, Вам всегда окажут необходимую помощь и проконсультируют по любым вопросам, касающиеся физиолечения.
Преимущества бишофитной ванны
Важно знать, что состав бишофита имеет очень высокую минерализацию и по своим целебным свойствам нисколько не уступает знаменитым солям Мертвого моря. Основным компонентом бишофита является магний, который играют важную роль в организме человека. Если наблюдается нехватка данного микроэлемента, то могут развиться серьезные нарушения в организме. Нехватка магния может спровоцировать возникновения нарушений в кровеносной системе, появлению частых головных болей, хронической усталости, появлению сердечных заболеваний.
Преимущества данной физиопроцедуры очевидны. Применяя бишофитные ванны можно снизить риск появления каких-либо заболеваний, улучшить собственное самочувствие, а также омолодить свой организм. Кроме того, бишофитные ванны будут очень полезны для тех, кто желает подтянуть свою фигуру и улучшить состояние кожи. Бишофит положительно влияет на состав крови, тормозит и устраняет любые воспалительные процессы в организме.
Польза бишофитовых ванн
Во время процедуры все полезные микроэлементы начинают проникать в организм через эпидермис и слизистые. Эффект оздоровления можно почувствовать уже через несколько сеансов.
Бишофит укрепляет иммунную защиту, а также способен эффективно уменьшить болевые ощущения в костях и мышцах. Кроме того, лекарственная ванна поможет снять возбудимость и заметно укрепить нервную систему, улучшить кровоснабжение мозга, сердца и других органов.
Лечение пяточной шпоры
Что же такое пяточные шпоры и откуда они берутся?
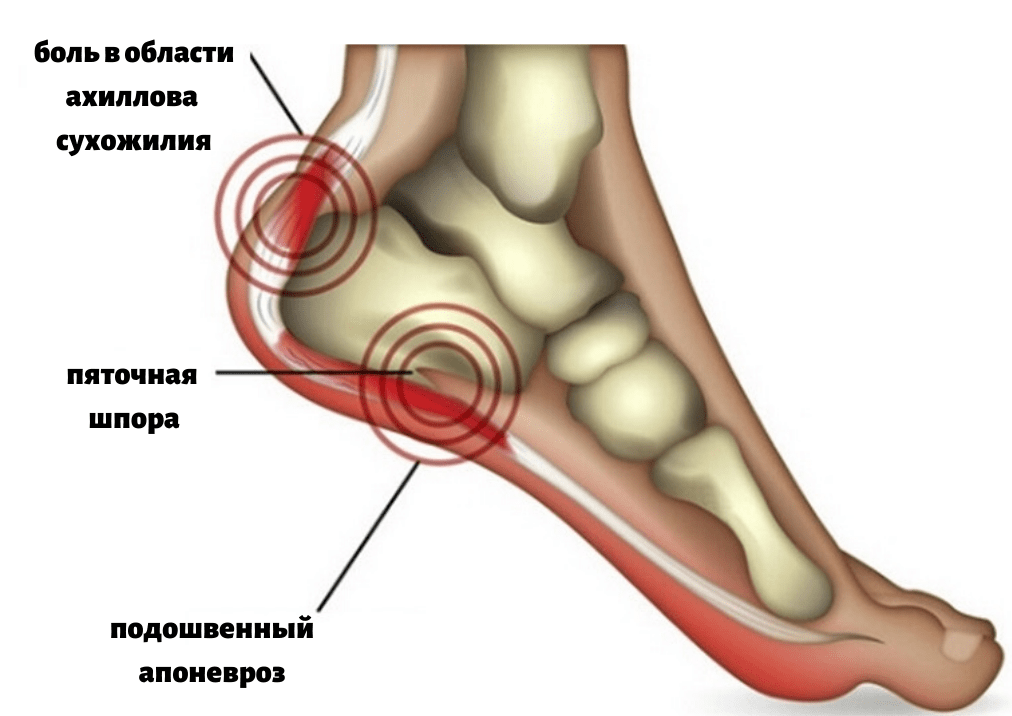
В результате различных процессов (избыточный вес, травма и др.) в данной области возникает хроническая травматизация сухожилия с образованием микронадрывов и постепенное развитие воспалительного процесса. Как компенсаторная реакция на травму и воспалительный процесс начинает образовываться костный вырост, он принимает форму шипа и, передавливая мягкие ткани подошвы стопы, вызывает характерные сильные боли в пяточной области. Самым значимым симптомом пяточной шпоры является сильная боль при ходьбе, особенно в самом начале ходьбы (так называемая, стартовая боль), при вставании со стула, с постели.
Основные причины образования пяточных шпор:
Проявления заболевания
Боли, возникающие при опоре на больную пятку, развиваются постепенно с ростом самой шпоры, характеризуются как жгучие или острые, с ощущением «гвоздя в пятке». Они могут локализоваться на внутренней поверхности больной пятки и переходить на всю стопу. При осмотре пяточной области нет никаких видимых изменений, редко отмечается отечность, болезненность определяется при надавливании на пятку. Интересно, что интенсивность боли не зависит от размера шпоры, что обусловлено, прежде всего, не наличием самой шпоры, а воспалительными изменениями в мягких тканях пятки. Диагноз пяточной шпоры подтверждается рентгенографией.
Основные принципы лечения пяточных шпор
1. Вначале необходимо выяснить причину развития воспалительного процесса в области подошвы и постараться максимально устранить ее. Т.е. выяснить, какой патологический процесс мог привести к избыточной травматизации фасции и возникновению воспаления. С этой же целью следует нормализовать вес, если он избыточный, дозировать физические нагрузки и ношение тяжестей, подобрать удобную, правильную обувь для занятий спортом и для повседневной носки. Снять и отложить в сторону неудобную обувь. На время экспресс-лечения следует ограничить нагрузку на ноги — сократить ходьбу и тем более бег или переноску тяжести насколько это возможно. Лучше носить удобные легкие кроссовки с хорошим супинатором.
2. Необходимо максимально возможное обеспечение физической разгрузки болезненной области, для чего рекомендуется подбор индивидуальных ортопедических стелек с выкладкой внутреннего и наружного продольного сводов, углублением и мягкой прокладкой под пяткой, а также временное ношение подпяточника с углублением или отверстием в центре. Как временную меру при лечении пяточной шпоры можно рекомендовать ношение обуви без задника;
3. Консервативное лечение направленно на ликвидацию воспалительного процесса и включает местное применение нестероидных противовоспалительных препаратов (гели и мази), обладающих противовоспалительным и рассасывающим эффектом. Но эти методы, как правило, приносят лишь только временный эффект, их обязательно нужно сочетать в комплексе с другими методами.
4. Наружное применение мазей при пяточной шпоре лучше сочетать с массажем стоп. Массаж при пяточной шпоре удобно делать самостоятельно.
5. В комплекс лечения пяточной шпоры включают теплые ванны с морской солью, содой. Ванночки необходимо делать перед применением мазей и массажа.
6. Определенные упражнения лечебной гимнастики с проведением массажа мышц стопы и голени — рекомендуются для улучшения кровоснабжения тканей стопы, с этой же целью можно проводить тепловые процедуры парафино- или озокеритотерапии.
7. В некоторых случаях (если развитие пяточной шпоры происходит на фоне артроза) в комплексной терапии рекомендуют прием хондропротекторов с анальгетическим и противовоспалительным эффектом, что останавливает прогрессивный воспалительный процесс, но эффект от внутреннего применения препаратов развивается только через 6 недель от начала лечения и сохраняется в течение 2–3 мес. после его отмены.
8. Методы медикаментозного лечения пяточной шпоры.
Официальная медицина на сегодняшний день разработала большое количество схем фармакологической терапии данного заболевания. Среди препаратов, применяемых для лечения пяточной шпоры: нестероидные противовоспалительные средства, гели, мази, кремы и пластыри для лечения пяточной шпоры местного применения, обладающие рассасывающим и противовоспалительным эффектом.
При малой эффективности консервативного лечения выполняются лекарственная блокада пяточной шпоры — обкалывание болезненного места шприцом с лекарственным веществом. Например, стойким эффектом обладает однократное местное введение дипроспана.
Препараты, применяемые с этой целью, оказывают выраженный местный противовоспалительный эффект, что быстро подавляет воспалительный процесс и снижает болевой синдром.
Данная процедура требует знаний и большого опыта, поэтому проводить ее может только квалифицированный специалист. Однако при частом использовании метода возможно разрушение связки или фасции.
9. К хирургическому лечению прибегают крайне редко, так как встречается много недостатков при данной методике. При проведении операции удаляют пяточную шпору. После чего конечность фиксируют гипсовой повязкой примерно на один месяц.
После снятия гипса назначают ортопедические стельки и проводят курсы восстановительного лечения. Помните, что в большинстве случаев пяточные шпоры вполне поддаются терапии и без операций.
10. Любой метод лечения необходимо сочетать с физиотерапевтическими воздействиями.
Ударно-волновая терапия пяточной шпоры
Является наиболее эффективным методом: терапия воздействует непосредственно на костные разрастания и способствует их уменьшению или даже рассасыванию. Ударно-волновая терапия — относительно новый метод лечения.
В нашей стране данная процедура начала практиковаться не очень давно, но первые результаты уже обнадеживают.
Имеющийся опыт позволяет утверждать, что при использовании данного метода лечения эффективность лечения пяточной шпоры очень высока. Метод основан на воздействии импульсов ударных волн определенной частоты. Эффект ударной волны разрыхляет отложения кальция в пяточной шпоре.
Это позволяет в дальнейшем вымывать разрыхленные отложения из организма с кровотоком. Пораженная связка избавляется таким образом от накопленных солей кальция.
Кроме того, при этом активизируются процессы регенерации тканей, уменьшаются отечность и воспалительные явления. С каждой проведенной процедурой болевой синдром становится все меньше и, как правило, значительно уменьшается или исчезает к концу лечения.
Пораженный участок во многом восстанавливает свою естественную структуру и возвращает себе способность переносить каждодневные нагрузки, не вызывая болезненных ощущений.
На начальных стадиях заболевания лечение требует небольшого количества процедур от 3 до 5 на курс, а при большой длительности процесса длительность лечения до 5-10 процедур на курс. Между сеансами обязателен перерыв 5-7 дней.
Продолжительность одного сеанса составляет 15-20 минут на одно поле. На кожу пятки наносят специальный гель, воздействие осуществляется с помощью излучателя.
Существуют противопоказаниями к лечению пяточной шпоры: нарушения свертываемости крови и тромбофлебит, злокачественные новообразования, беременность.
Нежелательно проведение процедур ударно-волновой терапии в течение месяца после введения в область пятки гормональных противовоспалительных препаратов.
Лучевая терапия (рентгенотерапия) пяточной шпоры
Использование рентгеновского излучения в лечении пяточной шпоры показывает весьма эффективные результаты. Метод заключается в том, что на область пятки направляются четко сфокусированные рентгеновские лучи, несущие пониженную дозу радиации.
Они вызывают блокирование нервных окончаний, и пациент перестает испытывать болевые ощущения.
Курс лечения чаще всего состоит из десяти сеансов, каждый из которых имеет продолжительность в 10 минут.
Рентгенотерапия в лечении пяточной шпоры обладает следующими преимуществами: полная безболезненность процедуры, высокая эффективность, минимум противопоказаний, воздействие излучения только на пяточную шпору, противоаллергическое и противовоспалительное действие, возможность амбулаторного лечения.
Противопоказанием к использованию данного метода является только беременность.
При применении рентгенотерапии сама шпора не исчезает, блокируются только болевые ощущения, исходящие от нее. Поэтому после проведения курса рентгенотерапии необходимо обязательной позаботиться о разгрузке стопы.
Лазерное лечение пяточной шпоры
В настоящее время низкоинтенсивная лазерная терапия — популярный и достаточно широко используемый метод лечения данного заболевания. Лазерная терапия воздействует на мягкие ткани, находящиеся вокруг шпоры.
Сфокусированное излучение вызывает увеличение кровообращения в области воспаления, что способствует уменьшению болей.
Среди пациентов бытует мнение о том, что лазерная терапия способна устранять саму пяточную шпору. Однако это является заблуждением. Проникая в ткани стопы, низкоинтенсивный лазерный луч на сам костный нарост не оказывает практически никакого действия.
Его эффект проявляется только на мягких тканях. А значит, после проведения курсов лазерной терапии также необходимо применять все методы, направленные на профилактику данного заболевания.
УВЧ-СВЧ-терапия
Этот метод заключается в применении переменного электромагнитного поля ультравысокой и сверхвысокой частоты. Влияние этих токов приводит к расширению капилляров в мягких тканях и к значительному усилению кровообращения. При этом уменьшается болевой синдром и воспаление.
Длительность одного сеанса составляет 10-15 минут. Для лечения пяточной шпоры требуется около 10-12 сеансов терапии.
Чаще врачи назначают пациентам переменное магнитное поле. Образуются слабые токи в крови и лимфе, которые влияют на метаболизм, а также на структуру воды и белков. Повышается сосудистая и кожная проницаемость, рассасываются отеки, уменьшается воспаление.
Данная методика позволяет достичь те же результаты, что и УВЧ-терапия.
Лечить шпоры на пятке можно и с помощью электрофореза или СМТ-ДДТ-фореза
Электрический ток повышает ионную активность в проводящих тканях, при этом увеличивается синтез многих биологически активных веществ. Лечебное действие обусловлено поступлением ионов лекарственных веществ (именно в ионной форме вещества наиболее активны), а также формированием кожного депо, из которого ионы постепенно поступают в ткани в последующие дни.
При электрофорезе используют специальные прокладки, пропитанные лекарством. Прокладки располагают между кожей пятки и пластинами электродов. Для лечения пяточной шпоры используют йодистый калий, гидрокортизон, новокаин и прочие препараты.
Эффективность таких методов физиолечения, как ультразвука и фонофореза (сочетанное применение ультразвука и лекарственного препарата) при пяточных шпорах составляет более 30%.
Основной эффект физиотерапии ультразвуком при лечении пяточной шпоры заключается в устранении воспалительного процесса, учитывая, что лучше всего ультразвук поглощается костной тканью.
При этом не следует бояться, что ультразвуковое лечение будет влиять на здоровую костную ткань пятки. Проведенные исследования низкочастотным ультразвуком показали, что разрушений костных тканей не вызывалось, но локальное применение ультразвуковых волн на область шпоры способствовало снижению содержания в ней кальция с замещением волокнистой соединительной тканью.
Также ультразвук оказывает рассасывающее и спазмолитическое действие, улучшая процессы локальной микроциркуляции.
Эффект от ультразвукового лечения усиливается сочетанным применением противовоспалительных мазевых препаратов. Озвучивание низкочастотным ультразвуком повышает проницаемость клеточных мембран, улучшает проницаемость и введение лекарственных веществ.
Наиболее часто применяют гидрокортизоновую мазь. Фонофорез способствует более глубокому проникновению лекарственного вещества в пораженную область, нежели применять мазь как самостоятельное средство лечения.
Метод фонофореза основан на свойстве ультразвука изменять проницаемость кожных покровов, в связи с чем лекарства, нанесенные на кожу, всасываются более активно.
Продолжительность самой процедуры — до 10 минут. На курс лечения может понадобится 5-10 процедур, с возможными повторными курсами.
Профилактика пяточной шпоры
Профилактические меры должны быть направлены, в первую очередь, на предупреждение преждевременного износа, старения и травм костно-суставного аппарата:
Санаторий «Северное Сияние»
Бишофитовые ванны
Польза процедуры обусловлена богатым составом бишофита и его натуральным происхождением. По своей сути данное вещество — это минерализованный соляной «коктейль», образованный твердыми частицами морской воды, которая испарялась на протяжении миллионов лет.
Наиболее выраженная терапевтическая польза обусловлена хлоридом магния — основной составляющей бишофита. Этот химический элемент играет важнейшую роль в регуляции работы нервной системы, является ценным электролитом и обеспечивает межклеточный обмен. Также это незаменимое вещество для здоровья сердца.
Именно со свойствами магния связаны показания к процедурам с использованием бишофита:
Отзывы врачей однозначны: процедуры с солью бишофита не принесут ощутимого облегчения в качестве самостоятельного средства, но при этом окажут заметную помощь, применяемые в комплексе с другими направлениями терапии.
Противопоказания
Противопоказания к процедурам с бишофитам ограничены, но их следует обязательно учитывать.
Главное, о чем следует помнить — эта процедура категорически противопоказана при любых острых состояниях. Это значит, что если симптомы болезни ярко выражены, повышена температура тела, обострилась боль в суставах или наблюдаются другие признаки того, что болезнь рецидивировала — бишофит может сильно навредить.
Также эта процедура противопоказана при следующих состояниях:
Во многих случаях наличие противопоказаний не делает бишофит запрещенным. Например, вместо общих водных процедур можно делать компрессы, ножные ванночки, растирания и пр.
Побочные эффекты:
В первые несколько процедур могут наблюдаться неприятные симптомы: головокружение, учащенное сердцебиение, чувство сильной слабости.
Такая реакция считается естественной и указывает на то, что действие бишофита началось. В большинстве случаев специального лечения не требуется, и такие проявления проходят через 2-3 процедуры.
Положительные качества:
Классификация патологий
Болезни опорно-двигательного аппарата
Ванны с бишофитом оказывают положительное влияние на опорно-двигательный аппарат. К примеру, процедуру можно использовать при артрите (исключением является туберкулёзная форма), артрозе, полиартрите. Она уменьшает спазм, поэтому допускается применение в случае радикулита, миозита, болезни Бехтерева. Дополнительное показание – патологии позвоночника (остеохондроз, сколиоз).
Патологии нервной системы
Ванна оказывает положительное влияние на ЦНС, а также успокаивающее действие.
Поэтому допускается назначение процедуры при следующих состояниях:
Гидротерапию (водные процедуры) бишофитом можно применять в детском возрасте. К примеру, при ДЦП (церебральный паралич).
Патологии сердца и сосудов
Бишофитовые ванны будут полезны для людей с гипертонической болезнью Iстадии.
А также процедуру назначают при:
Половые органы
Процедуру часто назначают гинекологи в следующих случаях:
Заболевания дыхательной системы
На протяжении процедуры действующие вещества могут проникать в организм не только через кожу, но и систему дыхания.
Поэтому ванны рекомендуется использовать при следующих заболеваниях:
Кожный покров
Гидротерапия бишофитом рекомендуется людям с поражением кожного покрова.
Процедуру назначают в следующих случаях:
Эндокринология
После использования процедуры происходит стабилизация гормонального фона, организм насыщается йодом.
Поэтому ванны можно применять в следующих случаях:
Псориаз и современные методы его лечения
Псориаз (чешуйчатый лишай) — хроническое, весьма распространенное заболевание кожи, известное с давних времен. Распространенность его в различных странах колеблется от 0,1 до 3%. Однако эти цифры отражают лишь удельный
Псориаз (чешуйчатый лишай) — хроническое, весьма распространенное заболевание кожи, известное с давних времен. Распространенность его в различных странах колеблется от 0,1 до 3%. Однако эти цифры отражают лишь удельный вес псориаза у больных с другими дерматозами или частоту его встречаемости у пациентов с внутренними болезнями. Поскольку болезнь часто носит локализованный и неактивный характер, больные обычно не обращаются за помощью в медицинские учреждения, а следовательно, нигде не регистрируются.
Причина болезни остается неясной. Несмотря на огромное количество предлагаемых гипотез, ни одна не является общепризнанной. Четко установлена лишь роль генетических факторов — семейный показатель больных в несколько раз превышает популяционный. Есть указания на связь псориаза с антигенами HLA-cистемы — В13, В15, В16, В17, В27, В39, Dw11, DRW6, DR7, A1. Имеются данные о возможной патогенетической значимости генетических маркеров Lewis, MN, Ss, Duffy, Hp.
Основным патогенетическим звеном, вызывающим появление кожных высыпаний, являются повышенная митотическая активность и ускоренная пролиферация клеток эпидермиса, приводящая к тому, что клетки нижних слоев «выталкивают» вышележащие клетки, не дав им ороговеть. Этот процесс носит название паракератоза и сопровождается обильным шелушением. Большое значение в развитии псориатических поражений в коже играют местные иммунопатологические процессы, связанные с взаимодействием различных цитокинов — фактора некроза опухоли, интерферонов, интерлейкинов, а также лимфоцитов различных субпопуляций.
Пусковым моментом возникновения болезни часто является сильный стресс — этот фактор присутствует в анамнезе большинства больных. К другим триггерным факторам можно отнести травмы кожи, применение медикаментов, злоупотребление алкоголем, инфекции.
Многочисленные нарушения в эпидермисе, дерме и во всех системах организма тесно связаны и не могут по отдельности объяснить механизм развития болезни.
Общепринятой классификации псориаза нет. Традиционно наряду с обычным (вульгарным) псориазом выделяют эритродермическую, артропатическую, пустулезную, экссудативную, каплевидную, ладонно-подошвенную формы.
Обычный псориаз клинически проявляется образованием плоских папул, четко отграниченных от здоровой кожи. Папулы розовато-красного цвета, покрыты рыхлыми серебристо-белыми чешуйками. С диагностической точки зрения интересна группа признаков, возникающих при поскабливании папул и называемых псориатической триадой. Сначала появляется феномен «стеаринового пятна», характеризующийся усилением шелушения при поскабливании, что придает поверхности папул сходство с каплей стеарина. После удаления чешуек наблюдается феномен «терминальной пленки», проявляющийся в виде влажной блестящей поверхности элементов. Вслед за этим при дальнейшем поскабливании отмечается феномен «кровяной росы» — в виде точечных, несливающихся капелек крови.
Высыпания могут располагаться на любом участке кожного покрова, но преимущественно локализуются на коже коленных и локтевых суставов и волосистой части головы, с поражения которой очень часто заболевание начинается. Для псориатических папул характерна склонность к периферическому росту и слиянию в бляшки различных размеров и очертаний. Бляшки могут быть изолированными, небольшими или крупными, занимающими обширные участки кожных покровов.
При экссудативном псориазе меняется характер шелушения — чешуйки становятся желтовато-сероватыми, склеиваются с образованием корочек, плотно прилегающих к коже. Сами высыпания более яркие и отечные, чем при обычном псориазе.
Псориаз ладоней и подошв может наблюдаться в виде изолированного поражения или сочетаться с поражениями других локализаций. Проявляется он в виде типичных папуло-бляшечных элементов, а также гиперкератотических, мозолеподобных очагов с болезненными трещинами или пустулезных высыпаний.
Практически всегда при псориазе поражаются ногтевые пластинки. Наиболее патогномоничным считается появление на ногтевых пластинках точечных вдавлений, придающих ногтевой пластинке сходство с наперстком. Также могут отмечаться разрыхление ногтей, ломкость краев, изменение окраски, поперечные и продольные борозды, деформации, утолщение, подногтевой гиперкератоз.
Псориатическая эритродермия является одной из наиболее тяжелых форм псориаза. Она может развиваться за счет постепенного прогрессирования псориатического процесса и слияния бляшек, но чаще возникает под влиянием нерационального лечения. При эритродермии вся кожа приобретает ярко-красный цвет, становится отечной, инфильтрированной, отмечается обильное шелушение. Больных беспокоит сильный зуд, ухудшается общее состояние.
Рентгенологически различные изменения костно-суставного аппарата наблюдаются у большинства больных без клинических признаков поражения суставов. К таким изменениям относят околосуставной остеопороз, сужение суставных щелей, остеофиты, кистозные просветления костной ткани. Диапазон клинических проявлений может варьировать от незначительных артралгий до развития инвалидизирующего анкилозирующего артроза. Клинически обнаруживаются припухлость суставов, покраснение кожи в зоне пораженных суставов, болезненность, ограничение подвижности, деформации суставов, анкилозы, мутиляции.
Пустулезный псориаз проявляется в виде генерализованных или ограниченных высыпаний, локализованных преимущественно на коже ладоней и подошв. Хотя ведущим симптомом этой формы псориаза считается возникновение на коже пустул, считающихся в дерматологии проявлением гнойничковой инфекции, содержимое этих пузырьков обычно стерильно.
Каплевидный псориаз чаще развивается у детей и сопровождается внезапным высыпанием рассеянных по всему кожному покрову мелких папулезных элементов.
Псориаз наблюдается примерно с одинаковой частотой у мужчин и женщин. У большинства пациентов заболевание начинает развиваться до 30 лет. У многих больных отмечается связь обострений с временем года: чаще заболевание обостряется в холодный период (зимняя форма), гораздо реже — летом (летняя форма). В дальнейшем эта зависимость может меняться.
В течении псориаза различают 3 стадии: прогрессирующую, стационарную и регрессирующую. Для прогрессирующей стадии характерны рост по периферии и появление новых высыпаний, особенно на местах прежних высыпаний (изоморфная реакция Кебнера). В регрессирующей стадии наблюдается уменьшение либо исчезновение инфильтрации по окружности или в центре бляшек.
Вульгарный псориаз дифференцируют от парапсориаза, вторичного сифилиса, красного плоского лишая, дискоидной красной волчанки, себорейной экземы. Сложности возникают при дифференциальной диагностике ладонно-подошвенного и артропатического псориаза.
При вульгарном псориазе прогноз для жизни благоприятный. При эритродермии, артропатическом и генерализованном пустулезном псориазе возможны инвалидизация и даже летальный исход из-за истощения и развития тяжелых инфекций.
Неопределенным прогноз остается в отношении продолжительности заболевания, длительности ремиссии и обострений. Высыпания могут существовать длительно, многие годы, но чаще обострения чередуются с периодами улучшения и клинического выздоровления. У значительной части больных, в особенности не подвергавшихся интенсивному системному лечению, возможны многолетние, самопроизвольные периоды клинического выздоровления.
Нерациональное лечение, самолечение, обращение к «целителям» ухудшают течение болезни, приводят к обострению и распространению кожных высыпаний. Именно поэтому основная цель данной статьи — дать краткую характеристику современным методам лечения этой болезни.
Сегодня существует огромное количество методов лечения псориаза, в терапии этого заболевания используются тысячи различных препаратов. Ноэто лишь означает, что ни один из методов не дает гарантированного эффекта и не позволяет вылечить болезнь окончательно. Более того, вопрос об излечении и не ставится — современная терапия в состоянии лишь свести к минимуму кожные проявления, не затрагивая многих неизвестных на сегодня патогенетических факторов.
Лечение псориаза проводится с учетом формы, стадии, степени распространенности высыпаний, общего состояния организма. Как правило, лечение комплексное, предусматривающее сочетание наружных и системных препаратов.
Большое значение при лечении имеют мотивация пациента, семейные обстоятельства, социальное положение, образ жизни, злоупотребление алкоголем.
Способы лечения можно разделить на следующие направления: наружная терапия, системная терапия, физиотерапия, климатотерапия, нетрадиционные и народные методы.
Наружная терапия
Терапия препаратами наружного действия имеет при псориазе важнейшее значение. В легких случаях лечение начинают с местных мероприятий и ими ограничиваются. Как правило, препараты для местного применения реже оказывают какие-либо побочные действия, но по эффективности уступают системной терапии.
В прогрессирующей стадии наружное лечение проводят с большой осторожностью, чтобы не вызвать ухудшения состояния кожи. Чем интенсивнее воспаление, тем меньшей должна быть концентрация мазей. Обычно на этой стадии при лечении псориаза ограничиваются кремом «Унна», 0,5–2% салициловой мазью, травяными ваннами.
На стационарной и регрессирующей стадии показаны более активные препараты — 5–10% нафталановая мазь, 2–10% мазь АСД, 2–5% салициловая мазь, 2–5% серно-дегтярная мазь, а также многие другие способы терапии.
В современных условиях при выборе способа терапии или конкретного препарата должен руководствоваться официальными протоколами и формулярами, разработанными руководящими органами здравоохранения. В Федеральном руководстве по использованию лекарственных средств (выпуск IV) для местного лечения больных псориазом предлагаются стероидные лекарственные средства, салициловая мазь, препараты дегтя и кальципотриол.
Исходя из «Методических материалов по диагностике и лечению наиболее распространенных инфекций, передаваемых половым путем, и заболеваний кожи», разработанных ЦНИКВИ в 2001 г., в качестве наружной терапии используют 1–2% салициловую мазь, мази с содержанием дегтя 5–10%, нафталана 5–10%, витамина Д3, а также кортикостероидные мази (бетаметазон с салициловой кислотой, мометазон) и аэрозоль цинка пиритионата. В «Протоколах ведения больных», разработанных учеными ЦНИКВИ в 2003 г., рекомендуются те же препараты.
Остановимся в основном на указанных в руководствах препаратах.
Гидратитрующие средства. Смягчают шелушащуюся поверхность псориатических элементов, уменьшают стягивание кожи, улучшают эластичность. Используют кремы на основе ланолина с витаминами, крем «Унна». По данным литературы, даже после такого легкого воздействия клинические эффекты (снижение зуда, эритемы и шелушения) достигаются у трети больных.
Препараты салициловой кислоты. Обычно используют мази с концентрацией от 0,5 до 5% салициловой кислоты. Она обладает антисептическим, противовоспалительным, кератопластическим и кератолитическим действием, может применяться в комбинации с дегтем и кортикостероидами. Салициловая мазь размягчает шелушащиеся слои псориатических элементов, а также усиливает действие местных стероидов путем усиления их всасывания, поэтому часто используется в комбинации с ними. Сама салициловая кислота легко проникает в кожу и затем в кровь. Поэтому ее не применяют на обширных поверхностях и в концентрации больше 2%, а у детей даже 2-процентную мазь накладывают только на ограниченных участках кожи. Непереносимость встречается редко, однако салициловая кислота может вызывать в качестве побочного эффекта усиление воспаления кожи.
Дегтярные препараты. Применяются издавна в виде 5–15% мазей и паст, часто в сочетании с другими местными препаратами. В России используются мази с древесным дегтем (обычно березовым), в некоторых зарубежных странах — с каменноугольным. Последний более активен, но, как считают наши ученые, обладает канцерогенными свойствами, хотя многочисленные публикации и зарубежный опыт не подтверждают этого. Деготь превосходит салициловую кислоту по активности, обладает противовоспалительными, кератопластическими и антиэксфолиативными свойствами. Его применение при псориазе обусловлено, кроме того, влиянием на клеточную пролиферацию. Применение дегтярных препаратов ограничено из-за неприятного запаха, их нельзя накладывать на лицо. Комбинации дегтя с цинком или салициловой кислотой не обладают значительными преимуществами перед монокомпонентными препаратами дегтя. Способность дегтя повышать фоточувствительность используется для комбинированной терапии в сочетании с ультрафиолетовым облучением. Не следует применять препараты дегтя длительно и в повышенной концентрации, так как это может привести к всасыванию и системному действию (поражение почек, общая интоксикация, паралич). При назначении препаратов дегтя следует учитывать его фотосенсибилизирующее действие и риск ухудшения функции почек у лиц с нефрологическими болезнями.
Для мытья головы используют шампуни с дегтем (фридерм-тар, Т/гель).
Нефть нафталанская. Смесь углеводородов и смол, содержит серу, фенол, магний и много других веществ. Препараты нафталанской нефти обладают противовоспалительными, рассасывающими, противозудными, антисептическими, отшелушивающими и репарационными свойствами. Для лечения псориаза применяются 10–30% нафталановые мази и пасты. Часто нафталанская нефть используется в комбинации с серой, ихтиолом, борной кислотой, цинковой пастой.
Местная терапия ретиноидами. Первый эффективный местно применяемый ретиноид, разрешенный к употреблению как средство для лечения псориаза, — тазаротен. В России этот препарат пока не зарегистрирован. Он представляет собой желе на водной основе и выпускается в концентрации 0,05 и 0,1%. По эффективности он сравним с сильнодействующими ГКС. Из побочных эффектов отмечаются зуд и раздражение кожи. Одним из преимуществ этого препарата является более продолжительная по сравнению с ГКС ремиссия. Так, по данным J. Koo, через 3 мес после лечения рецидив наблюдали только у 185 больных (после флуоцинонида — у 55%). В работе A. Marchetti показаны фармакоэкономические преимущества тазаротена в виде 0,1% геля в сравнении с мазью флуоцинонида (местный ГКС) и кальципотриена (разновидность витамина Д3 для местного использования).
Гидрантроны. В первой половине XX в. применялись мази со смесью естественных дериватов антрацена — хризаробином, который получали из стволов бразильского дерева Vonacopua araroba семейства бобовых.
В настоящее время в Европе и США используются синтетические гидроксиантроны — дитранол, антралин, цигнолин, антраробин.
Дитранол — аналог естественного хризаробина, оказывает цитотоксическое и цитостатическое действие, приводит к снижению активности окислительных и гликолитических процессов в эпидермисе. В результате уменьшаются количество митозов в эпидермисе, а также гиперкератоз и паракератоз. К сожалению, дитранол обладает выраженным местно-раздражающим действием, и при попадании на здоровую кожу могут возникать ожоги. С другой стороны, дитранол очень эффективен и не вызывает системных побочных эффектов. Несколько лет назад в Европе появились препараты, которые высвобождают дитранол только при температуре кожи человека (миканол). В результате ослабляется окрашивание кожи. Сегодня дитранол применяют в достаточно высоких концентрациях (>1%), нанося его на 5–30 минут. Этот способ не уступает по эффективности применению препарата в низких концентрациях на ночь. По данным литературы, средняя ремиссия при лечении дитранолом составляет 4 – 6 мес.
Российские специалисты редко используют препараты этой группы, в России они не производятся и за рубежом не закупаются. Ранее предлагались несколько препаратов этой группы — цигнодерм, дитрастик, псоракс. Они выпускаются в виде стержня, наподобие губной помады. Добавление парафина позволяет наносить препараты точно на область поражения, что особенно удобно при лечении ограниченных, застарелых очагов.
К препаратам этой группы можно отнести антралин, который применяется в европейских и американских лечебных центрах. Препарат тормозит синтез ДНК ядра и митохондрий, угнетает метаболизм в тканях, что приводит к снижению пролиферации. При использовании сильно окрашивает контактируемые поверхности, может вызывать раздражения и ожоги.
Производные иприта.
К ним относятся псориазин и антипсориатикум. В их состав входят вещества кожно-нарывного действия — иприт и трихлорэтиламин. Лечение этими препаратами проводят с большой осторожностью, применяя сначала мази с небольшой концентрацией на небольшие очаги поражения 1 раз в день. Затем при хорошей переносимости концентрацию, площадь и кратность при использовании увеличивают. Лечение осуществляют под тщательным врачебным контролем, проводя еженедельные тесты крови и мочи. Сейчас данные препараты практически не применяются, однако они весьма эффективны в стационарной стадии болезни.
Цинка пиритионат. Активное вещество, выпускаемое в виде аэрозолей, кремов и шампуней под торговым названием «Скин-кап». Обладает противомикробным, противогрибковым, а также антипролиферативным действием — подавляет патологический рост клеток эпидермиса, находящихся в состоянии гиперпролиферации. Последнее свойство определяет эффективность препарата при псориазе. Препарат снимает воспаление, уменьшает инфильтрацию и шелушение псориатических элементов. Лечение проводят в среднем в течение месяца. Для терапии больных с поражениями волосистой части головы используют аэрозоль и шампунь, при поражениях кожи — аэрозоль и крем. Препарат наносят 2 раза в сутки, шампунь применяют 3 раза в неделю. В России начиная с 1995 г. проводилось изучение клинической эффективности и переносимости всех лекарственных форм цинка пиритионата. По заключению ведущих дерматологических центров — ЦНИКВИ, РГМУ, ММА, ВМА — эффективность препарата при лечении больных псориазом достигает 85–90%. Исходя из данных, опубликованных в периодической печати ведущими специалистами этих и других центров, клинического излечения удается добиться к концу 3–4 нед лечения. Эффект развивается постепенно, но очень важно, что результаты лечения очевидны уже к концу первой недели с момента начала применения препарата — резко снижается зуд, устраняется шелушение, бледнеет эритема. Такое быстрое достижение клинического эффекта приводит, соответственно, к быстрому улучшению качества жизни пациентов. Препарат хорошо переносится. Разрешен для применения с 3- летнего возраста.
Мази с витамином Д3. С 1987 г. при местном лечении используется синтетический препарат витамина Д3 — кальципотриол. Многочисленными экспериментальными исследованиями показано, что кальципотриол вызывает торможение пролиферации кератиноцитов, ускоряет их морфологическую дифференциацию, воздействует на факторы иммунной системы кожи, регулирующие пролиферацию клеток, обладает противовоспалительными свойствами. На российском рынке представлены 3 препарата данной группы от различных производителей. Препараты наносят на пораженные участки кожи 1-2 раза в сутки. Эффективность мазей с Д3 примерно соответствует эффекту кортикостероидных мазей I, II классов, а по данным J. Koo — даже III класса. При применении этих мазей выраженный клинический эффект наступает у большинства больных (до 95%). Однако для достижения хорошего эффекта может понадобиться достаточно много времени (от 1 мес до 1 г.), а площадь поражения не должна превышать 40%. И. В. Хамаганова сообщает о положительном опыте применения кальципотриола у детей. Препарат наносили 2 раза в день, выраженный эффект наблюдался к концу четвертой недели лечения. Побочных эффектов не выявлено. О таких же результатах лечения при использовании кальципотриола у взрослых сообщает В. А. Самсонов.
Иногда при использовании кальципотриола могут наблюдаться раздражение кожи, дерматит, фотосенсибилизация, обострение псориатического процесса, гиперкальциемия. Однако кальципотриол не вызывает побочных эффектов, характерных для стероидов, и иногда дает более стойкий эффект, чем мази с ГКС. Хотя, по данным того же J. Koo, рецидивы возникают у более 50% больных, при этом средняя продолжительность ремиссии не превышает 1,5 мес.
Более выраженных эффектов достигают при сочетанном применении кальципотриола с любыми формами фототерапии, а также с системной терапией.
Кортикостероидные препараты. Применяются в медицинской практике в качестве наружных средств с 1952 г., когда Sulzberger впервые показал эффективность наружного применения стероидов. На сегодняшний день на российском фармацевтическом рынке зарегистрированы около 50 глюкокортикостероидных средств для наружного применения. Это, несомненно, затрудняет выбор врача, который должен иметь информацию обо всех препаратах. Специальное анкетирование, проведенное Н. Г. Кочергиным среди дерматологов, показало, что при выборе средств для наружной терапии врачи исходят из следующих данных: активности кожного процесса, локализации высыпаний, возраста больного, эффективности рекламы и стоимости препарата в аптеке. К наиболее часто назначаемым при псориазе ГКС, по данным того же опроса, относятся комбинированные препараты (флуметазона пивалат с салициловой кислотой), мометазона фуроат или бетаметазона дипропионат.
Терапевтический эффект наружных ГКС обусловлен целым рядом потенциально благоприятных эффектов:
Изменение структуры ГКС отражалось на их свойствах, активности. Так появилась достаточно обширная группа препаратов, различающихся по своему химическому строению и активности. Гидрокортизона ацетат сегодня при псориазе практически не применяется, его используют в клинических исследованиях для сравнения со вновь получаемыми препаратами. Например, считается, что если активность гидрокортизона принять за единицу, то активность триамцинолона ацетонида составит 21 единицу, а бетаметазона — 24 единицы. Из препаратов второго класса при псориазе чаще используется флуметазона пивалат в комбинации с салициловой кислотой, а наиболее современными являются нефторированные ГКС. В связи с минимальным риском возникновения побочных явлений мази и кремы с аклометазоном разрешены для применения на чувствительных участках (лицо, кожные складки), лечения детей и пожилых людей, при нанесении на обширные участки кожи.
Среди препаратов третьего класса можно выделить группу фторированных ГКС — флуоцинолона ацетонид, триамцинолона ацетонид, бетаметазона валерат и дипропионат. Фармакоэкономический анализ применения этих препаратов (правда, не при псориазе), заключающийся в изучении соотношения «цена/безопасность/эффективность», по данным В. А. Аковбяна, выявил благоприятные показатели у бетаметазона валерата — быстрое развитие терапевтического эффекта, более низкая стоимость курса лечения.
При лечении псориаза начинать следует с более легких препаратов — гидрокортизона, преднизолона, аклометазона, а при повторных обострениях и неэффективности используемых препаратов давать более сильные. Однако среди американских дерматологов популярна следующая тактика: вначале применяется сильный ГКС для достижения быстрого эффекта, а потом пациента переводят на умеренный или слабый препарат для проведения поддерживающей терапии. В любом случае сильные препараты используют короткими курсами и лишь на ограниченные участки, так как при их назначении чаще развиваются побочные эффекты.
Помимо указанной классификации, препараты подразделяют на фторированные, дифторированные и нефторированные средства разных поколений. Нефторированные ГКС первого поколения (гидрокортизона ацетат) по сравнению с фторированными, как правило, менее эффективны, но более безопасны в отношении побочных реакций. Сейчас проблема низкой эффективности нефторированных ГКС уже решена — созданы нефторированные препараты четвертого поколения, сравнимые по силе с фторированными, а по безопасности — с гидрокортизона ацетатом. Это, в частности, гидрокортизона бутират, мометазона фуроат, метилпреднизолона ацепонат. Проблема усиления действия препарата решается не путем галогенизации, а благодаря этерификации. Кроме усиления действия это позволяет использовать этерифицированные препараты 1 раз в сутки. К примеру, гидрокортизона бутират имеет следующие фармакодинамические свойства: торможение миграции лейкоцитов и лимфоцитов в область воспаления, угнетение протеолитической активности тканевых кининов, задержка роста фибробластов, предупреждение развития соединительной ткани в очаге воспаления. Именно нефторированные ГКС четвертого поколения являются сегодня предпочтительными для местного применения при псориазе.
Стандартные побочные эффекты при применении местных стероидов — это развитие атрофии кожи, гипертрихоза, телеангиэктазий, гнойничковых инфекций, системное действие с влиянием на гипоталамо-гипофизарно-надпочечниковую систему. В современных нефторированных препаратах, упомянутых выше, эти побочные эффекты сведены к минимуму.
Фармацевтические компании стараются разнообразить спектр лекарственных форм и выпускают ГКС в виде мазей, кремов, лосьонов. Жирная мазь, создавая пленку на поверхности очага поражения, вызывает более эффективное рассасывание инфильтрации, чем другие лекарственные формы. Крем лучше купирует островоспалительные явления, увлажняет, охлаждает кожу. Безжировая основа лосьона обеспечивает его легкое распределение по поверхности волосистой части головы без склеивания волос.
По литературным данным, при использовании, например, мометазона в течение 3 нед положительного терапевтического эффекта (уменьшения количества высыпаний на 60–80%) удается добиться почти у 80% больных. По данным В. Ю. Уджуху, наиболее выгодного соотношения «эффективность/безопасность» можно достичь при использовании гидрокортизона бутирата. Выраженный клинический эффект при применении этого препарата сочетается с хорошей переносимостью — ни у одного из прошедших курс лечения больных авторы не наблюдали побочных реакций, даже при нанесении на лицо. При длительном использовании других ГКС приходилось останавливать лечение из-за развития побочных эффектов. По данным B. Bianchi и Н. Г. Кочергина, сравнение результатов клинического применения мометазона фуората и метилпреднизолона ацепоната показало одинаковую эффективность этих лекарственных средств при наружном применении. Ряд авторов (Е. Р. Аравийская, Е. В. Соколовский) предлагают этапную кортикостероидную терапию псориаза. Рекомендуется начинать наружную терапию с комбинированных препаратов, содержащих ГКС (например, бетаметазон и салициловую кислоту). Средняя продолжительность такого лечения — около 3 нед. В дальнейшем происходит переход на чистый ГКС, желательно третьего класса (например, гидрокортизона бутират или мометазона фуроат).
Больных привлекают простота использования стероидных препаратов, возможность достаточно быстро снять клиническую симптоматику заболевания, доступность, отсутствие запаха. Кроме того, эти лекарственные средства не оставляют жирных пятен на одежде. Однако их применение должно быть кратковременным, во избежание ухудшения течения болезни. При длительном применении стероидных мазей развивается привыкание. Резкая отмена кортикостероидов может вызвать обострение кожного процесса. В литературе указывается разная длительность ремиссии после местного лечения кортикостероидами. Большинство работ свидетельствует о непродолжительной ремиссии — от 1 до 6 мес. Исследования R. Seville установили, что ГКС в комбинации с другими методами (в частности, с дитранолом) повышают эффективность лечения, но уменьшают длительность ремиссии. Пациентам нужно рекомендовать как можно дольше обходиться без применения кортикостероидных мазей. Во многих зарубежных источниках мази, содержащие глюкокортикостероидные гормоны, рекомендуют предпочтительно использовать на ограниченных открытых участках поверхности кожи — лицо, руки. Однако следует помнить об опасности развития на лице стероидного периорального дерматита или розацеа, особенно при применении фторированных ГКС.
При псориазе наиболее эффективны комбинации стероидных гормонов (чаще всего бетаметазона) с салициловой кислотой. Салициловая кислота благодаря своему кератолитическому и противомикробному действию дополняет дерматотропную активность стероидов.
На волосистую часть головы удобно наносить комбинированные лосьоны с кортикостероидами и салициловой кислотой. По данным отечественных авторов (Г. И. Суколин, В. А. Молочков, Н. С. Потекаев), эффективность комбинированных препаратов достигает 80 — 100%, при этом очищение кожи происходит очень быстро —в течение 3 нед.
Подводя итоги, следует сказать, что на практике врачу всегда необходимо решать, использовать ли только наружные методы лечения или назначать их в сочетании с какой-либо системной терапией в целях повышения эффективности лечения и удлинения ремиссии.
Ю. Н. Перламутров, доктор медицинских наук, профессор
А. М. Соловьев, кандидат медицинских наук
МГМСУ, Москва