чем полечить печень после длительного употребления алкоголя
Можно ли восстановить печень после нескольких лет употребления алкоголя, и если – да, то как?
Злоупотребление алкоголем может не только очень сильно ухудшить здоровье – стать причиной алкогольного гепатита и цирроза, но и привести к летальному исходу. Лишний вес, неправильное питание, наследственность и другие факторы в несколько раз увеличивают вероятность появления и скорость развития патологий.
Но болезни печени не являются приговором. О том, как восстановить печень после алкоголя, читайте ниже. В частности:
Самое важное в лечении печени
Есть несколько способов, как помочь печени после алкоголя:
К чему может привести пристрастие к спиртным напиткам?
Серьезный вред печени и здоровью в общем наносится при двух типах поведения:
В итоге можно столкнуться с таким заболеванием, как алкогольная болезнь печени. Для того чтобы не допустить этого, достаточно иметь чувство меры в употреблении алкоголя.
Алкогольная болезнь печени проявляется по-разному:
Несмотря на то, что цирроз может стать причиной летального исхода, есть те, кто смог вылечиться. И главным был полный отказ от алкоголя.
Не откладывайте помощь! Звоните!
«Отягчающие обстоятельства»
Согласно исследованиям, не у всех людей, которые злоупотребляют алкоголем, появляется алкогольная болезнь печени. Высокая вероятность жирной печени, алкогольного гепатита и цирроза у тех, кто:
Если вас можно отнести к одной (или нескольким) группам, то обязательно откажитесь от алкоголя. Иначе можете тяжело заболеть и даже умереть.
Безопасная норма алкоголя в день для мужчин и женщин
Безопасной нормой алкоголя в день для мужчин является 28 гр чистого спирта, т.е.:
В свою очередь, безопасная норма алкоголя в день для женщин составляет в 2 раза меньше, всего лишь 14 гр чистого спирта. Столько содержится в:
Такой объем алкоголя не навредит ни печени, ни здоровью. Но только в том случае, если вы здоровью. При любом заболевании печени следует полностью отказаться от алкоголя.
Как обнаружить алкогольную болезнь печени?
Чтобы обнаружить алкогольную болезнь печени, необходимо:
Протекание алкогольной болезни печени
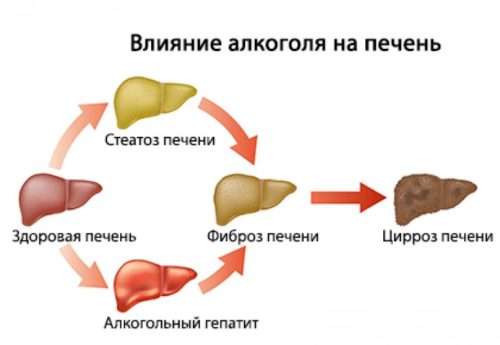
Как уже говорилось ранее, протекание алкогольной болезни печени может быть различным. Кто-то проходит все стадии: жирную печень, алкогольный гепатит, цирроз, а кто-то сразу сталкивается с циррозом. Это зависит от очень большого количества факторов (веса, питания, наследственности, пола, раса и этноса, объема спиртных напитков и др.).
Проконсультируйтесь со специалистом, сколько можно пить именно вам.
Осложнения алкогольной болезни печени
К осложнениям алкогольной болезни печени относится:
Нельзя не отметить и то, что заболевания печени могут привести к сбоям в работе и других органов, особенно, желудочно-кишечного тракта (ЖКТ).
Что делать, если вам поставили диагноз алкогольная болезнь печени?
Если в кабинете врача вы услышали диагноз жирная печень, то для того, чтобы поправить здоровье, достаточно отказаться от алкоголя и следовать схеме лечения – правильно питаться и принимать препараты. После того, как вылечитесь, вы сможете продолжить пить, но немного и нечасто.
Что касается тех, у кого обнаружен алкогольный гепатит или цирроз, то им лучше всего навсегда забыть об алкоголе.
Согласно статистике, у около 10% людей, которые после выявления заболеваний печени не отказываются от алкоголя, появляются и развиваются недуги, угрожающие жизни.
Если же вы найдете в себе силы для того, чтобы на 100% отказаться от алкоголя, правильно питаться и принимать препараты, то сможете устранить чуть ли не все последствия разгульного образа жизни.
По поводу вопроса о том, сколько восстанавливается печень после алкоголя, можно сказать только одно: все зависит от того, как часто и сколько вы пили. Минимум – полгода. Если же Вас интересует комплексное лечение алкоголизма, то смело обращайтесь к нам за помощью.
Чем полечить печень после длительного употребления алкоголя
Хотя стеатоз печени обнаруживается у 90% злоупотребляющих лиц, стеатогепатит развивается у относительно небольшой их части, а цирроз формируется лишь у 10–20%. Стеатоз протекает, как правило, бессимптомно и полностью регрессирует в условиях абстиненции. Естественное течение алкогольной болезни печени (АБП) определяется в первую очередь паттерном употребления спиртных напитков. Нередко в качестве непосредственной причины смерти выступает не декомпенсация цирроза и не гепатоцеллюлярная карцинома, а алкогольный гепатит, «наслоившийся» на хроническую патологию печени и ведущий к острой печеночной недостаточности на фоне хронической ( liver failure). Тяжелый алкогольный гепатит характеризуется высокой летальностью, достигающей 30–50% в течение трех месяцев. У выживших больных наблюдается ускоренное формирование фиброза с нередким формированием цирроза в течение 1–2 лет. Возможности терапии АБП ограничены. При гепатите тяжелого течения, наряду с коррекцией трофологического статуса, назначаются преднизолон и пентоксифиллин. Для лечения хронических форм АБП в настоящее время применяются средства для лечения алкогольной зависимости. Эффективность препаратов метаболического (гепатопротективного) действия ставится под сомнение, хотя в отдельных исследованиях получены обнадеживающие результаты.
Хотя стеатоз печени обнаруживается у 90% злоупотребляющих лиц, стеатогепатит развивается у относительно небольшой их части, а цирроз формируется лишь у 10–20%. Стеатоз протекает, как правило, бессимптомно и полностью регрессирует в условиях абстиненции. Естественное течение алкогольной болезни печени (АБП) определяется в первую очередь паттерном употребления спиртных напитков. Нередко в качестве непосредственной причины смерти выступает не декомпенсация цирроза и не гепатоцеллюлярная карцинома, а алкогольный гепатит, «наслоившийся» на хроническую патологию печени и ведущий к острой печеночной недостаточности на фоне хронической ( liver failure). Тяжелый алкогольный гепатит характеризуется высокой летальностью, достигающей 30–50% в течение трех месяцев. У выживших больных наблюдается ускоренное формирование фиброза с нередким формированием цирроза в течение 1–2 лет. Возможности терапии АБП ограничены. При гепатите тяжелого течения, наряду с коррекцией трофологического статуса, назначаются преднизолон и пентоксифиллин. Для лечения хронических форм АБП в настоящее время применяются средства для лечения алкогольной зависимости. Эффективность препаратов метаболического (гепатопротективного) действия ставится под сомнение, хотя в отдельных исследованиях получены обнадеживающие результаты.
Последствия злоупотребления алкоголем представляют собой общемировую проблему, включающую не только органную патологию, но также несчастные случаи и преступления, связанные с состоянием опьянения. Так, в Европе 11% летальных исходов у мужчин и 1,8% у женщин рассматриваются в ассоциации с алкоголизмом [1]. Если анализировать структуру поражений внутренних органов, то доминирующую позицию среди них занимает именно алкогольная болезнь печени (АБП), ведущая к развитию цирроза печени и гепатоцеллюлярной карциномы [2]. Несмотря на то, что в последние годы на пути изучения патогенеза поражения печени достигнуты серьезные успехи, лечение тяжелых форм АБП в определенной мере «законсервировалось», не давая основания говорить о революционном прорыве в ближайшем будущем. Тем не менее, определенные направления в терапии АБП можно расценивать как перспективные, причем это относится не только к методам, которые не вышли пока за рамки экспериментальных, но и к давно известным средствам, открывающим новые грани в процессе углубленного изучения.
Естественное течение АБП: от стеатоза к циррозу
Хотя стеатоз печени обнаруживается у 90% злоупотребляющих лиц, стеатогепатит развивается у относительно небольшой их части, а цирроз формируется лишь у 10–20% [3, 4]. Стеатоз протекает, как правило, бессимптомно и полностью регрессирует в условиях абстиненции. Естественное течение АБП определяется в первую очередь паттерном употребления спиртных напитков: постоянным или перемежающимся типом пьянства; периодами запоев, сменяющихся абстиненцией; нарастанием или сокращением суточной дозы алкоголя Учитывая обстоятельство, что большинство пациентов обращаются за медицинской помощью на поздних стадиях, оптимальной моделью наблюдения служат больные после трансплантации печени [5].
Генетическая предрасположенность к АБП также служит предметом активного изучения. Недавние исследования выявили значимую корреляцию определенных аллельных вариантов адипонутрина (PNPLA3) и прогрессированием фиброгенеза [6, 7]. Более того, генетический полиморфизм адипонутрина ассоциирован и с развитием ГЦК [8]. В то же время попытки идентифицировать генетические маркеры предрасположенности к АБП, в том числе полиморфизм генов, участвующих в метаболизме этанола, пока не увенчались успехом [9].
В ретроспективном исследовании S. Naveau, включавшем более 2000 злоупотребляющих алкоголем пациентов, по данным биопсии печени у 34% выявлен цирроз, у 9% — активный гепатит, у 46% — стеатоз печени с наличием или отсутствием фиброза, а у 11% патологические изменения печени отсутствовали [10]. По данным T. Poynard, вероятность развития цирроза нарастает с возрастом, достигая при регулярном употреблении высоких доз алкоголя 50% к 61 году, причем у женщин сроки формирования цирроза короче [11]. Суммируя опубликованные результаты ретроспективных исследований, можно констатировать, что среди госпитализированных алкоголиков частота обнаружения цирроза составляет около 20% [2].
Стеатоз обычно предшествует образованию соединительной ткани, но влияние аккумуляции жира в печени на фиброгенез изучено недостаточно [2, 13, 14]. Долгосрочная выживаемость пациентов с алкогольным стеатозом в отсутствии воспаления и фиброза сопоставима с таковой у трезвенников. Если сравнивать течение неалкогольной жировой болезни печени (НАЖБП) и АБП, можно констатировать более высокие темпы прогрессирования последней. В течение 10 лет у больных алкогольным стеатозом значительно чаще развивается цирроз (21% vs. 1%) и наблюдаются летальные исходы (74% vs. 25%) [15]. Интересно, что у больных алкогольным циррозом повышен риск аутоиммунных заболеваний [16]. Можно предположить, что ацетальдегид, образующийся в разных тканях под действием алкогольдегидрогеназы, образует прочные комплексы с белками, выступающие в роли неоантигенов.
Цирроз печени рассматривается в качестве причины смерти 25% алкоголиков, занимая первое место среди летальных исходов [1, 2, 15]. Нередко в качестве непосредственной причины смерти выступает не декомпенсация цирроза и не гепатоцеллюлярная карцинома, а алкогольный гепатит, «наслоившийся» на хроническую патологию печени и ведущий к острой печеночной недостаточности на фоне хронической ( liver failure). Это состояние проявляется желтухой, в тяжелых случаях энцефалопатией и гипокоагуляцией, и требует обязательного отражения в диагнозе, так как принципиально меняет прогноз и подходы к лечению.
Недавно завершенные исследования, основанные на биопсийном материале, убедительно продемонстрировали, что у подавляющего большинства пациентов с тяжелым алкогольным гепатитом имеется исходный цирроз или септальный фиброз печени [9, 18]. Тяжелый алкогольный гепатит характеризуется высокой летальностью, достигающей 30–50% в течение трех месяцев. У выживших больных наблюдается ускоренное формирование фиброза с нередким формированием цирроза в течение 1–2 лет [2].
В то время как ожирение является общепризнанным коморбидным фактором стеатоза, имеются также сведения о его влиянии на развитие алкогольного гепатита и фиброза печени. В качестве ключевых патогенетических факторов называются инсулинорезистентность и гипергликемия [19]. С другой стороны, небольшие дозы этанола способствуют замедлению прогрессирования неалкогольной жировой болезни печени [20].
Лечение АБП: акцент на абстиненцию
К вопросу о безопасной дозе алкоголя
Необходимость обсуждения лимита употребляемого алкоголя, превышение которого ведет к повреждению печени, в аспекте лечения АБП определяется тем, что соблюдение пациентом полной абстиненции является важной, но зачастую недостижимой целью. Так, в США 67–81% больных возобновляют прием алкоголя в течение одного года [21]. В последние годы дозу этанола часто измеряют в «дозах» (drinks), равных 10–14 г чистого этанола. «Доза» примерно соответствует бокалу пива, фужеру сухого вина или рюмке крепкого напитка. Показано, что прием ≤ 2 «доз» в день для мужчин и ≤ 1 «дозы» в день для женщин не ассоциировано с повышенной вероятностью развития органной патологии по сравнению с трезвенниками [2]. Другие исследования демонстрируют сходные результаты. Согласно метаанализу G. Corrao, употребление > 25 г этанола в день увеличивает относительный риск цирроза печени [22]. В итальянском исследовании Dionysos у лиц, ежедневно принимающих ≥ 30 г этанола, цирроз наблюдался в 2,2% случаев, тогда как у непьющих — в 0,08%. Риск цирроза экспоненциально возрастал по мере увеличения доз алкоголя, достигая 13,5% у употребляющих > 120 г в день [23].
Средства для лечения алкогольной зависимости
Ввиду того, что большинство пациентов нарушают предписанный режим абстиненции, в последние годы активно изучаются препараты, снижающие потребность в алкоголе: налтрексон, акампрозат, топирамат, баклофен и др. Наибольшее число исследований на сегодняшний день выполнено с агонистом баклофеном, продемонстрировавшим эффективность и безопасность при тяжелых формах АБП [24].
Метадоксин, зарегистрированный в ряде европейских стран для лечения алкогольной интоксикации, в нескольких небольших исследованиях значимое снижение употребления алкоголя, что сопровождалось редукцией биомаркеров АБП (трансаминазы, γ-глутамилтранспептидаза, средний объем эритроцитов) [25]. Сходные результаты получены в исследовании внутривенной формы глицирризиновой кислоты. Интересно, что соблюдение предписанного режима абстиненции коррелировало со снижением сывороточного уровня фактора некроза опухоли-α [26].
Коррекция трофологического статуса
Нутритивная поддержка наиболее важна для больных тяжелым алкогольным гепатитом, хотя и при других формах АБП у большинства пациентов наблюдаются те или иные формы нарушения трофологического статуса [2]. В исследовании С. Mendenhall et al. показано, что у пациентов, самостоятельно принимающих пищу с энергетической ценностью более 3000 ккал в сутки, отмечалась нулевая летальность, в то время как из потреблявших менее 1000 ккал в сутки умерло более 80% [27]. Несмотря на безусловную ценность этих данных, нельзя игнорировать высокую вероятность более тяжелого течения гепатита у больных второй группы, к типичным проявлениям которого относится анорексия [28].
Общие рекомендации по коррекции трофологического статуса у больных тяжелым алкогольным гепатитом предусматривают суточное потребление 1500–2500 ккал. Диета должна быть сбалансирована по содержанию основных нутриентов и витаминов, ограничение белка показано лишь в случаях его индивидуальной непереносимости. Следует помнить о преимуществе перорального приема пищи над зондовым и парентеральным; последнее назначается только при невозможности физиологического питания (повторная рвота, нарушения сознания).
Как отмечалось выше, избыточная масса тела и ожирение тоже способствуют прогрессированию повреждения печени ввиду общности ряда патогенетических звеньев алкогольного и неалкогольного стеатогепатита [10, 29], что необходимо учитывать при разработке программы лечения.
Кортикостероиды применяются для лечения тяжелого алкогольного гепатита на протяжении более 40 лет. Наиболее хорошо изучена схема с пероральным преднизолоном 40 мг в сутки в течение одного месяца, с одномоментной отменой или постепенным снижением дозы. Хотя многочисленные исследования весьма разнородны по дизайну и отбору пациентов, метаанализ показал достоверное повышение краткосрочной выживаемости по сравнению с больными, не получавшими преднизолон [14]. Оценка эффективности терапии обычно осуществляется с помощью индекса Лилле (Lille), который рассчитывается через семь дней лечения по формуле:
R = 3,19 — 0,101 (возраст в годах) + 0,147 (альбумин в день поступления, ) + 0,0165 (сывороточный билирубин, мкмоль) + 0,206 (наличие почечной недостаточности — 0 или 1) + 0,0065 (сывороточный билирубин в день поступления, мкмоль) + 0,0096 (протромбиновое время, с)
Индекс Лилле = Exp ® /[1 +Exp ® ]
Значение индекса Лилле > 0,45 указывает на неэффективность преднизолона и 75%-ю вероятность летального исхода в течение шести месяцев. С почти пятикратным ростом летальности сопряжено также отсутствие снижения уровня сывороточного билирубина, по меньшей мере, на 25% за аналогичный срок стероидной терапии [30]. У этой когорты больных дальнейшее применение преднизолона нецелесообразно, с учетом повышения риска инфекционных осложнений, особенно легочного аспергиллеза [31]. В упомянутом метаанализе выделены три группы пациентов в зависимости от реакции на преднизолон: с полным, частичным и нулевым ответом. Краткосрочная выживаемость в этих группах составила 91%, 79% и 53%, соответственно [14].
В первом сообщении о применении пентоксифиллина при тяжелом алкогольном гепатите были представлены обнадеживающие результаты, свидетельствующие о существенном снижении риска гепаторенального синдрома (ГРС) [32]. Большое рандомизированное контролированное исследование STOPAH, включавшее более 1000 пациентов, не продемонстрировало преимущество пентоксифиллина перед плацебо в отношении краткосрочной выживаемости [33]. Хотя необходимо принимать во внимание, что из исследования были исключены наиболее тяжелые больные — с ГРС, сепсисом и манифестной энцефалопатией — целесообразность применения пентоксифиллина представляется сомнительной.
Комбинация преднизолона и пентоксифиллина не выявила преимуществ по сравнению с монотерапией преднизолоном [13]. Таким образом, на сегодняшний день улучшение прогноза больных тяжелым алкогольным гепатитом, резистентных к кортикостероидам, возможно только путем выполнения срочной трансплантации печени [14].
Метаболические препараты («гепатопротекторы»)
Международные гепатологические ассоциации не рекомендуют применение лекарственных средств данной группы при АБП, что обусловлено слабой доказательной базой.
В исследовании J. Mato пероральное применение в дозе 1200 мг в сутки на протяжении двух лет сопровождалось более низкой летальностью или потребностью в трансплантации печени по сравнению с группой плацебо у больных компенсированным и субкомпенсированным алкогольным циррозом (класс, А и В по ) — 12% и 29% (p = 0.04), соответственно. Количество пациентов, прекративших и продолживших употребление алкоголя, было сопоставимо в обеих группах [35].
Результаты недавно опубликованного исследования и соавторов указывают на более низкую частоту ГРС у больных, получавших комбинацию преднизолон + по сравнению с монотерапией преднизолоном (p = 0.035). Показатели летальности в группах при этом статистически значимо не различались [28].
и соавторы представили результаты парентерального применения глицирризиновой кислоты у пациентов с алкогольным стеатогепатитом. Помимо отмеченного выше позитивного влияния на алкогольную зависимость, констатировано значимое снижение активности трансаминаз и уровня сывороточного билирубина [26].
L- ускоряет метаболизм аммиака, уменьшая проявления печеночной энцефалопатии. Показано, что препарат обладает способностью улучшать биохимические параметры у пациентов с хронической патологией печени, в том числе АБП [36]. Не исключено, что этот эффект обусловлен дезинтоксикацией обладающего универсальным цитотоксическим действием аммиака.
Неудовлетворительные результаты лечения тяжелых форм АБП служат основанием для разработки новых подходов, базирующихся на ключевых патогенетических механизмах. К находящимся на разных стадиях изучения, относятся модулирование иннатного иммунного ответа, подавление кишечной бактериальной и эндотоксиновой транслокации, блокирование апоптоза и активация фарнезоидного Х рецептора. В качестве многообещающего направления рассматривается технология индукции плюрипотентных стволовых клеток [37].
История медицины свидетельствует о том, что именно элиминация этиологического фактора определяет успех лечения большинства болезней, в том числе в эпидемиологическом ракурсе. Так, широкое внедрение в клиническую практику антигеликобактерной терапии позволило значимо снизить распространенность язвенной болезни желудка и двенадцатиперстной кишки, а противовирусных препаратов — эффективно контролировать заболеваемость гепатитом С. Казалось бы, в отношении АБП и других заболеваний решение проблемы лежит на поверхности: абстиненция ведет к выздоровлению или, по крайней мере, резкому снижению риска фатальных последствий. Однако этот постулат вызывает, по крайней мере, два вопроса: 1) что делать с больными, которые хотят, но не могут отказаться от алкоголя вследствие зависимости; 2) какой тактики ведения следует придерживаться в случае прогрессирования патологических изменений, несмотря на абстиненцию. Следовательно, весьма актуальным остается вопрос о медикаментозном лечении АБП, особенно тяжелых ее форм — гепатита и цирроза. Достижения в этой области не столь грандиозны, как в других разделах гепатологии. Многие лекарственные средства, на которые ранее возлагались надежды, основанные на результатах экспериментальных и пилотных данных, не оправдали их в рандомизированных контролированных исследованиях; показательным примером могут служить эссенциальные фосфолипиды. Тем важнее выбрать из относительно небольшого терапевтического арсенала препараты, проверенные временем и зарекомендовавшие себя с позиций доказательной медицины.
European Association for the Study of Liver. EASL clinical practical guidelines: management of alcoholic liver disease. J. Hepatol. 2012; 57: 399–420.
Mathurin P., Bataller R. Trends in the management and burden of alcoholic liver disease. J. Hepatol. 2015; 62(1S): S..
Lefkowitch of alcoholic liver disease. Clin. Liver Dis. 2005; 9: 37–53.
Lucey M., Mathurin P., Morgan hepatitis. N. Engl. J. Med. 2009; 360: 2758–2769.
DiMartini A., Dew M.A., Day N. et al. Trajectories of alcohol consumption following liver transplantation. Am. J. Transplant. 2010; 10: 2305–2312.
Stickel F., Buch S., Lau K. et al. Genetic variation in the PNPLA3 gene is associated with alcoholic liver injury in Caucasians. Hepatology. 2010; 53: 86–95.
Trépo E., Gustot T., Degré D. et al. Common polymorphism in the PNPLA3/adiponutrin gene confers higher risk of cirrhosis and liver damage in alcoholic liver disease. J. Hepatol. 2011; 55: 906–912.
Liu Y.L., Patman G.L., Leathart J.B. et al. Carriage of the PNPLA3 rs738409 C >G polymorphism confers an increased risk of fatty liver disease associated hepatocellular carcinoma. J. Hepatol. 2014; 61: 75–81.
Bataller R., North K. Brenner polymorphisms and the progression of liver fibrosis: a critical appraisal. Hepatology. 2003; 37: 493–503.
Naveau S., Giraud Borotto E. et al. Excess weight risk factor for alcoholic liver disease // Hepatology. 1997; 25: 108–111.
Poynard T., Mathurin P., Lai C.L. et al. A comparison of fibrosis progression in chronic liver diseases. J. Hepatol. 2003; 38: 257–265.
Song M., Chen T., Prough alcohol consumption causes liver injury in male mice through enhanced hepatic inflammatory response. Alcohol. Clin. Exp. Res. 2016; 40(3): 518–528.
Mathurin P., Louvet A., Duhamel A. et al. Prednisolone with vs. without pentoxifylline and survival of patients with severe alcoholic hepatitis: a randomized clinical trial. JAMA. 2013; 310: 1033–1041.
Mathurin P., Moreno C., Samuel D. et al. Early liver transplantation for severe alcoholic hepatitis // N. Engl. J. Med. 2011; 365: 1790–1800.
S., Franzmann M., Andersen I.B. et al. Longterm prognosis of fatty liver: risk of chronic liver disease and death. Gut. 2004; 53: 750–755.
Raynard B., Balian A., Fallik D. et al. Risk factors of fibrosis in liver disease. Hepatology. 2002; 35: 635–638.
Dunn W., Sanyal A.J., Brunt E.M. et al. Modest alcohol consumption is associated with decreased prevalence of steatohepatitis in patients with fatty liver disease (NAFLD) J. Hepatol. 2012; 57: 384–391.
Miller W.R, Walters S.T., Bennett effective is alcoholism treatment in the United States? J. Stud. Alcohol. 2001; 62: 211–220.
Corrao G., Bagnardi Zambon A., Torchio P. of alcohol intake in relation to risk of liver cirrhosis. Alcohol Alcohol. 1998; 33: 381–392.
Bellentani S., Saccoccio G., Costa G. et al. Drinking habits as cofactors of risk for alcohol induced liver damage. The Dionysos Study Group. Gut. 1997; 41: 845–850.
Vuittonet C.L., Halse M., Leggio L et al. Pharmacotherapy for alcoholic patients with alcoholic liver disease. Am. J. Health Syst. Pharm. 2014; 71(15): 1265–1276.
Leggio L., Kenna G.A., Ferrulli A. et al. Preliminary findings on the use of metadoxine for the treatment of alcohol dependence and alcoholic liver disease. Hum. Psychopharmacol. 2011; 26: 554–559.
Никитин И.Г, Байкова И.Е., Волынкина В.М. и др. Опыт использования глицирризиновой кислоты в лечении пациентов с алкогольной болезнью печени. Росс. журн. гастроэнтерол. гепатол. колопроктол. 2009; 19(1): 53–58.
Mendenhall C., Roselle G.A., Gartside P., Moritz T. Relationship of protein calorie malnutrition to alcoholic liver disease: A reexamination of data from two Veterans Administration Cooperative Studies. Alcoholism: Clinical and Experimental Research. 1995; 19(3): 635–641.
Tkachenko P, Maevskaya M, Pavlov A et al. Prednisolone plus S- in severe alcoholic hepatitis. Hepatol Int. 2016 Jun 23.
Diehl and alcoholic liver disease. Alcohol. 2004; 34: 81–87.
Louvet A., Naveau S., Abdelnour M. et al. The Lille model: a new tool for therapeutic strategy in patients with severe alcoholic hepatitis treated with steroids. Hepatology. 2007; 45: 1348–1354.
Gustot T., Maillart E., Bocci M. et al. Invasive aspergillosis in patients with severe alcoholic hepatitis. J. Hepatol. 2014; 60: 267–274.
Thursz M., Richardson P., Allison M.E. et al. Steroids or pentoxifylline for alcoholic hepatitis: results of the STOPAH trial. Hepatology. 2014; 60: LB1.
E., Thevenot T., Piquet M.A. al. Glucocorticoids plus in severe alcoholic hepatitis. N. Engl. J. Med. 2011; 365: 1781–1789.
Грюнграйф К., Й. Эффективность гранул L- при лечении хронических заболеваний печени. Сучасна гастроентерология. 2008; 2: 59–66.
Saberi B, Dadabhai AS, Jang YY Current Management of Alcoholic Hepatitis and Future Therapies. J Clin Transl Hepatol. 2016; 4(2): 113–122.
Рисунок. Схема стадийного течения алкогольной болезни печени (по P. Mathurin, R. Bataller, 2015, с изменениями).