Паркинсонизм
Паркинсонизм или синдром Паркинсона – это патологическое состояние, которое проявляется скованностью в движениях, непроизвольным дрожанием конечностей и головы, постоянным мышечным гипертонусом. Как правило, паркинсонизм связывают с различными органическими патологиями головного мозга.
Не стоит путать синдром Паркинсона и болезнь Паркинсона – болезнь считается самостоятельным заболеванием со схожими симптомами. А паркинсонизм – это синдром, который может развиваться вторично (например, после воздействия токсинов, черепно-мозговых травм).
Симптомы паркинсонизма
У паркинсонизма есть ряд характерных симптомов, которые позволяют четко дифференцировать это заболевание:
Даже характерные симптомы не гарантируют достоверную диагностику. Поэтому необходимо пройти полноценное обследование.
Формы
Выделяют два основных типа паркинсонизма:
Выделяют несколько форм вторичного заболевания, которые классифицируют исходя из предпосылок заболевания.
Причины
Основная причина заболевания – это отмирание нейронов в области головного мозга, которая отвечает за координированное действие мышц и мышечный тонус. Также неврологи отметили недостаток дофамина в этой области мозга, который вызывает такие симптомы, как тремор и мышечная скованность. А вот факторов риска или предпосылок довольно много. Они не обязательно напрямую приводят к развитию заболевания, но значительно повышают его вероятность.
Выявить точную причину может только врач-невролог после полноценного обследования.
Наши врачи
Диагностика
Сначала собирает анамнез. Пациенту задают такие вопросы:
Затем проводит стандартный для подобных жалоб неврологический осмотр: оценивает походку, мышечный тонус, характер тремора и т.д.
Следующий этап – фармакологический тест. Он заключается в назначении пациенту препарата на основе дофамина или аналогичных веществ. Если есть паркинсонизм, то это способствует снижению симптоматики.
Нередко требуется консультация психолога для оценки когнитивной и эмоциональной сферы. Обычно для этого используют стандартные тесты и опросники.
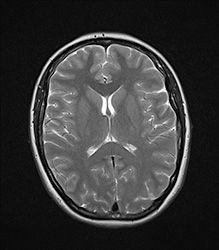
Подтвердить диагноз можно на МРТ – обследование покажет патологические участки в области, отвечающей за мышечный тонус и координацию. Эти высветленные участки показывают отмершие нейроны. МРТ позволяет также подтвердить или исключить опухоль.
Диагностика заканчивается постановкой диагноза, в соответствии с которым назначают лечение.
Лечение паркинсонизма
Лечение сходно и для синдрома Паркинсона, и для болезни Паркинсона. Главное отличие заключается в том, что при синдроме требуется установить причину и начать лечение основного заболевания.
Рекомендуются следующие методы лечения:
Эффективность медикаментозного лечения оценивают по снижению симптоматики. Если консервативная терапия оказалась неэффективной, то назначают хирургическое вмешательство.
Оперативное лечение: к нему прибегают при неэффективности медикаментозного. Операция называется стереотаксической деструкцией ядер таламуса и заключается в разрушении области мозга, отвечающей за чувствительность. Процедура позволяет снизить симптоматику и вернуть способность к нормальному движению.
В клинике ЦЭЛТ работают квалифицированные неврологи, которые предлагают терапию синдрома Паркинсона. Современные методы диагностики позволяют врачам точно установить причину болезни, а многолетний опыт – назначить максимально эффективное лечение.
Болезнь Паркинсона и астроциты: новый взгляд на лечение нейродегенеративных заболеваний
Болезнь Паркинсона и астроциты: новый взгляд на лечение нейродегенеративных заболеваний
Ученые из Калифорнийского университета в Сан-Диего показали успешную трансформацию астроцитов в нейроны in situ для лечения болезни Паркинсона. Поможет ли эта работа приблизиться к созданию успешной терапии?
Автор
Редакторы
Статья на конкурс «Био/Мол/Текст»: Болезнь Паркинсона до сих пор остается неизлечимой. Однако в июне 2020 года в журнале Nature вышла статья, способная произвести революцию в терапии этого недуга. В этой работе мы рассмотрим, какие предыдущие исследования привели к такому результату и как это может повлиять на будущее всей нейробиологии.
Конкурс «Био/Мол/Текст»-2020/2021
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2020/2021.
Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.

Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.
Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Дисклеймер
Обычно «Биомолекула» не публикует статьи по одинаковым инфоповодам, но в этом году мы приняли две работы, базирующиеся на одной и той же публикации в Nature 2020 года. Статья, которую вы читаете, — обзорная, а вот и ее парная новостная [16].
Болезнь Паркинсона является вторым по распространенности нейродегенеративным расстройством. Она характеризуется отмиранием нейронов в черной субстанции мозга. Существующая терапия направлена на ограниченное сдерживание заболевания. Эффективного лекарства до сих пор не существует. Недавнее исследование может в корне изменить плачевную ситуацию. Хао Цянь из Калифорнийского университета в Сан-Диего (США) вместе с коллегами из Пекинского университета (Китай) продемонстрировал успешное превращение астроцитов в нейроны in situ на мышиной модели болезни Паркинсона. Однако начнем с общей характеристики этого заболевания.
Болезнь Паркинсона: история и молекулярный патогенез
В 1817 году английский Джеймс Паркинсон [1] опубликовал работу «Эссе о дрожательном параличе», в которой дал описание неврологического недуга, а также провел анализ и выявил общие закономерности. В названии отражено необычное сочетание основных симптомов — тремор, скованность мышц и неспособность удерживать равновесие [2].
Кстати, одним из ученых, который помог разгадать тайны патогенеза болезни Паркинсона, стал русский невропатолог Константин Николаевич Третьяков, занимавший в 1916–1923 годах должность заведующего лабораторией мозга имени Шарко кафедры нервных болезней Парижского университета (Франция). Он предложил нигральную теорию патогенеза болезни Паркинсона, согласно которой, проявления заболевания были связаны с утратой черной субстанции головного мозга.
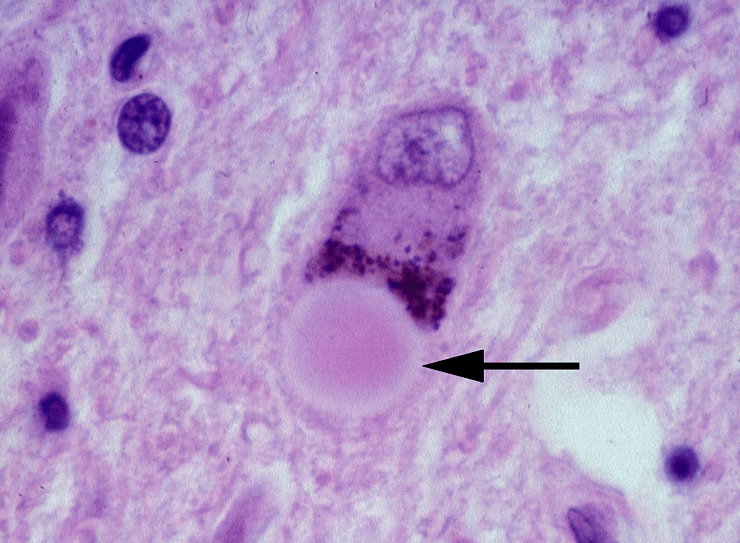
Сегодня известно, что болезнь Паркинсона развивается вследствие дегенерации дофаминергических нейронов в черной субстанции, что приводит к снижению уровня вырабатываемого дофамина — нейромедиатора, ответственного за чувство удовлетворения и привязанности. Клинические проявления связаны с нейротоксическим эффектом: по мере прогрессирования заболевания в клетках накапливается белок альфа-синуклеин [3]. Альфа-синуклеин в норме задействован в механизме транспорта и высвобождения везикул с нейротрансмиттерами. Однако у пациентов с болезнью Паркинсона наблюдается фосфорилирование и аномальное свертывание этого белка с образованием агрегатов — телец Леви (рис. 1). В 2018 году группа ученых из научно-исследовательского института Скриппса (США) обнаружила, что фосфорилированная форма альфа-синуклеина локализуется в митохондриях, вызывая их фрагментацию [4].
Рисунок 1. Тельце Леви в нейроне черной субстанции головного мозга
Возможности сегодняшней терапии
Сейчас существует только симптоматическое лечение, направленное на облегчение имеющихся проявлений заболевания. Одним из наиболее эффективных и широко применяемых лекарств является леводопа, или 3-гидрокси-L-тирозин [5]. Леводопа — биологический предшественник дофамина. Помимо леводопы, иногда используется ряд других лекарственных средств. Агонисты дофаминовых рецепторов имеют химическую структуру, похожую на дофамин, и за счет этого могут стимулировать его рецепторы [6]. Ингибиторы моноаминоксидазы B способны блокировать высвободившийся дофамин и продлевать время его действия. Ингибиторы катехол-О-метилтрансферазы подавляют распад принятой леводопы и удлиняют время ее действия в организме.
Также для терапии болезни Паркинсона применяют так называемые нейротрофические факторы — регуляторные белки, которые поддерживают жизнеспособность и функционирование нейронов. Хотя было проведено множество исследований по использованию нейротрофических факторов в клинической практике, у них есть ряд недостатков. Во-первых, они нуждаются в точной доставке к месту назначения. Для этого используют специальные катетеры. Во-вторых, нейротрофические факторы целесообразно использовать только в том случае, если у пациента еще не повреждены аксоны дофаминергических нейронов. Если же транспортная система в черной субстанции нарушена или уничтожена, то такое лечение не даст никаких положительных эффектов [7].
Часть из вышеперечисленных способов борьбы с болезнью широко используется, однако ничего из этого не поможет вернуть человеку его утраченные нейроны. Поэтому были попытки разработать терапию, направленную на восстановление популяции дофаминергических нейронов. В 2018 году группа ученых из японского Университета Киото [8] пересадила в