Влияние сибутрамина (Меридиа) на метаболические параметры больных с ожирением.
| В настоящее время ожирение является одним из самых распространенных заболеваний в экономически развитых странах. Согласно расчетам экспертов ВОЗ предполагается, что в 2005 году число больных, страдающих ожирением, в мире может составить 300 миллионов человек. |
Значимость проблемы ожирения прежде всего определяется высоким риском развития сердечно-сосудистых заболеваний, сахарного диабета 2 типа, а также нарушений репродуктивной функции [6, 21, 23, 24]. Многие ученые выявили взаимосвязь между возникновением выше перечисленных заболеваний и характером распределения жировой ткани [3, 22, 28]. Имеются данные о том, что именно висцеральная жировая ткань, обладающая гормонально-метаболической активностью, провоцирует развитие инсулинорезистентности (ИР) и гиперинсулинемии (ГИ), что является ключевым звеном в формировании метаболического синдрома (МС). Абдоминальное ожирение, представляющее собой один из основных компонентов МС, способствует возникновению нарушений липидного спектра крови, наиболее часто проявляющихся дислипидемией (ДЛП), характеризующейся повышенным содержанием свободных жирных кислот, триглицери дов и снижением уровня липопротеидов высокой плотности [5, 6, 20]. Сочетание подобных факторов приводит к раннему развитию атеросклероза, ИБС, артериальной гипертензии и снижению общей продолжительности жизни [2, 13].
Поскольку избыточный вес негативно воздействует на здоровье населения, то лечение ожирения является крайне важной проблемой здравоохранения. Внимание клиницистов сконцентри ровано на лечении ожирения и его негативных последствий, которое выражается в коррекции метаболических и сердечно-сосудистых нарушений, восстановлении репродуктивной функции, а также устранении физических и психологиче ских проблем, связанных с избыточным весом. Продолжают совершенствоваться методы фармакотерапии ожирения. Сибутрамин представляет собой новое средство в арсенале препаратов для лечения ожирения. Исходно сибутрамин был синтезирован как антидепрессант, в последующем была выявлена его способность выраженно снижать массу тела пациентов. Это свойство препарата опосредовано двойным механизмом действия. Так, сибутрамин (Меридиа) селективно подавляет обратный захват серотонина и норадреналина в синапсах центральной нервной системы, что снижает аппетит и увеличивает расход энергии [16, 27]. Согласно результатам проведенных исследований препарат способствует доза-зависимому снижению массы тела пациентов и поддержанию сниженного веса [16, 18, 26]. Однако данные о влиянии сибутрамина на показатели липидного и углеводного обмена крайне малочисленны [8, 16, 26]. Практически не изучено влияние препарата на характер секреции инсулина и возможность коррекции гиперинсули немии, которая является ведущим звеном в патогенезе метаболического синдрома, сопряженного с нарушением функции яичников.
В связи с этим целью исследования явилось изучение влияния терапии сибутрамином (Меридиа) на метаболические параметры больных с ожирением и нарушением репродуктивной функции.
Нарушение функции яичников у 25 (83,3%) больных характеризовалось олигоменореей, у 5 (16,7%) больных менструальный цикл был регулярным, однако у одной имела место недостаточность лютеиновой фазы (НЛФ) и у 4 — ановуляция. У 25 (83,3%) отмечалось первичное или вторичное бесплодие. Клинические признаки андрогенизации имелись у 22 (73,3%) больных, среднее значение гирсутного числа по шкале Ферримана — Голлвея было равно 15,8±1,31. У 23 больных были выявлены эхографические признаки СПКЯ. Наличие яичниковой гиперандрогении подтверждало повышение уровня тестостерона. У больных, включенных в исследование, не было сахарного диабета и гипертонической болезни, лишь у 7 (23,3%) — отмечалась ВСД по гипертоническому типу.
Для лечения ожирения всем пациенткам был назначен сибутрамин (Меридиа, «Knoll AG», Германия), начальная суточная доза которого составила 10 мг. В тех случаях, когда после первого месяца лечения потеря массы тела была менее 2 кг, дозу препарата увеличивали до 15 мг в сутки. Общая продолжительность лечения составила 12 недель.
Ежемесячно проводилась оценка антропомет рических параметров: массы тела, ИМТ, объема талии и бедер и их соотношения, а также характера менструального цикла.
Исходно и после окончания лечения исследовали липидный спектр крови: холестерин (ХС), триглицериды (ТГ), ХС ЛП низкой плотности (ХС ЛПНП) и ХС ЛП высокой плотности (ХС ЛПВП) и коэффициент атерогенности (КА). Кровь для исследования брали натощак, спустя 12 и более часов после приема пищи. Определение указанных липидных показателей производилось на аппарате «KONE» (Финляндия) с применением специальных, стандартных методик и компьютерной обработки. Полученные результаты оценивали согласно нормативным показателям лаборатории и классификации дислипидемий, принятой ВОЗ.
С целью диагностики нарушений углеводно го обмена пациенткам проводили пероральный 2-х часовой глюкозотолерантный тест (ГТТ) с 75 г глюкозной нагрузки. Уровни глюкозы определялись в цельной капиллярной крови натощак, а также каждые 30 мин в течение 2 ч. Концентра цию глюкозы определяли с использованием тест-полосок на глюкометре фирмы «Джонсон-Джон сон» (США). Диагностику нарушений толерантности к глюкозе проводили согласно классификации, принятой ВОЗ. На фоне ГТТ оценивался также характер секреции иммунореактивного инсулина (ИРИ). Концентрация ИРИ определялась натощак и каждые 30 мин в течение последующих 2 ч исследования. Исследование содержания ИРИ проводилось методом IRMA, c использованием тест-систем ИБОХ (Беларусь), в соответствии с прилагаемыми к ним инструкци ям. Количественную оценку гликемических и инсулиновых ответов на нагрузку глюкозой проводили расчетным путем по величинам молярных площадей (S) под соответствующими секреторными кривыми, рассчитанными по трапецевидному правилу. Исследования проводили в динамике: до начала терапии и после ее окончания.
Исходно и после проведенного курса лечения радиоиммунными методами с использова нием тест-систем «Immunotech» (Чехия) или ИБОХ (Беларусь), согласно приложенным к ним инструкциям, проводили исследование содержания в сыворотке крови больных СТГ и тестостерона (Т).
На фоне терапии сибутрамином у всех пациенток отмечалось снижение массы тела. ИМТ уменьшился с 34,2±0,92 до 31,4±0,84 кг/м 2 (р 5,2 ммоль/л), у 8 (26,7%) — гипертриглицеридемия (ТГ>2,2 ммоль/л) и у 18 (60%) — гипоальфалипопротеи демия, характеризующаяся снижением уровня ХС ЛПВП
Сибутрамин в лечении ожирения (по материалам конгресса «Человек и лекарство». Москва, апрель 2001 г.)
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Эндокринологический научный центр РАМН, Москва
З а последние годы в подходах к терапии ожирения произошли значительные изменения. Пересмотрены сами принципы лечения этого распространенного хронического заболевания, которое по определению должно быть пожизненным. Показано, что нецелесообразно в погоне за идеальными формами тела стараться любыми способами и как можно скорее избавиться от излишнего веса.
Лечение ожирения в первую очередь необходимо направить на предупреждение заболеваемости и увеличение продолжительности жизни пациентов. То есть нужно стремиться к достижению так называемой здоровой массы тела, именно той массы, при которой происходит улучшение или нормализация метаболических нарушений, которую пациент может относительно легко достичь и удержать в течение длительного времени. На сегодняшний день считается клинически значимой и приносящей реальную пользу для здоровья снижение массы тела на 5–10% в течение 4–6 месяцев. При таком подходе, как правило, потеря веса составляет 0,5 –1,0 кг в неделю и преимущественно за счет жировой ткани, реже происходят рецидивы. Причем такое снижение массы тела не требует резкого изменения пищевых привычек и образа жизни пациента. Систематичность наблюдения – не менее важный принцип лечения, особенно на этапе поддержания массы тела. Удержание достигнутой в процессе похудания массы тела является наиболее трудновыполнимой задачей в лечении ожирения. Большинству пациентов для сохранения мотивации и продолжения лечения необходимы постоянное наблюдение и поддержка лечащего врача. Опыт многих центров, которые занимаются лечением ожирения, показывает, что именно систематичность наблюдения оказывает подчас решающую роль в успехе борьбы за поддержание достигнутого в ходе лечения веса и предотвращение его повторной прибавки. Следование пациентом тем рекомендациям по изменению образа жизни и характера питания, которые дал ему врач, обычно со временем ухудшается. В этой связи в терапии ожирения большая роль отводится специальному обучению пациентов, направленному на повышение мотивации и формирование их активной позиции в лечении. Ожирение характеризуется избыточным, патологическим накоплением жировой ткани в организме. На сегодняшний день многие рассматривают ожирение, как состояние дисфункции жировой ткани.
В последние годы показано, что жировая ткань – не только “депо” энергии и место, где происходит метаболизм стероидных гормонов, но и активный эндокринный орган. Установлено, что жировая ткань выделяет более 20 биологически активных веществ, которые участвуют в регуляции потребления пищи, расхода энергии, нейроэндокринных функций, процессов метаболизма. Очевидным доказательством того, что жировая ткань имеет прямое отношение к развитию всех тех нарушений, которые имеют место при ожирении, является тот факт, что при снижении массы тела улучшаются показатели метаболизма и уменьшается вероятность развития тяжелых сопряженных заболеваний.
Ожирение – это результат длительно существующего положительного энергетического баланса, когда поступление энергии с пищей превышает энергетические траты организма. Поэтому все методы лечения ожирения, как немедикаментозные, так и медикаментозные, направлены на уменьшение поступления энергии с пищей и/или увеличение расхода энергии.
Основа лечения ожирения – сбалансированное рациональное питание: гипокалорийное в фазе снижения и эукалорийное на этапе поддержания массы тела. Это регулярный прием пищи с правильным распределением калорийности в течение суток, и, разумеется, ограничение поступления жиров. Жир является наиболее калорийной составляющей пищи, обладает низкой насыщающей способностью и плохо метаболизируется в организме. В последние годы также показано, что избыточное поступление жиров с пищей способствует развитию инсулинорезистентности. Доля жиров в рационе должна составлять не более 30%, углеводов – 55% суточной калорийности, ограничиваются продукты с высоким гликемическим индексом. Увеличение физической активности имеет очень большое значение для увеличения расхода энергии. Кроме того, физическая активность способствует уменьшению абдоминально–висцерального жира, того метаболически активного жира, который играет важную роль в развитии и прогрессировании синдрома инсулинорезистентности.
Целесообразность использования фармакотерапии в лечении ожирения в настоящее время не вызывает сомнений. При применении только немедикаментозных методов лечения нередко не удается достичь желаемых результатов. Медикаментозная терапия при ожирении нужна так же, как при любом другом хроническом заболевании. В принципе любой пациент с ожирением имеет право на медикаментозную поддержку, другое дело – пока такой поддержки мы ему предоставить не можем. Так, если для лечения артериальной гипертонии в распоряжении врача имеется очень широкий арсенал антигипертензивных средств, то для лечения ожирения в настоящее время сертифицировано только 2 препарата. Поэтому вопрос о назначении фармакологического лечения в каждом случае решается индивидуально.
Одним пациентам предпочтительнее назначать в период поддержания массы тела, другим – при нарастании массы тела, а некоторым пациентам медикаментозное лечение следует проводить в самом начале.
Фармакотерапия прежде всего необходима для повышения эффективности немедикаментозных методов лечения. Применение медикаментозной терапии облегчает соблюдение рекомендаций по питанию, способствует более быстрому и эффективному снижению массы тела, а также помогает удержать достигнутую массу тела и предотвратить развитие рецидива. Препараты для лечения ожирения обязательно должны иметь известный механизм действия, быть безопасными при длительном применении и иметь лишь слабые, преходящие побочные эффекты.
Медикаментозная терапия назначается больным с индексом массы тела (ИМТ) > 30 и с ИМТ > 27 кг/м2 – при наличии абдоминального ожирения, либо факторов риска или уже развившихся сопряженных заболеваний, а также при наследственной предрасположенности к ним.
Фармакотерапия не назначается детям до 16 лет, т.к. не проводились соответствующие исследования по безопасности применения препаратов для лечения ожирения у детей. Не применяются фармакопрепараты при беременности и лактации.
Современным препаратом центрального механизма действия нового поколения для лечения ожирения является сибутрамин (Меридиа, “Knoll AG”, Германия). Фармакологическое действие препарата состоит в селективном торможении обратного захвата нейромедиаторов – серотонина и норадреналина из синаптической щели. Вследствие такого двойного действия быстро достигается чувство насыщения и снижается количество потребляемой пищи, при этом вследствие усиления термогенеза увеличивается расход энергии. То есть сибутрамин действует на обе стороны энергетического баланса, способствуя снижению массы тела. Препарат выгодно отличается по механизму действия от препаратов группы амфетаминов и фенфлурамина: не влияет на допаминергическую систему и на высвобождение моноаминов из нервных окончаний.
В крупных многоцентровых плацебоконтролируемых исследованиях эффективности применения препарата, включавших 6000 пациентов, клинически значимое снижение массы тела (і5%) было достигнуто в течение года у 82% пациентов. Снижение массы тела сопровождалось положительными сдвигами со стороны липидного и углеводного обменов. Была отмечена безопасность и хорошая переносимость сибутрамина. Побочные реакции носили преходящий характер и были слабо выражены: сухость во рту, запоры, отсутствие аппетита, бессонница, повышение систолического и диастолического давления в среднем на 2–3 мм рт.ст., увеличение числа сердечных сокращений на 3–5 уд. в мин.
Недавно были опубликованы результаты длительного мультицентрового (8 европейских медицинских центров) рандомизированного плацебоконтролированного исследования клинической эффективности применения сибутрамина с целью снижения и поддержания массы тела в течение в течение 2 лет (STORM – Sibutramine Trial in Obesity Reduction and Maintenance).
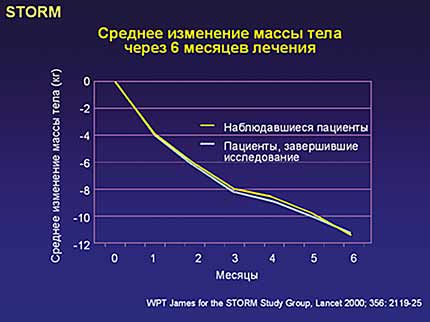
В исследование были включены пациенты (n=605) в возрасте 17–65 лет с ИМТ 30–45 кг/м2. Сибутрамин назначался в суточной дозе 10 мг с рекомендациями по соблюдению умеренно гипокалорийного питания и увеличению физической активности. В течение первой фазы исследования (6 месяцев) – стадия снижения массы тела, 93% исследуемых потеряли >5% исходной массы тела и 54% – более 10%. В среднем снижение массы тела составляло 11,3±5,5 кг (приблизительно 11% от исходной).
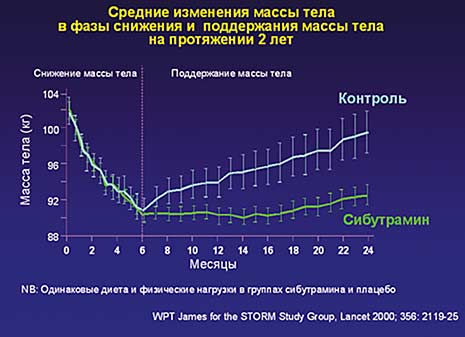
Во вторую фазу исследования (18 месяцев) – стадия поддержания массы тела – были включены пациенты, снизившие массу тела > 5% (n=467). Пациенты были рандомизированы в соотношении 3:1 для приема препарата сибутрамин или плацебо, соответственно. Рекомендации по соблюдению диеты и выполнению физических нагрузок сохранялись в обеих группах. Дозу препарата увеличивали до 15 мг. Если через 6 месяцев отмечалось увеличение массы тела более чем на 1 кг, при продолжающемся увеличении массы тела суточную дозу сибутрамина увеличивали до 20 мг. К окончанию исследования в группе сибутрамина 69% пациентов сохраняли снижение массы тела на 5% от исходной, 46% удерживали 10%-ное снижение массы тела и 27% удерживали достигнутую в фазе снижения массу тела. Снижение массы тела составило 10,2 кг. Отмечено незначительное увеличение массы тела – на 1,1 кг. В контрольной группе 16% пациентов удерживали і 80% достигнутой в процессе снижения массы тела, а на фоне сибутрамина – 43% больных. Масса тела в группе плацебо увеличилась на 6,6 кг и снижение массы тела к окончанию исследования составило 4,7 кг. Среднее различие в массе тела между группами составило 5,5 кг. Окружность талии на фоне приема сибутрамина уменьшилась в среднем на 9,2 см и на 4,5 см на плацебо. Результаты исследования представлены на рисунках 1–4.
У больных с ожирением и дислипидемией на фоне лечения сибутрамином отмечалось снижение уровня общего холестерина (в среднем на 13,5%), триглицеридов (на 14,7%), повышение уровня ХС ЛПВП (на 21%). Снижались также уровни инсулина и С–пептида (на 14,9 и 15,4%, соответственно). Из 51 пациента с артериальной гипертензией, участвовавших в исследовании, 31 принимали сибутрамин в течение 2 лет. Как правило, проводимая антигипертензивная терапия не требовала изменений, за исключением 4 пациентов из группы принимавших сибутрамин. В двух случаях доза антигипертензивных препаратов была увеличена и в двух – снижена. Отмечались незначительные побочные эффекты: бессонница (8% пациентов), тошнота (7%), сухость во рту (9%), увеличение артериального давления (0,1–2,3 мм рт.ст.) и частоты сердечных сокращений (4,1 уд.мин.).
Открытое исследование эффективности и переносимости сибутрамина проведено в 8 российских клинических центрах. В течение 12 недель 160 пациентов с ожирением (ИМТ 27,7–50 кг/м2) получали препарат по 10–15 мг/сут на фоне умеренно гипокалорийного питания и увеличения физической активности. Среди этих пациентов 10 обследованных имели сахарный диабет 2 типа: 9 получали таблетированные сахароснижающие препараты, 1 – инсулинотерапию.
У 12 больных зарегистрирована артериальная гипертония, 9 из них получали антигипертензивную терапию. В результате лечения снижение массы тела > 5% от исходной было достигнуто у 88,1% больных, в том числе і10% – у 25%. В среднем масса тела снизилась на 10,91±2,12 кг. Не ответили на лечение 9 больных, у 10 снижение массы тела составило Меридиа (торговое название)
Ожирение у мужчин. Как помочь пациенту: практические советы
 | Е.Ю. Грицкевич врач-эндокринолог, андролог (г. Москва) |
В ходе урологической интернет-конференции №6 врач-эндокринолог, андролог и специалист по снижению веса Елена Юрьевна Грицкевич выступила с докладом о возможных подходах к решению проблемы ожирения.
Согласно определению ВОЗ, ожирение — это хроническое заболевание, гетерогенное по этиологии и клиническим проявлениям, прогрессирующее при естественном течении, характеризующееся избыточным отложением жировой массы в организме и рецидивирующим характером
Что точнее: ИМТ или окружность талии?
Инструментом, позволяющим оценить наличие и степень выраженности ожирения, является индекс массы тела (ИМТ) — отношение массы тела в килограммах к квадрату роста в метрах (кг/м2). Согласно ВОЗ, диагноз «избыточный вес» или «ожирение» ставится у взрослых в следующих случаях:
Вместе с тем, следует помнить о том, что даже с ИМТ выше нормы пациент может иметь большой процент мышечной массы, а значит, не страдать от ожирения. Ориентироваться на окружность талии в ряде случаев может быть более резонно.
Если раньше мужчины по распространенности ожирения отставали от женщин, то сегодня показатели его распространенности практически равны между полами.
Алгоритм обследования пациента
Индивидуально, по показаниям у пациентов с ожирением может применяться ряд лабораторных методов обследования:
В числе инструментальных методов обследования могут применяться:
Какая диета лучше?
Основные принципы снижения массы тела — это рациональное питание, физическая нагрузка, нормализация углеводного, липидного и других видов обмена при их нарушении, при необходимости — медикаментозная терапия, а при морбидном ожирении — бариатрическая хирургия.
Наиболее подходящая диетотерапия для похудения должна быть безопасной, эффективной и такой, чтобы пациент мог ее придерживаться. Питание должно включать все основные группы пищевых продуктов. Рекомендуется мониторинг съеденной пищи в виде пищевого дневника, в котором также отмечается ежедневная физическая активность. Необходимо учитывать индивидуальные предпочтения в еде, пищевое поведение и схемы питания, а также культурные особенности, традиции и доступность пищи, сроки и финансовые проблемы, пищевые знания и кулинарные навыки.
Низкокалорийные диеты с ограничением содержания жиров приводят к большему снижению общего холестерина и холестерина ЛПНП, с ограничением углеводов — к большему снижению уровня триглицеридов в сыворотке крови и повышению уровня холестерина ЛПВП, а также к большему снижению уровня глюкозы в сыворотке крови HbA1c.
Отдельно Елена Юрьевна упомянула «средиземноморскую» диету, представляющую собой не определенный рацион, а скорее обобщенный термин для нескольких вариантов питания, которые часто встречаются в Греции, Италии и Испании. Средиземноморская диета имеет наиболее последовательную и надежную научную поддержку в снижении риска атеросклеротических сердечно-сосудистых заболеваний. Можно выделить ряд основных принципов такой диеты:
Также можно рассмотреть диету DASH (Dietary Approach to Stop Hypertension), разработанную Национальным институтом сердца, легких и крови США, — главным образом, для коррекции высокого артериального давления.Согласно ей, предпочтительно употребление овощей, фруктов и цельных зерен, обезжиренных или нежирных молочных продуктов, рыбы, птицыи постного мяса, орехов, семян и бобовых, а также волокон и минералов, в частности, кальция, калия и магния. Ограничивается потребление натрия (1500–2300 мг в день), жира (не более 27% от общего количества ежедневных калорий), насыщенных жиров ( 40 кг/м2 — независимо от наличия сопутствующих заболеваний, а также при ИМТ > 35 кг/м2 и наличии тяжелых заболеваний, на течение которых можно воздействовать путем снижения массы тела.
В бариатрической хирургии может применяться ряд методик. В частности, Roux-en-Y обходной желудочный анастомоз обеспечивает существенное улучшение метаболических нарушений, однако связан с повышенным риском развития мальабсорбционных осложнений. Способствует снижению веса до 65–75%. Имеет преимущества при высоком ИМТ, ГЭРБ, сахарном диабете 2 типа.
Лапароскопическое регулируемое бандажирование — наименее инвазивный метод, при этом риск смещения манжеты бандажа равен 25–40% в течение 5 лет. Обеспечивает снижение веса на 30–50%. Используется при ожирении без выраженных метаболических нарушений.
Продольная (рукавная) резекция желудка улучшает метаболические заболевания, не нарушая при этом тонкокишечную анатомию. Может возникать нечастый дефицит микроэлементов. После нее наблюдается снижение веса на 50–70%.
Билиопанкреатическое шунтирование обеспечивает максимальную потерю веса и устранение метаболических заболеваний. Сопряжено с повышенным риском дефицита витаминов и микроэлементов. Это наиболее технически сложный метод, обеспечивающий снижение веса до 70–80%.
Помимо этого, Елена Юрьевна упомянула американскую систему BAROnova с силиконовым устройством TransPyloricShuttle. Внутрижелудочная система имеет малые размеры — на 80–90% меньше, чем баллон. Она изменяет пассаж желудочного содержимого путем замедленного опорожнения желудка. Эффективность системы подтверждена результатами рандомизированного, двойного слепого, плацебо-контролируемого исследования ENDObesity II, в котором приняли участие 302 пациента из девяти исследовательских центров США. Приблизительно 67% пациентов потеряли 5 и более процентов своей массы тела, 40% потеряли 10% веса и более, по сравнению с 14% пациентов в группе плацебо. Резких колебаний артериального давления и других кардио метаболических факторов риска, а также снижения качества жизни при данном лечении не наблюдалось. Побочные эффекты включали в себя желудочно-кишечные явления, такие как боль в животе, тошнота, рвота и диспепсия, как и ожидалось при использовании внутрижелудочного устройства, предназначенного для лечения ожирения посредством замедленного опорожнения желудка.
Другая относительно новая методика — эмболизация левой желудочной артерии. Результаты первых таких операций для снижения веса у человека были представлены в 2013 году. Ранее данная методика применялась для остановки желудочных кровотечений. Исследователи обнаружили, что эмболизация левой желудочной артерии приводит к снижению выработки гормона грелина, участвующего в регуляция голода и насыщения, чем и объясняется снижение массы тела. Среднее снижение веса у пациентов составило 8–9% за первые 2–6 месяцев после операции и 16% — за 2 года. После снижения веса прооперированные удерживали его в течение как минимум года, никаких осложнений не выявлялось. Операция выполняется с использованием микрокатетера, в качестве эмболизационного материала используются сферы из молекул трис-акрила, связанных с молекулами желатина.
В целом, выбор между принятием мер по изменению образа жизни пациента, как подчеркнула Елена Юрьевна, зависит от многих факторов, основными из которых считаются пол пациента, ИМТ, окружность талии и наличие коморбидных патологий.
Материал подготовила В.А. Шадеркина
Видео выступления можно посмотреть на Uro.T
Статья опубликована в журнале «Дайджест урологии» №6-2019