Большая Энциклопедия Нефти и Газа
Малая сжимаемость жидкостей учащимся известна. [39]
Можно считать, что при обычных условиях жидкости практически несжимаемы. Малая сжимаемость жидкостей объясняется тем, что небольшое уменьшение расстояния г между молекулами на малых взаимных расстояниях между ними приводит к появлению больших сил межмолекулярного отталкивания. Понятно, что при очень больших внешних давлениях жидкости должны обнаруживать значительную сжимаемость. Опыты Бриджмена и других показали, что это действительно так. [41]
Количественно сжимаемость жидкостей значительно ближе к сжимаемости твердых тел, чем газов. Малая сжимаемость жидкостей связана с тем, что в них существует огромное молекулярное давление, обусловленное силами притяжения молекул. Величина молекулярного давления составляет от 1000 до 20000 атм. Поскольку жидкости уже сжаты почти до предела внутренними силами, внешнее давление вызывает лишь небольшое дополнительное сжатие. [42]
Все упомянутые явления сцепления объясняются притягательными силами между молекулами. Но малая сжимаемость жидкостей и твердых тел указывает на то, что при некоторых чрезвычайно малых расстояниях появляются, причины, мешающие полному совпадению или соприкосновению соседних молекул. Эти сложные и еще мало изученные изменения сил по всей вероятности связаны с явлениями электрическими и магнитными, сопровождающими очень быстрые движения электронов внутри атомов. [43]
Жидкости имеют малую сжимаемость. Ввиду малой сжимаемости жидкостей во многих случаях практики ею пренебрегают. [44]
Объясните пожалуйста с точки зрения МКТ упругость и малую сжимаемость жидкости?
Объясните пожалуйста с точки зрения МКТ упругость и малую сжимаемость жидкости!
Между молекулами жидкости одновременно действуют как силы притяжения, так и силы отталкивания.
Упругость же объясняется тем, что расстояние между молекулами больше размера самих молекул.
Кроме изохорного нагревания существует изохорное охлаждение?
Кроме изохорного нагревания существует изохорное охлаждение.
Объясните, что при этом происходит с газом с точки зрения МКТ.
ПОМОГИТЕ?
Как с физической точки зрения обьяснить процесс выпивания жидкости?
Чем объясняется малая сжимаемость жидкостей и твердых тел?
Чем объясняется малая сжимаемость жидкостей и твердых тел?
В чем различие сжимаемости газов жидкостей и твердых тел?
В чем различие сжимаемости газов жидкостей и твердых тел.
Почему сжимаемость житкости мало отличается от сжимаемости твёрдих тел?
Почему сжимаемость житкости мало отличается от сжимаемости твёрдих тел?
Чем объясняется малая сжимаемость жидкостей по сравнению с газами?
Чем объясняется малая сжимаемость жидкостей по сравнению с газами?
На основе мкт объяснить качественное различие в молекулярном строении газов, жидкостей и твердых тел?
На основе мкт объяснить качественное различие в молекулярном строении газов, жидкостей и твердых тел.
Пожалуйста, помогите Объясните предложение изречения с физической точки зрения ( то есть как понять и объяснить) Воды в новом кувшине холоднее будет?
Пожалуйста, помогите Объясните предложение изречения с физической точки зрения ( то есть как понять и объяснить) Воды в новом кувшине холоднее будет.
Охарактерезуйте строение твердых тел с точки зрения основных положений МКТ?
Охарактерезуйте строение твердых тел с точки зрения основных положений МКТ.
Почему жидкости плохо сжимаемы?
Почему жидкости плохо сжимаемы?
Потенциальной. То есть газ способен расшириться и совершить работу.
Модуль напряженности найдем по формуле : E = k * q / r² Тогда : Е = 9 * 10⁹ * 5 * 10⁻⁸ / (0, 03)² = 500 000 В / м или 500 кВ / м (Внимание! Вы, наверное неверно указали величину заряда. Получается колоссальная напряженность. Я взял 5 * 10⁻⁸ Кл. )..
Основные положения молекулярно-кинетической теории и их опытное обоснование
Молекулярно-кинетическая теория (МКТ) – это учение, которое объясняет тепловые явления в макроскопических телах и внутренние свойства этих тел движением и взаимодействием атомов, молекул и ионов, из которых состоят тела. В основе МКТ строения вещества лежат три положения:
Эти основные положения подтверждаются экспериментально и теоретически.
Состав вещества
Хаотическое движение частиц
Непрерывное хаотическое движение частиц подтверждается броуновским движением и диффузией. Хаотичность движения означает, что у молекул не существует каких-либо предпочтительных путей и их движения имеют случайные направления. Это означает, что все направления равновероятны.
Диффузия (от латинского diffusion – растекание, распространение) – явление, когда в результате теплового движения вещества происходит самопроизвольное проникновение одного вещества в другое (если эти вещества соприкасаются).
Взаимное перемешивание веществ происходит по причине непрерывного и беспорядочного движения атомов или молекул (или других частиц) вещества. С течением времени глубина проникновения молекул одного вещества в другое увеличивается. Глубина проникновения зависит от температуры: чем выше температура, тем больше скорость движения частиц вещества и тем быстрее протекает диффузия.
Диффузия наблюдается во всех состояниях вещества – в газах, жидкостях и твёрдых телах. Примером диффузии в газах служит распространение запахов в воздухе при отсутствии прямого перемешивания. Диффузия в твёрдых телах обеспечивает соединение металлов при сварке, пайке, хромировании и т.п. В газах и жидкостях диффузия происходит намного быстрее, чем в твёрдых телах.
Взаимодействие частиц
Существование устойчивых жидких и твёрдых тел объясняется наличием сил межмолекулярного взаимодействия (сил взаимного притяжения и отталкивания). Этими же причинами объясняется малая сжимаемость жидкостей и способность твёрдых тел сопротивляться деформациям сжатия и растяжения.
Силы межмолекулярного взаимодействия имеют электромагнитную природу – это силы электрического происхождения. Причиной этого является то, что молекулы и атомы состоят из заряженных частиц с противоположными знаками зарядов – электронов и положительно заряженных атомных ядер. В целом молекулы электрически нейтральны. По электрическим свойствам молекулу можно приближённо рассматривать как электрический диполь.
Силы притяжения принято считать отрицательными, а силы отталкивания – положительными, хотя это деления является условным.
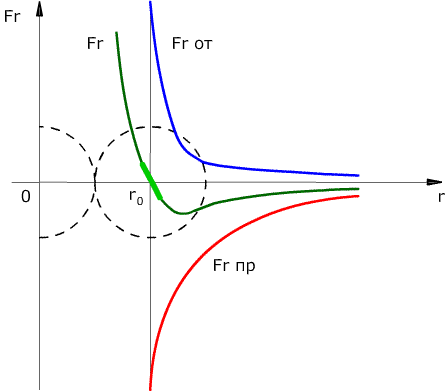
Сила взаимодействия между молекулами имеет определённую зависимость от расстояния между молекулами. Эта зависимость изображена на рис. 1.1. Здесь показаны проекции сил взаимодействия на прямую, которая проходит через центры молекул.
Рис. 1.1. Зависимость межмолекулярных сил от расстояния между взаимодействующими атомами.
Как видим, по мере уменьшения расстояния между молекулами r сила притяжения Fr пр увеличивается (красная линия на рисунке). Как уже было сказано, силы притяжения принято считать отрицательными, поэтому по мере уменьшения расстояния кривая уходит вниз, то есть в отрицательную зону графика.
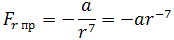 | (1.1) |
где a – коэффициент, зависящий от вида сил притяжения и строения взаимодействующих молекул.
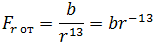 | (1.2) |
где b – коэффициент, зависящий от вида сил отталкивания и строения взаимодействующих молекул.
На расстоянии r = r0 (это расстояние примерно равно сумме радиусов молекул) силы притяжения уравновешивают силы отталкивания, а проекция результирующей силы Fr = 0. Этому состоянию соответствует наиболее устойчивое расположение взаимодействующих молекул.
В общем случае результирующая сила равна:
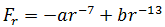 | (1.3) |
При r > r0 притяжение молекул превосходит отталкивание, при r
Броуновское движение (или брауновское движение ) – это непрерывное хаотическое движение малых частиц, взвешенных в жидкости или газе (при этом подразумевается, что сила тяжести не влияет на их движение).
Это явление впервые наблюдал Роберт Броун (Браун, годы жизни 1773 – 1858), когда рассматривал в микроскоп движение цветочной пыльцы, взвешенной в воде. В наше время для таких наблюдений используют маленькие части краски гуммигут, которая не растворяется в воде. В газе броуновское движение совершают, например, взвешенные в воздухе частицы пыли или дыма.
Броуновское движение частицы возникает потому, что импульсы, с которыми молекулы жидкости или газа действуют на эту частицу, не компенсируют друг друга. Молекулы среды (то есть молекулы газа или жидкости) движутся хаотично, поэтому их удары приводят броуновскую частицу в беспорядочное движение: броуновская частица быстро меняет свою скорость по направлению и по величине.
Броуновское движение – это тепловое движение, интенсивность которого возрастает с ростом температуры среды и продолжается неограниченно долго без каких-либо видимых изменений.Интенсивность броуновского движения также возрастает с уменьшением размера и массы частиц, а также при уменьшении вязкости среды.
Броуновское движение служит наиболее наглядным экспериментальным подтверждением существования атомов (молекул) и их хаотического теплового движения. Полнаямолекулярно-кинетическая теория броуновского движения была дана в 1905 – 1906 годах немецким учёным Альбертом Эйнштейном (1879 – 1955) и польским физиком Марианом Смолуховским (1872 – 1917). В 1908 – 1911 годах французский учёный Жан Перрен (1870 – 1942) провёл серию экспериментов по изучению броуновского движения и окончательно подтвердил закономерности этого движения, предсказанные на основе молекулярно-кинетической теории.
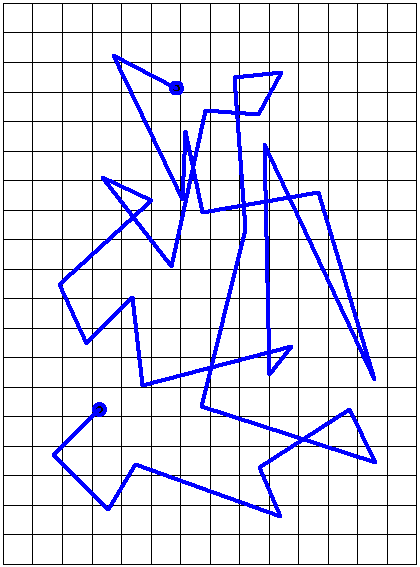
Рис. 1.2. Траектория движения броуновской частицы (частиц краски гуммигута в воде по Перрену).
Броуновское движение, например, в метрологии, является основной причиной, по которой точность чувствительных измерительных приборов ограничена, потому что тепловое движение атомов деталей приборов и окружающей среды вызывает дрожание стрелок измерительных приборов.
Масса и размер молекул
Многие опыты показывают, что размер молекулы очень мал. Линейный размер молекулы или атома можно найти различными способами. Например, с помощью электронного микроскопа, получены фотографии некоторых крупных молекул, а с помощью ионного проектора (ионного микроскопа) можно не только изучить строение кристаллов, но определить расстояние между отдельными атомами в молекуле.
Для характеристики атомов используют представление об атомных радиусах, которые дают возможность приближённо оценить межатомные расстояния в молекулах, жидкостях или твёрдых телах, так как атомы по своим размерам не имеют чётких границ. То естьатомный радиус – это сфера, в которой заключена основная часть электронной плотности атома (не менее 90…95%).
Размер молекулы настолько мал, что представить его можно только с помощью сравнений. Например, молекула воды во столько раз меньше крупного яблока, во сколько раз яблоко меньше земного шара.
Моль вещества
Массы отдельных молекул и атомов очень малы, поэтому в расчётах удобнее использовать не абсолютные значения масс, а относительные.
Относительная молекулярная масса (или относительная атомная масса) вещества Мr – это отношение массы молекулы (или атома) данного вещества к 1/12 массы атома углерода.
где m0 – масса молекулы (или атома) данного вещества, m0C – масса атома углерода.
Относительная молекулярная масса вещества может быть вычислена путём сложения относительных атомных масс элементов, входящих в состав молекулы вещества. Относительная атомная масса химических элементов указана в периодической системе химических элементов Д.И. Менделеева.
В периодической системе Д.И. Менделеева для каждого элемента указана атомная масса, которая измеряется в атомных единицах массы (а.е.м.). Например, атомная масса магния равна 24,305 а.е.м., то есть магний в два раза тяжелее углерода, так как атомная масса углерода равна 12 а.е.м. (это следует из того, что 1 а.е.м. = 1/12 массы изотопа углерода, который составляет большую часть атома углерода).
Зачем измерять массу молекул и атомов в а.е.м., если есть граммы и килограммы? Конечно, можно использовать и эти единицы измерения, но это будет очень неудобно для записи (слишком много чисел придётся использовать для того, чтобы записать массу). Чтобы найти массу элемента в килограммах, нужно атомную массу элемента умножить на 1 а.е.м. Атомная масса находится по таблице Менделеева (записана справа от буквенного обозначения элемента). Например, вес атома магния в килограммах будет:
Массу молекулы можно вычислить путём сложения масс элементов, которые входят в состав молекулы. Например, масса молекулы воды (Н2О) будет равна:
Количество вещества принято считать пропорциональным числу частиц. Количество вещества – это физическая величина, характеризующая относительное число молекул и атомов в теле. Единица количества вещества называется молем (моль).
Постоянная Авогадро
Количество вещества ν равно отношению числа молекул в данном теле к числу атомов в 0,012 кг углерода, то есть количеству молекул в 1 моле вещества.
где N – количество молекул в данном теле, NA – количество молекул в 1 моле вещества, из которого состоит тело.
NA – это постоянная Авогадро. Количество вещества измеряется в молях.
Постоянная Авогадро – это количество молекул или атомов в 1 моле вещества. Эта постоянная получила своё название в честь итальянского химика и физика Амедео Авогадро (1776 – 1856).
В 1 моле любого вещества содержится одинаковое количество частиц.
Молярная масса – это масса вещества, взятого в количестве одного моля:
где m0 – масса молекулы.
Молярная масса связана с относительной молекулярной массой соотношением:
Масса любого количества вещества m равна произведению массы одной молекулы m0 на количество молекул:
Количество вещества равно отношению массы вещества к его молярной массе:
Массу одной молекулы вещества можно найти, если известны молярная масса и постоянная Авогадро:
Более точное определение массы атомов и молекул достигается при использовании масс-спректрометра – прибора, в котором происходит разделение пучком заряженных частиц в пространстве в зависимости от их массы заряда при помощи электрических и магнитных полей.
Как видим, молярная масса (в граммах) практически равна атомной массе, указанной для элемента в таблице Менделеева. Поэтому когда указывают атомную массу, то обычно делают так:
Движение молекул в газах, жидкостях и твёрдых телах
Молекулярно-кинетическая теория даёт объяснение тому, что все вещества могут находиться в трёх агрегатных состояниях: в твёрдом, жидком и газообразном. Например, лёд, вода и водяной пар. Часто плазму считают четвёртым состоянием вещества.
Агрегатные состояния вещества (от латинского aggrego – присоединяю, связываю) – состояния одного и того же вещества, переходы между которыми сопровождаются изменением его физических свойств. В этом и заключается изменение агрегатных состояний вещества.
Во всех трёх состояниях молекулы одного и того же вещества ничем не отличаются друг от друга, меняется только их расположение, характер теплового движения и силы межмолекулярного взаимодействия.
Движение молекул в газах
В газах обычно расстояние между молекулами и атомами значительно больше размеров молекул, а силы притяжения очень малы. Поэтому газы не имеют собственной формы и постоянного объёма. Газы легко сжимаются, потому что силы отталкивания на больших расстояниях также малы. Газы обладают свойством неограниченно расширяться, заполняя весь предоставленный им объём. Молекулы газа движутся с очень большими скоростями, сталкиваются между собой, отскакивают друг от друга в разные стороны. Многочисленные удары молекул о стенки сосуда создаютдавление газа.
Движение молекул в жидкостях
Время оседлой жизни уменьшается с повышением температуры. Расстояние между молекулами жидкости меньше размеров молекул, частицы расположены близко друг к другу, а межмолекулярное притяжение велико. Тем не менее, расположение молекул жидкости не является строго упорядоченным по всему объёму.
Жидкости, как и твёрдые тела, сохраняют свой объём, но не имеют собственной формы. Поэтому они принимают форму сосуда, в котором находятся. Жидкость обладает таким свойством, кактекучесть. Благодаря этому свойству жидкость не сопротивляется изменению формы, мало сжимается, а её физические свойства одинаковы по всем направлениям внутри жидкости (изотропия жидкостей). Впервые характер молекулярного движения в жидкостях установил советский физик Яков Ильич Френкель (1894 – 1952).
Движение молекул в твёрдых телах
Молекулы и атомы твёрдого тела расположены в определённом порядке и образуют кристаллическую решётку. Такие твёрдые вещества называют кристаллическими. Атомы совершают колебательные движения около положения равновесия, а притяжение между ними очень велико. Поэтому твёрдые тела в обычных условиях сохраняют объём и имеют собственную форму.
Тепловое равновесие
Тепловое равновесие (или термодинамическое равновесие) – это такое состояние, при котором все макроскопические параметры сколь угодно долго остаются неизменными.
В состоянии термодинамического равновесия не происходит теплообмен с окружающими телами, не изменяются объём и давление тела, отсутствуют взаимные превращения жидкостей, газов и твёрдых тел.
Температура и её физический смысл
Любая термодинамическая система при неизменных внешних условиях самопроизвольно переходит в состояние термодинамического равновесия.
Температура тела – это физический параметр, одинаковый во всех частях системы тел, которая находится в состоянии термодинамического равновесия.
При тепловом равновесии микроскопические процессы внутри тела (движение частиц и взаимодействие частиц) не прекращаются. Термодинамическая система может находиться в различных состояниях теплового равновесия, каждому из которых соответствует определённое значение температуры. При теплообмене между телами происходит обмен энергией: тела с большей энергией передают свою энергию телам с меньшей энергией. Направление теплообмена между ними указывает разность температур тел. То есть энергия передаётся от более горячего тела к менее горячему.
Температура и её измерение
Для измерения температуры используется тот факт, что с изменением температуры тела изменяются почти все его физические свойства: длина, объём, плотность, электрическое сопротивление, упругие свойства и др. Основой для измерения температуры может являться изменение какого-либо свойства термометрического тела.
Термометрическое тело – это тело, для которого известна зависимость какого-либо свойства данного тела от температуры. Термометрическим телом может быть, например, жидкость или газ, для которого известна зависимость изменения его объёма от температуры.
Эмпирическая шкала – это температурная шкала, установленная с помощью термометрического тела.
Наиболее распространён способ измерения температуры с помощьюжидкостного термометра, в котором используется расширение жидкости (изменение объёма) при нагревании.
При градуировке термометра отмечают опорные точки, расстояние между которыми на шкале делят на равные части, которые называются градусами.
Шкала температур Цельсия
Для практического употребления по решению IX Генеральной конференции по мерам и весам в 1948 году была принята международная стоградусная температурная шкала – шкала Цельсия.
Шведский физик и астроном Андерс Цельсий (1701 – 1744) в 1742 году предложил шкалу термометра, в которой за ноль градусов (начало отсчёта температуры) принял температуру таяния льда, а за сто градусов – температуру кипения воды при нормальном атмосферном давлении в 1,01325 * 10 5 Па. Изменение длины столба жидкости в термометре на одну сотую долю длины между отметками 0 и 100 °С соответствует изменению температуры на 1 °С. По данной шкале единица измерения температуры – градус Цельсия.
Перевести градусы из Цельсия в Фаренгейт можно так:
Перевод из Фаренгейта в Цельсий:
Здесь tF – температура по Фаренгейту, tC – температура по Цельсию
Итоговый тест по физике для 7 класса к учебнику А.В.Перышкин по главе 1. «Первоначальные сведения о строении вещества. Вариант 3
Тест: C:\Users\Рамзия\Desktop\7 класс\итоговый тест по главе 1. Первоначальные сведения о строении вещества. Вариант 3.mtf
2) его физические свойства
3) физические величины, характеризующие размеры тел
4) среди ответов нет верного
К физическим телам относятся
К веществам относятся
Выразите длину тела, равную 70 дм, в сантиметрах и метрах.
Определите цену деления изображённой здесь шкалы прибора.
Каков объём налитой в мензурку воды? Какая погрешность допущена?
Цена деления шкалы весов 10 г. С какой погрешностью взве ¬ шивают на них продукты?
1) невидимая глазом частица
2) очень маленькая частица тела
3) мельчайшая частица вещества, из которого состоит тело
Молекулы в веществе взаимодействуют:
1) притягиваются друг к другу
2) отталкиваются друг от друга
3) иногда притягиваются, иногда отталкиваются
4) в зависимости от расстояния между ними преобладает то притяжение, то отталкивание
Чем отличаются молекулы в куске свинца от молекул в расплавленном свинце?
1) Проникновение беспорядочно движущихся молекул одного вещества в промежутки между молекулами другого вещества
2) Перемешивание жидких веществ
3) Сокращение промежутков между молекулами при сжатии тел
4) Перемещение одних молекул среди других по промежуткам между ними
Чтобы диффузия происходила быстрее, надо
1) поместить контактирующие тела в холодное место
2) поместить их в тёмное место
4) отодвинуть от нагревателя
4) Во всех телах одинаково
Какие общие свойства имеют газы?
1) Собственную форму
2) Собственный объём
3) Отсутствие собственного объёма и формы
4) Лёгкую сжимаемость
Какие общие свойства характерны для твёрдых тел?
1) Наличие собственных объёма и формы
2) Сохранение объёма и изменчивость формы
3) Отсутствие собственных объёма и формы
4) Сохранение формы и изменчивость объёма
Какими общими свойствами обладают жидкости?
1) Собственной формой
2) Собственным постоянным объёмом
3) Малой сжимаемостью
4) Способностью занимать объём сосуда
4) В любом из трёх состояний
Почему газы занимают всё предоставленное им пространство?
1) Потому что их молекулы быстро движутся
2) Из-за отталкивания молекул друг от друга
3) Вследствие диффузии
4) Потому что молекулы газа практически не взаимодействуют и движутся во всех направлениях
Как движутся и взаимодействуют молекулы твёрдого тела?
1) Слабо взаимодействуют и движутся хаотично, но медленно
2) Сильно взаимодействуют и не движутся
Чем объясняется малая сжимаемость жидкостей?
1) Достаточно близким друг к другу расположением молекул
2) Относительно большими размерами их молекул
3) Быстротой движения молекул
1) (1 б.) Верные ответы: 3;
2) (1 б.) Верные ответы: 1; 4;
3) (1 б.) Верные ответы: 2;
4) (1 б.) Верные ответы: 3;
5) (1 б.) Верные ответы: 2;
6) (1 б.) Верные ответы: 4;
7) (1 б.) Верные ответы: 3;
8) (1 б.) Верные ответы: 3;
9) (1 б.) Верные ответы: 4;
10) (1 б.) Верные ответы: 1;
11) (1 б.) Верные ответы: 1;
12) (1 б.) Верные ответы: 3;
13) (1 б.) Верные ответы: 1;
14) (1 б.) Верные ответы: 2; 3;
15) (1 б.) Верные ответы: 1;
16) (1 б.) Верные ответы: 2; 3;
17) (1 б.) Верные ответы: 4;
18) (1 б.) Верные ответы: 4;
19) (1 б.) Верные ответы: 3;
20) (1 б.) Верные ответы: 1;
Если Вы считаете, что материал нарушает авторские права либо по каким-то другим причинам должен быть удален с сайта, Вы можете оставить жалобу на материал.
Курс повышения квалификации
Дистанционное обучение как современный формат преподавания
Курс профессиональной переподготовки
Физика: теория и методика преподавания в образовательной организации
Курс профессиональной переподготовки
Методическая работа в онлайн-образовании
Ищем педагогов в команду «Инфоурок»
Найдите материал к любому уроку, указав свой предмет (категорию), класс, учебник и тему:
также Вы можете выбрать тип материала:
Общая информация
Похожие материалы
Итоговый тест по физике для 7 класса к учебнику А.В Перышкин по главе 1. «Первоначальные сведения о строении вещества.» Вариант 2
Тематический тест по физике для 7 класса к учебнику А.В. Перышкина «Физика 7 класс» «Тест 37. Энергия»
Тематический тест по физике для 7 класса к учебнику А.В. Перышкина «Физика 7 класс» «Тест 36. Коэффициент полезного действия механизма»
Тематический тест по физике для 7 класса к учебнику А.В. Перышкина «Физика 7 класс» «Тест 35. Центр тяжести. Условия равновесия тел.»
Тематический тест по физике для 7 класса к учебнику А.В. Перышкина «Физика 7 класс» «Тест 34. Золотое правило механики»
Тематический тест по физике для 7 класса к учебнику А.В. Перышкина «Физика 7 класс» «Тест 33. Блоки»
Презентация по физике «Задачи с историей»
Тематический тест по физике для 7 класса к учебнику А.В. Перышкина «Физика 7 класс» «Тест 32. Момент силы. Применение рычагов»
Не нашли то что искали?
Воспользуйтесь поиском по нашей базе из
5353109 материалов.
Вам будут интересны эти курсы:
Оставьте свой комментарий
Авторизуйтесь, чтобы задавать вопросы.
Безлимитный доступ к занятиям с онлайн-репетиторами
Выгоднее, чем оплачивать каждое занятие отдельно
ДНР полностью перешла на стандарты и программы России в образовании
Время чтения: 1 минута
В России утверждены новые аккредитационные показатели для школ и колледжей
Время чтения: 2 минуты
Учителям предлагают 1,5 миллиона рублей за переезд в Златоуст
Время чтения: 1 минута
К 2024 году в каждой российской школе должен появиться спортивный клуб
Время чтения: 2 минуты
В Ленобласти педагоги призеров и победителей олимпиады получат денежные поощрения
Время чтения: 1 минута
Путин поручил не считать выплаты за классное руководство в средней зарплате
Время чтения: 1 минута
Подарочные сертификаты
Ответственность за разрешение любых спорных моментов, касающихся самих материалов и их содержания, берут на себя пользователи, разместившие материал на сайте. Однако администрация сайта готова оказать всяческую поддержку в решении любых вопросов, связанных с работой и содержанием сайта. Если Вы заметили, что на данном сайте незаконно используются материалы, сообщите об этом администрации сайта через форму обратной связи.
Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления. Авторские права на материалы принадлежат их законным авторам. Частичное или полное копирование материалов сайта без письменного разрешения администрации сайта запрещено! Мнение администрации может не совпадать с точкой зрения авторов.