Доброкачественные опухоли легких
1. Что такое доброкачественная легких и ее симптомы?
Опухоли легких во многих случаях не являются злокачественными, т.е диагноз рак легких при наличии опухоли ставится не всегда. Нередко легких имеет характер доброкачественной.
Узелки и точки в легких можно увидеть на рентгеновском снимке или компьютерной томографии. Они представляют собой плотные небольшие участки ткани круглой или овальной формы, окруженные здоровыми тканями легких. Узелок может быть один или несколько.
По статистике, новообразования в легких чаще всего оказываются доброкачественными, если:
Доброкачественная легких появляется в результате аномального роста тканей и может развиваться в различных частях легких. Определить, является ли легких доброкачественной или злокачественной очень важно. И сделать это нужно как можно раньше, ведь раннее выявление и лечение рака легких существенно повышает вероятность полного излечения и, в итоге, выживания пациента.
Симптомы доброкачественной опухоли легких
Доброкачественные узелки и опухоли в легких обычно не вызывают никаких симптомов. Именно поэтому ни практически всегда диагностируются случайно во время рентгена грудной клетки или компьютерной томографии.
Однако они могут стать причиной следующих симптомов болезни:
2. Причины доброкачественных опухолей
Причины того, почему появляются доброкачественные опухоли легких, мало изучены. Но в целом они часто появляются после таких проблем со здоровьем, как:
Воспалительные процессы, возникшие из-за инфекции:
Воспаление, не связанное с инфицированием:
3. Виды опухолей
Вот некоторые из наиболее распространенных типов доброкачественных опухолей легких:
4. Диагностика и лечение
Диагностика доброкачественных опухолей легких
Помимо рентгеновского обследования и компьютерной томографии для диагностики опухолей легких, о которых мы уже говорили, диагностика состояния здоровья пациента может заключаться в контроле динамики развития опухоли в течение нескольких лет. Обычно такая практика используется, если размер узелка не превышает 6 мм и пациент не входит в группу риска по заболеванию раком легких. Если узелок остается того же размера, по крайней мере, два года, он считается доброкачественным. Это связано с тем, что доброкачественные опухоли легких растут медленно, если вообще растут. Раковые опухоли, напротив, удваиваются в размере каждые четыре месяца. Дальнейшее ежегодной наблюдение, по меньшей мере, в течение пяти лет поможет окончательно убедиться, что легких доброкачественная.
Доброкачественные узелки в легких обычно имеют гладкие края и более равномерный цвет по всей поверхности. Они более правильной формы, чем раковые узелки. В большинстве случаев для проверки скорости роста, формы и других характеристик опухоли (к примеру, кальцификации), достаточно рентгена грудной клетки или компьютерной томографии (КТ).
Но возможно, что Ваш назначит и другие исследования, особенно если изменила размер, форму или внешний вид. Это делается для того, чтобы исключить рак легких или определить основную причину появления доброкачественных узелков.
Для диагностики может потребоваться:
Биопсия может быть выполнена при помощи различных методов, например, аспирации иглой или бронхоскопии.
Лечение доброкачественных опухолей легких
Во многих случаях специфическое лечение доброкачественной опухоли легких не требуется. Тем не менее, удаление новообразования может быть рекомендовано в том случае, если:
Если для лечения опухоли легких требуется операция, ее проводит торакальный хирург. Современные методики и квалификация торакального хирурга позволяют выполнить операцию с небольшими разрезами, и сокращают время пребывания в стационаре. Если удаленные узелок был доброкачественным, дальнейшее лечение не потребуется, за исключением тех случаев, когда наличие опухоли осложнялось другими проблемами, к примеру, пневмонией или обструкцией.
Иногда для лечения требуется более сложная инвазивная операция, в ходе которой удаляется узелок или часть легких. Какая именно операция будет необходима, решает врач, учитывая местоположение и тип опухоли.
Кальцинаты в легких
Здравствуйте! В 2016 году на кт были обнаружены многочисленные кальцинаты в легких. Повторные кт 2017 и 2019 года без динамики. В анамнезе хронический бронхит. В 1995, 2002, 2007, 2013 перенес пневмонию. В сентябре 2019 года в общем анализе крови были повышены лейкоциты, температура 37,3 и хрипы. Терапевт назначил лечение в том числе вильпрофен. В ноябре ситуация повторилась. Пульмонолог назначил клацид и консультацию фтизиатра. Фтизиатр назначил т спот и пцр. Т спот положительный, пцр отрицательный. По кт рентгенолог, которого привлек фтизиатр, увидел мелкие плотные очаги и немногочисленные кальцинаты в обоих легких и дал заключение: остаточные изменения, вероятно после диссеменированного туберкулеза легких и вглу (или микобактериоза). Рентгенологи, которые делали кт, писали заключение множественные кальцинаты без динамики. На момент обращения к фтизиатру, Общий анализ крови, после клацид, в норме, лейкоциты норма, соэ норма, только моноциты 0,8. Вес постоянно стабильный, сильного кашля, болей в груди, отдышки, ночной потливости нет, мокроты мало и без крови. Фтизиатр собирается поставить диагноз туберкулез легких и внести в реестр туберкулезных больных с сообщением по месту работы и жительства, либо предлагает пройти дообследование у них в клинике. подскажите, пожалуйста, насколько законно ставить диагноз туберкулез в данном случае и вносить в реестр, если кальцинаты были обнаружены в 2016 году случайно, динамики нет, пцр отрицательный. Насколько корректно было назначать т спот, если он не показывает закрытую форму и открытую. А кальцинаты в легких явно дают понять, что т спот априори будет положительным.
Хронические болезни: Хронический бронхит
Обызвествленные очаги в легких что
Интерес к этому загадочному заболеванию велик: в 1987 году создана Всемирная ассоциация по саркоидозу и гранулематозам. На различных форумах пульмонологов работают отдельные секции по саркоидозу и другим гранулематозам. Ежегодно публикуется ряд статей, издаются монографии [1].
Однако многие вопросы остаются нерешёнными. До конца не изучена этиология заболевания. Клинические проявления весьма различны и не патогномоничны. Нередко преобладают симптомы внелегочных форм саркоидоза, например иридоциклит, увеличение шейных, подмышечных и надлобковых лимфатических узлов, поражения кожи по типу волчанки, артралгии, лихорадка и др. В половине случаев клинические признаки заболевания отсутствуют. Все вышесказанное значительно затрудняет раннюю диагностику саркоидоза [1; 3; 4].
Долгое время больные саркоидозом наблюдались в противотуберкулёзных стационарах, и это было весьма нецелесообразно из-за длительного наблюдения за пациентами и возможности их заражения туберкулёзом. В настоящее время и в России, и за рубежом диспансерное наблюдение за больными саркоидозом передано с общую лечебную сеть врачам-пульмонологам, хотя у них и нет достаточного опыта работы с этими пациентами.
Саркоидоз до сих пор остаётся заболеванием с неясной этиологией. В настоящее время существует ряд гипотез, пытающихся объяснить причины развития саркоидоза: связь с инфекционными факторами, экзогенное воздействие окружающей среды (вдыхание пыли, дыма и прочее), курение, наследственность и другие.
Основу патоморфогенеза саркоидоза составляет эпителиоидная гранулёма, состоящая из эпителиоидных клеток, гигантских клеток Лангханса, кальцинированных тел Шауманна и «звездчатых тел». Саркоидная гранулема не подвергается казеозному некрозу, в отличие от туберкулеза [1; 3].
Выделяют 3 патогенетические стадии саркоидоза лёгких:
1. Негранулематозная (альвеолит) – на этой стадии наблюдается утолщение альвеолярных перегородок, скопление макрофагов и лимфоцитов. Типичным является увеличение лимфатических узлов.
2. Гранулематозная – на этой стадии образуются саркоидные гранулёмы без некроза. Исход гранулёмы: рассасывание либо гиалиновая фибротизация.
3. Фиброзная – при хроническом течении заболевания фиброз развивается у 10–20% пациентов и имеет распространённый характер. В лёгких образуются кистозные полости, грубые ретикулярные изменения и лёгочная ткань напоминает «медовые соты». Кисты возникают в результате растяжения альвеолярной ткани и образования бронхиолоэктазов. Одновременно развивается выраженная эмфизема, стенозы бронхов, за счёт поражения их стенок. Чаще изменения носят двусторонний характер [1].
Саркоидоз, являясь системным заболеванием, поражает разные органы и системы, помимо респираторной системы: кожа (27%), периферические лимфатические узлы (22%), глаза (15%), (6%), центральная нервная система (4%), паращитовидные железы (4%), кости (3%). Однако известно, что 90% больных саркоидозом имеют изменения в органах грудной полости. Таким образом, клинические симптомы многообразны, зависят от ряда факторов, в том числе от этнической принадлежности пациента, формы, давности болезни, фазы, локализации и распространённости процесса, а также его активности. Среди клинических симптомов выделяют общие, т.е. неспецифические, такие как лихорадка, слабость и др., а также клинические проявления, вызванные поражением различных органов [5; 6].
Диагностика саркоидоза включает клинико-лабораторные исследования, лучевую визуализацию (рентгенологические методы, в т.ч. компьютерную томографию) и морфологическую верификацию.
Цель исследования: продемонстрировать многообразие компьютерно-томографических признаков и оценить диагностические возможности мультиспиральной компьютерной томографии при саркоидозе органов грудной полости.
Материал и методы исследования. Мы располагаем большим консультативным материалом – данные компьютерной томографии более 300 пациентов с саркоидозом органов грудной полости в период с 2011 по 2018 год. Преимущественный возраст больных варьировал от 25 до 45 лет, что соответствует данным литературы. Соотношение мужчин и женщин было примерно одинаковым. Лучевое исследование проводилось всем больным и включало рентгенографию органов грудной клетки в прямой и боковой проекциях и мультиспиральную компьютерную томографию. Последняя выполнялась на компьютерном томографе Somatom Emotion-6 Simens (6-срезовый МСКТ) и аппарате Aquillion-TSX-101 (64-срезовый МСКТ) по стандартной методике с толщиной среза около 1,5 мм и реконструкцией изображений в режимах легочного и медиастинального окна.
Результаты исследования и их обсуждение
Важнейшая роль в выявлении и установлении диагноза принадлежит рентгенологическому методу исследования, включающему обзорную рентгенографию органов грудной полости в прямой и боковой проекциях, а также компьютерной томографии. Примерно в половине (50%) наших случаев патологические изменения выявлены при проверочной флюорографии органов грудной клетки. Рентгенография и КТ позволили детализировать и уточнить характер патологических изменений, а также наблюдать за динамикой на фоне лечения саркоидоза.
Основу КТ-симптомокомплекса саркоидоза составили: 1) преимущественно двустороннее увеличение средостенных лимфатических узлов, 2) диссеминированные легочные гранулёмы, 3) фиброз, рубцевание, в некоторых случаях образование полостей в легочной ткани.
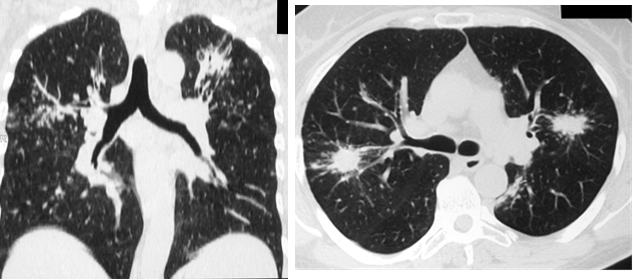
Рис. 1. РК-томограммы (медиастинальное окно) пациентки Е., 39 лет. Отмечается увеличение ВГЛУ паратрахеальной, бифуркационной и бронхопульмональной групп
Внутригрудная лимфоаденопатия визуализировалась в 70-80% случаев. Наблюдалось преимущественно двустороннее увеличение внутригрудных лимфатических узлов (ВГЛУ). Причем паратрахеальные лимфоузлы увеличивались как симметрично с обеих сторон, так и односторонне, чаще справа. Левостороннее увеличение демонстрировали лимфоузлы аортопульмонального окна. В некоторых случаях отмечалось обызвествление ВГЛУ в виде пунктира, по типу «скорлупы ореха» или аморфное. Симптом внутригрудной лимфоаденопатии наблюдался как изолированно, так и в сочетании с изменениями в легочной ткани. На компьютерных томограммах в режиме медиастинального окна увеличенные узлы средостения визуализировались достаточно хорошо (рис. 1).
Симптоматика изменений в лёгких при саркоидозе сводилась к появлению признаков в виде симптома «матового стекла», диссеминации, очаговых теней, пневмофиброза, буллёзно-дистрофических изменений и др. Относительно редко наблюдался плевральный выпот и симптом кольцевидной тени (образование полостей) в легких. У некоторых пациентов отмечалось изолированное поражение легких без лимфоаденопатии.
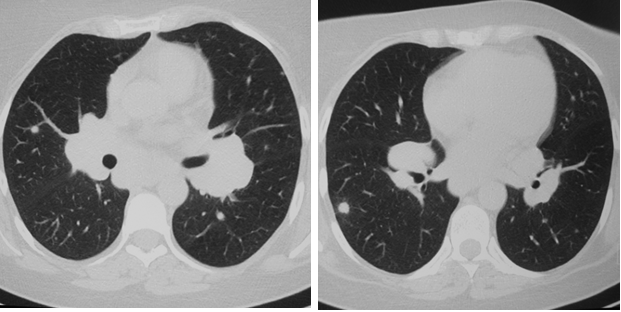
Симптом «матового стекла» (36%) визуализировался в виде небольших, ограниченных участков снижения прозрачности лёгочной ткани (рис. 2).
Рис. 2. РК-томограммы (режим лёгочного окна) пациента Г., 28 лет, с саркоидозом легких и ВГЛУ. Стрелкой указаны участки «матового стекла»
На ранних стадиях заболевания симптом «матового стекла» мог быть единственным, либо сочетаться с увеличением ВГЛУ.
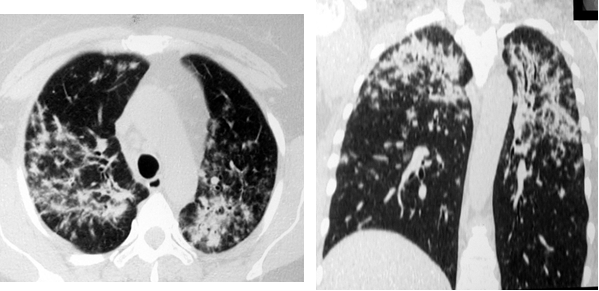
Одним из наиболее часто наблюдаемых нами при КТ признаков саркоидоза являлся симптом диссеминации (70-80% случаев). При этом превалировала картина интерстициальных изменений с ретикуло-нодулярными фокусами размерами около 1-2 мм. Распределение теней было, главным образом, перилимфатическим с локализацией в средних и верхних легочных зонах (рис. 3). Реже визуализировались гроздевидные очаги округлой или неправильной формы до 6 мм в диаметре, с преимущественно субплевральной локализацией.
Рис. 3. На РК-томограммах больной Ж., 49 лет, определяется двухсторонняя диссеминация с преимущественной локализацией в среднем легочном поясе
Еще одним относительно частым (20-30%) проявлением легочного саркоидоза являлся симптом локальной тени, в виде ограниченных фокусов консолидации. Как правило, изменения носили двусторонний характер с локализацией в средних и верхних легочных зонах. Контуры очагов имели преимущественно нечеткие неровные контуры, за счет инфильтрации вокруг. Нередко фокусы консолидации содержали включения воздуха. Очаги консолидации при саркоидозе отражают слияние множества мелких узелков (рис. 4, 5).
Рис. 4. РК-томограммы пациентки Г., 62 лет. Визуализируются участки альвеолярной инфильтрации округлой формы с неровными, лучистыми контурами (саркоидомы), расположенные перибронхиально
Рис. 5. РК-томограммы пациентки М., 42 лет. Субплеврально и перибронхиально с обеих сторон определяются относительно крупные очаговые тени (саркоидомы)
Картина фиброзных изменений при саркоидозе может достигать различной степени выраженности (от минимальной до грубой деформации легочного рисунка) и формируется постепенно. При хронически текущем саркоидозе, в случаях его позднего выявления, фиброз нередко оказывается первым признаком по данным лучевой визуализации и симулирует силикоз или туберкулёз. При формировании фиброза при саркоидозе часто происходит смещение главных бронхов, образование буллезных «сот», главным образом на периферии, и диффузное распространение линейных теней в легочной ткани (рис. 6).
Рис. 6. РК-томограммы больной Ч., 53 лет. Распространённый пневмофиброз с элементами буллёзной эмфиземы
Довольно часто при саркоидозе в процесс вовлекается плевра, в виде её утолщения от нерезко выраженного до массивного, иногда с элементами обызвествления (рис. 7).
Рис. 7. РК-томограммы пациентки Ф., 59 лет. Определяются участки уплотнения лёгочной ткани субплевральной локализации с вовлечением в процесс костальной и междолевой плевры
Заключение. С внедрением высокоразрешающей КТ в клиническую практику существенно возросли возможности лучевой диагностики в распознавании саркоидоза респираторной системы. Эта технология позволила детально оценить локализацию патологических изменений, распространенность поражения лёгочной ткани, отдифференцировать зоны инфильтрации и диссеминации, визуализировать участки снижения прозрачности легочной ткани по типу «матового стекла», скоплением гранулём в стенках альвеол и периваскулярно, определять состояние внутригрудных лимфатических узлов и бронхиального дерева в целом. Таким образом, КТ-картина патологических изменений в органах дыхания у больных саркоидозом весьма разнообразна и многолика. Выявленные КТ-симптомы позволяют определить стадию и распространенность патологического процесса, выявить осложнения и сопутствующие изменения в органах грудной клетки, а также оценить прогноз заболевания.
Обызвествленные очаги в легких что
На этой странице находиться только текст статьи. Полная статья с картинками и таблицами находится здесь.
Для просмотра требуется программа Adobe Reader.
Дифференциальная диагностика одиночных очагов в легких
И.Е. Тюрин, д.м.н., зав. кафедрой лучевой диагностики, лучевой терапии и медицинской физики РМАПО (Москва)
Одиночный очаг в легких (ООЛ) представляет собой относительно частый рентгенологический синдром. В отечественной и зарубежной литературе термин очаг определяется различно. Такие изменения представляют собой локальный участок уплотнения легочной ткани округлой или близкой к ней формы диаметром до 3 см, окруженный со всех сторон легочной тканью. Это международное определение несколько отличается от традиционного отечественного представления о легочных очагах, источником которого является фтизиатрическая практика. В классификации туберкулеза размеры очагов не превышают 1 см, а все уплотнения большего размера определяются как инфильтраты, туберкулемы и другие виды изменений. Максимальный размер одиночного очага, равный 3 см, соответствует принятой в настоящее время схеме стадирования немелкоклеточного рака легкого, в которой очаги такой величины относят к Т1 стадии опухолевого роста.
Очаги в легочной ткани могут быть одиночными, единичными, в количестве от 2 до 6 включительно, и множественными. Последние относятся к рентгеновскому синдрому диссеминации. Обычно они рассматриваются в контексте дифференциальной диагностики интерстициальных (диффузных паренхиматозных) заболеваний легких. Основной задачей лучевого исследования является неинвазивная дифференциальная диагностика злокачественного и доброкачественного процесса, а также выделение среди них отдельных форм туберкулеза легких. В ряде случаев это возможно на основании характерных симптомов, выявляемых при рентгенографии или рутинной компьютерной томографии (КТ). Тем не менее, специфичность большинства этих признаков низка, поэтому для правильной оценки ООЛ необходимо привлечение дополнительных методических приемов и альтернативных технологий. К ним можно отнести оценку скорости роста очага в легком, анализ вероятностных факторов злокачественности [7], динамика накопления контрастного вещества при КТ и 18фтордеоксиглюкозы (18FFDG) при ПЭТ исследованиях, а также морфологическая оценка изменений по результатам трансторакальной игловой аспирационной биопсии или видеоторакоскопии (ВТС).
Очевидно, что единый алгоритм дифференциальной диагностики, предназначенный для всех пациентов и для всех клинических ситуаций, вряд ли может существовать в клинической практике. Задачей любых клинических рекомендаций является точная оценка возможностей отдельных диагностических методов и их сочетаний.
Выявление
До настоящего времени методом первичного выявления очагов в легочной ткани остается обычное рентгеновское исследование в виде рентгенографии или флюорографии. Одиночные очаги отмечаются в 0,2–1,0% от всех рентгеновских исследований грудной клетки. На обзорных рентгенограммах или флюорограммах редко можно выявить одиночный очаг размером менее 1 см. Даже более крупные очаги могут быть пропущены изза интерпозиции анатомических структур (сердечная тень, корни легких, ребра и др.) или наличия так называемых отвлекающих факторов, например, аномалии развития или патологии сердца.
Все большее значение в диагностике легочных очагов приобретает КТ, которое может быть проведена как в случаях подозрения на наличие ООЛ по данным рентгенографии, так и другим причинам, например, исключение пневмонии, ТЭЛА, оценка больных с ХОБЛ и эмфиземой и т.п. В целом, КТ позволяет выявить в 2–4 раза больше очагов в легочной ткани, чем рентгенография, при этом средний размер выявляемых очагов в два раз меньше. Тем не менее, КТ также не является абсолютным методом диагностики. Результаты скрининга рака легкого с помощью низкодозной КТ показывают, что основными причинами пропуска патологии являются небольшие размеры очагов, низкая плотность очагов по типу матового стекла и их локализация в центральных зонах легкого.
Анатомическая оценка
Оценка скиалогических особенностей одиночного очага по данным рентгенографии или КТ имеет большое значение в дифференциальной диагностике. Очаги можно разделить по размерам, характеру контуров, структуре, плотности, состоянию окружающей легочной ткани. Практически все признаки имеют вероятностное значение. т.е. более или менее характерны для доброкачественного или злокачественного процесса. Лишь в исключительных случаях на основании данных лучевого исследования можно предположить нозологический диагноз. Так, наличие жировых включений типично для гамартомы, кольцевидное или тотальное обызвествление очага обычно наблюдается при туберкулемах, наличие приводящего и отводящего сосуда нарду с типичным усилением при контрастировании отличает артериовенозные мальформации.
Локализация очага в легочной ткани не имеет принципиального значения, так как исключения и совпадения наблюдаются здесь слишком часто. Известно, что более 70% одиночных очагов при периферическом раке легкого расположено в верхних долях легких, причем чаще в правом легком, чем в левом. Эта локализация типична и для большинства туберкулезных инфильтратов. Нижнедолевая локализация характерна для рака легкого, возникающего на фоне идиопатического легочного фиброза. Туберкулезные инфильтраты, расположенные в нижних долях, чаще локализуются в верхушечных их сегментах.
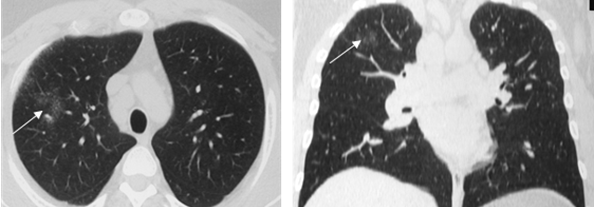
Очаги в легочной ткани могут иметь различные контуры, в том числе ровные или неровные (волнистые, бугристые), а также четкие или нечеткие (лучистые или размытые за счет зоны матового стекла по периферии). В целом нечеткие и неровные контуры более характерные для злокачественных новообразований, хотя могут наблюдаться и при воспалительных инфильтратах. При размерах очага более 1 см такие контуры являются веским аргументом в пользу наличия злокачественно процесса и, следовательно, показанием для морфологической верификации процесса (рис. 1). Четкие ровные контуры могут наблюдаться при доброкачественных заболеваниях, но постоянно наблюдаются при одиночных метастазах, отдельных гистологических формах рака легкого (плоскоклеточный, мелкоклеточный) и легочных карциноидах. Поэтому округлая форма и четкие контуры очага сами по себе не являются признаками доброкачественности процесса и не могут служить причиной завершения процесса дифференциальной диагностики.
Плотность ООЛ, определяемая при КТ, позволяет разделить все очаги на три группы: очаги по типу матового стекла, смешанные или частично солидные очаги, и очаги солидного типа. Очаги по типу матового стекла отличаются низкой плотностью, на их фоне видны стенки бронхов, контуры сосудов и элементы измененного легочного интерстиция. Они наблюдаются при недеструктивных воспалительных процессах, атипичной аденоматозной гиперплазии и при высокодифференцированных аденокарциномах.
Очаги смешанного или частично солидного типа характеризуются наличием более плотного участка в центре и зоны низкой плотности по типу матового стекла по периферии. Такие очаги обычно возникают вокруг старых рубцов в легочной ткани, в том числе и посттуберкулезных. В большинстве случаев они представляют собой разрастание железистой опухоли. Солидные очаги имеют типичную структуру локального уплотнения округлой формы мягкотканой плотности с различными контурами, которая может наблюдаться практически при любом патологическом процессе в легочной ткани.
Структура ООЛ, выявляемая при КТ, может быть различной: однородной, с участками низкой плотности, обусловленными некрозом, с воздушными, жировыми, жидкостными и высокоплотными включениями, с видимыми просветами бронхов. Ни одни из этих симптомов не является специфичным для какоголибо конкретного патологического процесса, за исключением уже упоминавшихся жировых включений при гамартомах. При рентгеновском исследовании удается выявить лишь часть обызвествлений и включения воздуха в виде полостей, воздушных ячеек (син.: сот, пор), наблюдающихся, например, при железистых карциномах, или просветов бронхов.
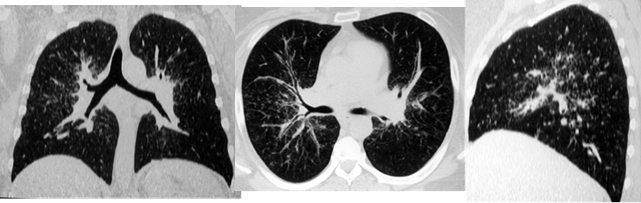
Обызвествления в ООЛ выявляются при КТ в два раза чаще, чем при обычном рентгеновском исследовании (рис. 2). Обызвествления могут быть очаговыми (по типу воздушной кукурузы), слоистыми, в том числе и виде обызвествления капсулы очага, и диффузными, занимающими весь объем очага (рис. 3). Такие обызвествления типичны для доброкачественных процессов. Исключения составляют лишь метастазы костных сарком, метастатические очаги железистого рака толстой кишки и яичников после химиотерапии и легочные карциноиды. Во всех остальных случаях вероятность неопухолевого процесса исключительно велика. В злокачественных очагах, в том числе в железистых карциномах, нередко выявляют точечные или аморфные, без четких контуров, включения кальция. В целом, частота обызвествлений в периферических раковых опухолях по данным КТ достигает 10%, однако в очагах менее 2 см в диаметре этот показатель обычно не превышает 2%. Такие изменения видны только при высокоразрешающей КТ и не являются дифференциальнодиагностическим признаком, так как могут обнаруживаться и в доброкачественных образованиях.
Включения жира обычно наблюдаются при гамартомах (рис. 4). Участки жировой плотности могут выявляться и при первичных липомах, исключительно редких, а также в метастазах липосарком и железистых опухолей почек. При отсутствии внелегочной злокачественной опухоли, наличие жира в легочном очаге является почти патогномоничным признаком гамартомы.
Оценка скорости роста
Сравнение размеров ООЛ на выполненных предшествующих снимках имеет огромное значение в дифференциальной диагностике. Это сравнение может быть проведено по любым изображениям – флюорограммам, рентгенограммам, линейным или компьютерным томограммам. Отсутствие увеличения очага в течение двух и более лет является одним из надежных признаков доброкачественной его природы. Значительная часть очагов в легочной ткани пропускается при любом первичном исследовании изза скиалогических особенностей патологии или психофизиологических факторов восприятия изображения. Поэтому анализ предшествующих снимков является первым и обязательным этапом дифференциальной диагностики любого ООЛ, а наличие архива изображений (например, флюорографического) значительно повышает эффективность лучевого исследования.
Очевидно, что злокачественные опухоли увеличиваются в размерах с большей или меньшей скоростью, что получает отображение на снимках. Время удвоения опухолей колеблется в широких пределах, от 40 до 720 дней. Поэтому появление нового очага в легочной ткани в течение месяца или очаг с неизменными в течение двух и более лет размерами вряд ли представляет собой злокачественную за исключением очагов по типу матового стекла, которые представляют высокодифференцированную аденокарциному. Пациенты с такого рода очагами требуют более длительного наблюдения.
Другим фактором, ограничивающим возможности динамического или ретроспективного наблюдения, являются размеры очага мене 1 см. Удвоение объема опухолевого очага размером 5 мм приводит к увеличению его диаметра на 1.5 мм, до 6,5 мм. Оценка такой динамики находится за пределами возможностей не только традиционной рентгенографии, но и. в большинстве случаев, КТ. В связи этим, большое значение сегодня придается компьютерной оценке объема очагов по данным спиральной КТ, когда ЭВМ строит трехмерные модели выявленных очагов и сравнивает изменение их объема. Эта методика, являющаяся составной частью CAD систем, рассчитана на солидные очаги и не может с уверенностью использоваться для очагов по типу матового стекла и очагов частично солидного типа.
Характеристика очагов при динамической КТ
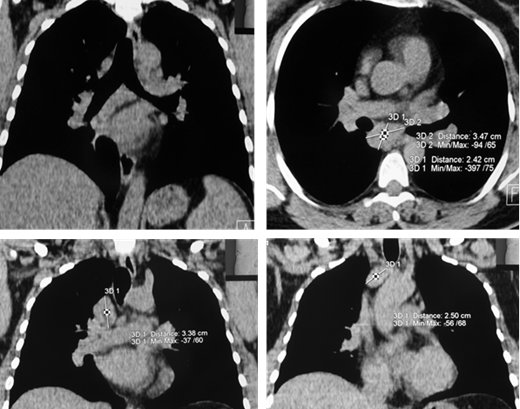
Оценка кровоснабжения ООЛ при динамической КТ показала свою эффективность в многочисленных исследованиях. Известно, что плотность очага в легочной ткани при нативном исследовании колеблется в широких пределах и не имеет какоголибо диагностического значения (кроме включений жира и кальция). Смысл динамической КТ заключается в том, что при внутривенном введении контрастного вещества в виде болюса объемом 100 мл патологические образования, имеющие собственную сосудистую сеть, активно его накапливают, при этом плотность их повышается (рис. 5). Типичным примером таких очагов являются злокачественные опухоли. Наоборот, образования, лишенные собственных сосудов, или заполненные бессосудистым содержимым (гной, казеоз, экссудат и т.п.) не изменяют свою плотность. Такие очаги могут быть представлены туберкулемами, кистами, абсцессами и другими патологическими процессами. Наибольшее значение методика динамической КТ при ООЛ имеет в регионах с высокой заболеваемостью туберкулезом, поскольку позволяет точно разделить злокачественные опухоли от туберкулем.
Динамическая КТ выполняется в виде серии томографических срезов через патологическое образование, которые выполняются до введения контрастного вещества, во время его введения, через 1, 2, 3 и 4 минуты после введения. Для разграничения доброкачественных и злокачественных процессов необходимо выбрать так называемый порог усиления, т.е. числовое значение коэффициента ослабления, превышение которого позволяет предположить наличие злокачественной опухоли. Начиная с 2000 г. таким порогом, определенным эмпирически в крупном многоцентровом исследовании, является 15 HU.
Несмотря на высокую чувствительность в отношении злокачественных опухолей, методика имеет ряд недостатков. К ним относят трудности оценки небольших, менее 1 см, очагов, низкую специфичность, технические ошибки, связанные с дыханием пациента и артефактами от костных структур и контрастного вещества. Эти недостатки частично компенсированы внедрением в клиническую практику многослойной КТ (МСКТ). Кроме того, в большинстве исследований проводиться оценка накопления, но не выведения контраста из очагов.
Метаболическая характеристика ООЛ при 18FФДГ ПЭТ
Все методы анатомической визуализации, включая рентгеновский, ультразвуковой, КТ или МРТ ориентированы на макроскопические признаки легочных очагов, большинство из которых недостаточно специфичны. В последние года все большее распространение получают исследования возможностей метаболических характеристик очага с помощью 18FФДГ ПЭТ. Известно, что злокачественные опухоли отличаются более высокой метаболической активностью, что характеризуется быстрым и значительным накоплением 18FФДГ в очаге и длительным ее сохранением. Многочисленные исследования показали, что метод отличает высокая чувствительность но относительно низкая специфичность в отношении злокачественных очагов в легких. Более высокие результаты получают при сочетанном использовании ПЭТ и КТ сканеров, так называемые ПЭТ/КТ исследования с последующим совмещением метаболической и анатомической картины.
Ложноположительные результаты наблюдаются при активных воспалительных процессах, в том числе при активном туберкулезе легких. Отрицательный результат ПЭТ исследования считается исключительно важным в исключении злокачественной природы легочного очага. Ложно отрицательные заключения могут наблюдаться при первичных опухолях легких по типу матового стекла и при наличии очагов размером менее 7 мм. В этой связи, данные ПЭТ должны обязательно сопоставляться с результатами КТ исследования для более точного понимания их клинического значения. В целом, следует признать, что в настоящее время ПЭТ исследование является наиболее точным методом разграничения доброкачественных и злокачественных очагов в легочной ткани размером более 1 см.
Биопсия
Для очагов, имеющих анатомические или метаболические признаки злокачественности, необходима морфологическая верификация до начала какоголибо лечения. Это правило обязательно, поскольку тактика обследования и лечения в отношении первичной немелкоклеточной, мелкоклеточной и метастатической опухоли в легком может быть различной. Существует несколько методов забора материала из легочного очага, в том числе трансторакальная игловая аспирация и биопсия, трансбронхиальная биопсия, ВТС резекция очага с последующей биопсией, открытая биопсия при торакотомии. Трансторакальная биопсия проводится под контролем рентгеноскопии, КТ, а в последние годы все чаще при КТ флюороскопии. Трансбронхиальная биопсия обычно выполняется под контролем рентгеноскопии. Пункция очагов, прилежащих к грудной стенке, может быть выполнена с помощью ультразвукового наведения.
Транбронхиальная биопсия может выполняться при локализации очага в прикорневых отделах, особенно в случаях, так называемой, централизации злокачественной опухоли. При этом эндобронхиальный компонент может быть выявлен при бронхологическом исследовании. Другим вариантом верификации является браш биопсия, при которой материал забирается с внутренней поверхности бронха, расположенного рядом с очагом или внутри него. Для проведения такой процедуры обязательным является предварительная оценка очага и прилежащих к нему бронхов при высокоразрешающей КТ.
Алгоритмы диагностики
В настоящее время не существует единого подхода к определению характера ООЛ. Очевидно, что для пациентов с высоким риском злокачественной опухоли оптимальным подходом является наиболее ранняя морфологическая верификация при трансторакальной биопсии. Для пациентов с низким риском злокачественного процесса более рациональным является наблюдение и оценка динамики.
В любом случае, современный подход требует выполнения КТ в случаях обнаружения ООЛ при рентгенографии, флюорографии или обычного КТ исследования. Вторым обязательным действием является поиск и изучения любых предшествующих снимков легких. Результатом этих действий может быть выделение группы пациентов с очевидно доброкачественным процессом: отсутствие динамики на протяжении более чем 2 года, наличие «доброкачественных» обызвествлений, включений жира (гамартома), жидкости (киста) в очаге по данным КТ, для которых необходимо только наблюдение. Сюда же относятся выявление АВ мальформации и других сосудистых изменений, случаи воспалительных процессов легких, таких как округлый туберкулезный инфильтрат, туберкулема, мицетома и другие, требующие специфического лечения.
Вторым возможным результатом является выявление признаков злокачественного процесса: очаг более 1 см с лучистыми неровными контурами, очаги по типу матового стекла и смешанного солидного типа, которые должны расцениваться как потенциально злокачественные, и для которых необходима морфологическая верификация в условиях специализированного лечебного учреждения.
Все остальные очаги определяются как промежуточные или неопределенные. Наиболее многочисленную группу среди них составляют впервые выявленные очаги размером более 10 мм мягкотканой плотности, с относительно четкими ровными или волнистыми контурами, без каких либо включений по данным КТ и без предшествующего рентгеновского архива. Уточнение природы очага в легочной ткани у таких пациентов может осуществляться с помощью биопсии, динамической КТ, ПЭТ и ПЭТ/КТ исследования. Выжидательная тактика и проспективное динамическое наблюдение допустимо здесь лишь в исключительных случаях, обоснованных клинической целесообразностью.
Отдельную группу составляют пациенты с выявленными при КТ некальцинированными очагами размером менее 10 мм. Обычно такие очаги обнаруживают при КТ исследовании легких в различных клинических ситуациях, например, исключение пневмонии или ТЭЛА, уточнение характера эмфиземы, трудности интерпретации рентгеновских снимков и т.п. Такие очаги обычно не видны при обычном рентгеновском исследовании, их верификация с помощью трансторакальной биопсии малоэффективна, использование ПЭТ исследования сопряжено с большим количеством ложноотрицательных результатов. Помимо этого, вероятность злокачественного процесса при очагах менее 5 мм не превышает 2%. В связи с этим принята следующая тактика. Очаги размером менее 5 мм не требуют никакого динамического наблюдения. Таким пациентам может быть рекомендовано обычное проверочное исследование (ФЛГ или КТ) через год. Очаги размером 5–10 мм требуют контрольного КТ исследования с интервалом 3, 6, 12 и 24 месяца. В случае отсутствия динамики наблюдение прекращается. Любые изменения формы, размеров, количество очагов является показанием для биопсии.
Таким образом, дифференциальная диагностика ООЛ является сложной клинической задачей, которая в современных условиях решается с помощью различных методов лучевой и инструментальной диагностики.