Влияние нейролептиков на мозг
Сложно разобраться
Изменения мозга при психических и неврологических расстройствах могут быть связаны с нейродегенеративными или нейротоксическими процессами, быть обусловленными пластической адаптации мозга к окружающей среде, нейротоксическими эффектами гипер-дофаминергии и гипер-глутаматергии (феномен эксайтотоксичности), а также окислительным стрессом и воздействием фармакологического лечения, например, нейролептиками.
Интеграция методов
Читатель моего Блога понимает, что разделить перечисленные выше эффекты очень сложно, но все же давайте попытаемся это сделать. Для этого нам стоит объединить результаты структурной и функциональной визуализации мозга, данные нейропсихологических и нейрофизиологических исследований, а также ряд лабораторных показателей, в частности, гормональных и иммунных.
Старые и новые нейролептики
Что показали исследования мозга
Многие исследования не продемонстрировали какой-либо значительной корреляции между прогрессирующими изменениями серого вещества мозга и воздействием антипсихотиков. Не было обнаружено значительной корреляции между лечением SGA детей и подростков с ранним началом шизофрении и изменениями мозга в течение двух лет. Однако, были найдены и прогрессирующие изменения серого вещества мозга (коры) на фоне затяжной терапии нейролептиками. Никто из психиатров не станет отрицать, что при длительном, шаблонном и, отчасти безалаберном лечении нейролептиками развивается токсическая энцефалопатия.
Слишком много и долго — это плохо
Возможны исключения и все неоднозначно?
Что касается новых нейролептиков, то длительный прием Оланзапина в течение пяти лет коррелировал с меньшим снижением объема серого вещества, и даже, возможно, с его незначительным увеличением. Лечение Рисперидоном увеличивало объем серого вещества мозга (GM) в правом и левом хвостатом ядре и левом АСС у пациентов с первым эпизодом психоза (FEP) после трех месяцев лечения. Кора лобной доли мозга была также увеличена у пациентов, принимавших Клозапин на протяжении длительного периода времени. Однако, в этом же исследовании Клозапин и Риспердон также приводили к уменьшению объема белого вещества мозга, то есть волокон связывающих между собой разные структуры мозга. Было отмечено, что длительный прием нейролептиков, особенно в больших дозах приводит к сокращению числа волокон мозга (данные диффузионно-тензорного изображения — DTI).
Влияние нейролептиков на кору мозга
Исследования, изучающие связь между антипсихотиками и изменениями толщины коркового слоя, также показали неоднозначные результаты. Однако, в 2013 г. Goghari et al. продемонстрировали, что краткосрочное лечение (восемь недель) Рисперидоном или Кветиапином увеличивало толщину префронтальной коры головного мозга у 19 пациентов с первым эпизодом психоза, ранее не получавших лекарств. В другом исследовании было отмечено, что «более высокое совокупное потребление классических нейролетиков в течение пятилетнего интервала сканирования было связано с более выраженным истончением кортикального слоя, в то время как более высокое совокупное потребление препаратов SGA (новых антипсихотиков) было связано с менее выраженным истончением кортикального слоя».
Влияние нейролептиков на подкорковые структуры мозга (базальные ганглии)
Некоторые исследования показали увеличение хвостатого ствола во время курса лечения FGA и SGA у молодых пациентов с шизофренией, не принимавших лекарственные препараты. В 1999 году исследователи опубликовали двухлетнее продольное МРТ-исследование пациентов мужского пола (средний возраст 25—57 лет) с диагнозом шизофрении. В течение двухлетнего периода средний объем базальных ганглиев у пациентов, получавших преимущественно классические нейролептики (FGA), увеличился, в то время как обратное наблюдалось у пациентов, получавших в основном атипичные антипсихотики (SGA). В другом исследовании значительное увеличение объема скорлупы было обнаружено в группе больных, лечившихся Рисперидоном. Иными словами, складывается впечатление, что классические нейролептики и некоторые атипичные антипсихотики увеличивают объем базальных ганглиев.
Прогноз
Можно полагать, что если у пациента имеет место увеличение желудочков мозга и уменьшение префронтального объема коры, то это коррелируют с худшим исходом течения болезни, независимо от того, обусловлен ли данный эффект приемом нейролептиков или прогрессирующим течением психического или неврологического расстройства.
Нейролептики (антипсихотики)
Нейролептики — это лекарственные препараты, восстанавливающие дисбаланс дофамина в мезокортикальном, мезолимбическом, нигростриарном и тубероинфундибулярном путях головного мозга, вызывающий психотические состояния. По этой причине препараты данной группы также называют антипсихотиками. Нейролептики воздействуют на дофаминергическую систему таким образом, что устраняют психотическую симптоматику — в первую очередь, обманы восприятия (слуховые, зрительные, тактильные галлюцинации), бред и психомоторное возбуждение.
Лечение нейролептиками назначается при психотических состояниях, возникающих на фоне заболеваний, например: шизофрении, шизоаффективного расстройства, биполярного аффективного расстройства, маний различной этиологии, депрессий, поражений головного мозга (например, ЧМТ, инсульт), неврологических заболеваний (например, эпилепсия, болезнь Паркинсона), деменции. Лечение антипсихотиками, как правило, длительное. В зависимости от заболевания, курс приема нейролептиков может длиться от 3 лет, при наличии хронического заболевания — принимаются пожизненно.
Поколения нейролептиков
Ведущая классификация нейролептиков основана на их химическом строении и терапевтическом механизме действия. Она включает три поколения антипсихотических препаратов:
Типичные нейролептики являются производными химических соединений — тиоксантена, фенотиазина, бутерофенона; атипичные нейролептики — производные 1,4-дибензодиазепина, замещенного бензамида и иного химического строения; нейролептики нового поколения — частичные агонисты дофаминовых рецепторов. Антипсихотики первого поколения быстро и эффективно снимают психотические состояния, но обладают выраженными непрофильными действиями, в отличие от антипсихотиков второго и третьего поколения. Нейролептики нового поколения имеют инновационный от предшествующих поколений механизм действия.
Рис. 1. Поколения нейролептиков.
Нейролептики первого поколения (типичные)
Типичные нейролептики принято делить на три типа по механизму воздействия на рецепторы, обуславливающему антипсихотический эффект, — на слабые, средние и сильные. Слабые антипсихотики имеют низкий аффинитет к дофаминовым рецепторам и высокий к гистаминовым, мускариновым и α-адренергическим. Сильные, напротив, активно связываются с рецепторами дофамина и имеют низкий аффинитет к мускариновым и α-адренергическим рецепторам.
Нейролептики первого поколения отличаются выраженным антипсихотическим эффектом. Впрочем, они могут подходить не всем пациентам по причине отсутствия отклика на лечение (примерно у 3 из 10 пациентов с шизофрений не купируется позитивная симптоматика) или вследствие возникновения побочных эффектов — нарушений сознания, дистонии, тремора конечностей, поздней дискинезии.
Нейролептики второго поколения (атипичные)
Как правило, при назначении лечения нейролептиками отдается предпочтение препаратам второго поколения. Атипичные антипсихотики блокируют дофаминовые рецепторы избирательно, тем самым снижая риск развития экстрапирамидальных расстройств. Помимо этого, в отличие от типичных нейролептиков, они обладают дополнительными терапевтически значимыми положительными эффектами:
Некоторые атипичные антипсихотики снижают суицидальные тенденции в период ремиссии за счет, например, седативного эффекта; другие — позволяют справиться с беспокойством и бессонницей и, напротив, при вялости пациента подбираются нейролептики второго поколения, которые не вызывают сильного седативного эффекта
Нейролептики третьего (нового) поколения
Нейролептики третьего поколения имеют отличный от типичных и атипичных антипсихотиков механизм действия. Механизм препаратов первых поколений заключается в блокировании рецепторов, что, безусловно, помогает эффективно купировать острые и длительно протекающие психотические состояния, проводить поддерживающее лечение. Однако резидуальная симптоматика, индивидуальный профиль побочных эффектов и некоторые трудности в подборе подходящего конкретному пациенту препарата не позволяют им стать эталоном лечения психозов.
Принцип действия нейролептиков нового поколения заключается в частичном агонизме к D2- и D3-дофаминовым рецепторам, которые являются более слабым синтетическим аналогом дофамина. Прием таких препаратов позволяет пациентам редуцировать негативную симптоматику, когнитивные нарушения, неврологические, метаболические, эндокринные и иные нарушения, эффективнее восстанавливать способность к самостоятельной жизни. Иными словами, нейролептики последнего поколения обладают расширенным спектром терапевтической эффективности, улучшенным профилем безопасности и переносимости.
Принцип частичного агонизма антипсихотиков нового поколения является инновационным механизмом, позволившим вывести лечение шизофрении на новый уровень за счет достижения следующих эффектов:
Антипсихотики третьего поколения представлены несколькими препаратами. Первый из них начал применяться с 2002 года (Арипипразол), последующие — с 2015 года (например, Брекспипразол, Карипразин). Естественно, список новейших нейролептиков будет расширяться, но необходимо знать, что Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) обозначает механизм их действия как «неизвестный».
Механизм действия нейролептиков
Терапевтический механизм действия нейролептиков связан с купированием повышенной дофаминовой активности в мезолимбическом пути, одном из дофаминергических нервных путей. Мезолимбический путь связывает черную субстанцию и вентральную область покрышки ГМ со структурами лимбической системы. Этот путь отвечает за процессы в организме, связанные с нейроэндокринной регуляцией, эмоциями, памятью, способностью к обучению и переживанию удовольствия. Помимо этого, данная система частично отвечает за контроль начала двигательных реакций и их аффективных вариаций.
Рис. 2. Механизм действия нейролептиков.
Блокада дофаминовых рецепторов
Повышенный уровень дофамина в мезолимбическом пути становится причиной психотических состояний и продуктивной симптоматики (например, галлюцинаций, бреда, активного проявления тревожных состояний). Типичные нейролептики, снижая активность дофамина посредством блокирования более чем 65% D2-рецепторов, редуцируют позитивную психотическую симптоматику.
Длительная блокада D2-рецепторов в мезолимбических структурах приводит к повышению чувствительности рецепторов или увеличению их количества, попыткам нейронов восстановить межсинаптические связи. В связи с чем возникает гиперчувствительность к дофамину и потенциальная опасность развития психоза даже при незначительном увеличении уровня нейромедиатора. Психоз «гиперчувствительности» (позитивная симптоматика) может быть спровоцирован употреблением алкоголя, табакокурением и иными увеличивающими дофамин веществами, в том числе лекарственными препаратами.
Частичная блокада дофаминовых рецепторов
Некоторые атипичные нейролептики, которые блокируют 2D-дофаминовые рецепторы частично, имитируют нейротрансмиттер в его «ослабленной форме». Таким образом, механизм действия антипсихотиков второго поколения связан с «мягкой» коррекцией уровня дофамина, которая способствует умеренной редукции позитивных симптомов и снижает риски возникновения непрофильных эффектов.
Лечение нейролептиками второго поколения снижается риск возникновения ангедонии, гиперпролактинемии, психозов гиперчувствительности, поздней дискинезии и экстрапирамидных расстройств. Однако препараты все же не лишены побочных эффектов, в частности, при их приеме сохраняется норадреналиновая активность в черной субстанции, способная вызвать развитие акатизии (внутреннее беспокойство, стремление к двигательной активности) при длительном приеме.
Блокада серотониновых 5-НТ2А-, 5-НТ1А-, 5-НТ2С-рецепторов
Механизм действия другой группы атипичных нейролептиков связан со способностью связываться с серотониновыми 5-НТ2А-рецепторам, опосредовано воздействуя на уровень дофамина. 5-НТ2А-рецепторы связывают серотониновую и дофаминовую систему, а их блокировка приводит к снижению активности дофаминового нейрона напрямую и опосредовано, за счет снижения выброса ГАМК.
При повышении уровня серотонина 5-HТ1А-рецепторы, отвечающие за саморегуляцию серотонинового нейрона, тормозят свою активность. Посредство этого прекращается воздействие серотонина на 5-НТ2А-рецепторы и снижается активность дофаминового нейрона. Аналогичного, но «мягкого» эффекта, можно добиться за счет агониста, имитирующего воздействие серотонина на 5-HТ1А-рецепторы.
Некоторые антипсихотики второго поколения блокируют серотониновые 5-НТ2С-рецепторы, увеличивая уровень дофамина и снижая серотонин. Возникающие при этом процессы в промежуточных ГАМК-нейронах позволяют снизить выработку дофамина. По такому же принципу работают препараты, воздействующие на α2-адренорецепторы (аналоги 5-HТ1А-рецепторов). Их блокада антипсихотиком приводит к выбросу норадреналина, угнетая его обратный захват и, соответственно, повышая его активность.
Мультирецепторная блокада
Нейролептики третьего поколения обладают свойством мультирецепторной блокады, воздействуя на дофаминовую, серотониновую, холинергическую, адренергическую и иные системы, связанные с возникновением психотических состояний. Они обладают расширенным профилем терапевтического эффекта, купируя позитивную симптоматику и редуцируя негативную; непрофильные эффекты в клинической практике возникают крайне редко.
Побочные действия нейролептиков
При лечении антипсихотиками может возникнуть нейролептический синдром. Экстрапирамидные расстройства синдрома выражаются в гипо- или гиперкинетических нарушениях. Первые характеризуются снижение двигательной активности, скованностью мышечного скелета, тремором конечностей, проблемами с удержанием равновесия; вторые — тремором, непроизвольно возникающими движениями, подергиванием мышц, спазмами жевательной мускулатуры, скованностью движений, замедленной речью, двигательной активностью. Обычно нейролептический синдром включает как гипо-, так и гиперкинетические нарушения.
Рис. 3. Побочные действия нейролептиков.
При нейролептическом синдроме спазмы мышц носят приступообразный характер. Обычно они затрагивают лицевую и мускулатуру шеи — сокращаются мышцы губ, языка, челюстей, глаз, глотки, горла. В некоторых случаях появляются вегетативные нарушения, вплоть до возникновения обморочных состояний.
Беспокойство, двигательная активность
Помимо экстрапирамидных расстройств, на фоне приема нейролептиков могут возникать явления акатизии:
Поздняя дискинезия
Если лечение нейролептиками проводится достаточно долго (от 2 лет), возникает риск развития поздней дискинезии. Она выражается в непроизвольных движениях губ, языка, мимики, конечностей, которые не поддаются контролю.
Расстройства вегетативной нервной системы
Нарушения со стороны вегетативной нервной системы могут проявляться в постуральной гипотензии (падение артериального давления во время принятия вертикального положения), дизурических расстройствах (болезненное, затрудненное мочеиспускание), расстройствах ЖКТ (поносы, запоры), повышенной потливости, увеличении массы тела, ухудшении зрения, нарушениях работы сердечно-сосудистой системы.
У женщин может развиться дисменорея (при повышении пролактина в крови), нарушиться цикл, возникнуть проявления псевдогермафродитизма; у мужчин — гинекомастия, снижение либидо, задержка эякуляции, галакторея (выделение молока из молочных желез), гирсутизм (избыточный рост волос). В редких случаях появляется повышенная чувствительность кожных покровов к солнечному свету и ультрафиолетовым лучам, дерматиты, пигментация и аллергические реакции.
Тяжелые осложнения нейролептической терапии
В случаях, когда пациент не наблюдается у лечащего врача (не делает контрольных визитов, не уведомляет доктора об изменениях состояния здоровья, вызывающих тревогу и опасения, не следует рекомендациям по контрольно-диагностическим мероприятиям) имеется риск развития тяжелых осложнений нейролептической терапии, например:
Помимо этого, при лечении антипсихотиками существует риск развития психических расстройств (например, депрессии астенического типа), тяжелых нарушений сна, делирия (в категорию риска попадают пациенты с органической патологией ЦНС, пожилые люди, дети), эпилептиформных припадков.
Список препаратов нейролептиков
В зависимости от случая (интенсивности проявления той или иной психотической симптоматики; особенностей течения заболевания), состояния здоровья, противопоказаний и иных важных с точки зрения терапии факторов, подбираются нейролептические препараты. Их дозировки корректируются в процессе лечения, нередко происходит смена препарата, назначается симптоматическая терапия.
Нейролептики первого поколения
Среди типичных антипсихотиков, применяемых с целью быстрого купирования острых состояний, наиболее известными являются:
Нейролептики второго поколения
Атипичные антипсихотики по причине улучшенного профиля действия применяются в качестве основной терапии при заболеваниях с психотической симптоматикой. В клинической практике наиболее широкое применение получили следующие нейролептики:
Нейролептики третьего поколения
К самым известным новейшим антипсихотикам, обладающим инновационным механизмом действия, относятся:
Перспективные разработки
В настоящее время разрабатываются антипсихотические препараты, которые не блокируют D2-рецепторы. Среди мишеней таких препаратов — метаботропные глутаматные рецепторы. Другие новейшие нейролептические препараты, также находящиеся в стадии испытаний, воздействуют на нейропептидную, ГАМКергическую, холинергическую и серотонинергическую рецепторные структуры. Все они демонстрируют эффективность в клинических испытаниях, однако их выход на рынок все еще остается вопросом времени.
Список использованной литературы
1. Джонс П.Б., Бакли П.Ф. «Шизофрения. Клиническое руководство».
2. Смулевич А.Б. «Лечение вялотекущей шизофрении».
3. Снедков Е.В. «Атипичные антипсихотики: поиск решения старых и новых проблем».
4. Краснов В.Н., Гурович И.Я., Мосолов С.Н., Шмуклер А.Б. «Стандарты оказания помощи больным шизофренией».
5. Иванов С.В., Смулевич А.Б., Воронова Е.И. «Антипсихотик нового поколения карипразин в лечении шизофрении: спектр клинической эффективности и безопасности».
6. Geddes J., Freemantle N., Harrison P., Bebbington P. «Atypical antipsychotics in the treatment of schizophrenia: systematic overview and meta-regression analysis».
7. Jindal R.D., Keshavan M.S. «Classifying antipsychotic agents. Need for new terminology».
8. Correll C.U., Rubio J.M., Inczedy-Farkas G. «Efficacy of 42 pharmacologic cotreatment strategies added to antipsychotic monotherapy in schizophrenia».
9. Wang S.M., Han C., Lee S.J. «Investigational dopamine antagonists for the treatment of schizophrenia».
10. К.С. Раевский. «Современные нейролептики: взаимодействие с системами нейротрансмиттеров мозга».
Как генетика и пол влияют на эффект нейролептиков
Как генетика и пол влияют на эффект нейролептиков
Авторы
Редакторы
Статья на конкурс «Био/Мол/Текст»: В этой статье мы попытались разобраться в том, почему лекарства работают по-разному у мужчин и женщин, и в том, что, с точки зрения фармакогенетики, может помешать эффективно лечить шизофрению нейролептиками.
Конкурс «Био/Мол/Текст»-2020/2021
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2020/2021.
Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.

Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.
Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Введение
Известно, что на фармакокинетику и фармакодинамику лекарственных препаратов влияет множество факторов. Это не только возраст, различные заболевания, вредные привычки, образ жизни пациента, но пол и мутации в генах. Генетические вариации, чаще всего представленные однонуклеотидными полиморфизмами (ОНП), по последним данным [1], определяют до 50% побочных эффектов от лекарственных препаратов и резистентности к ним у пациентов с шизофренией. В свою очередь гены, в которых находятся ОНП, кодируют определенные белки, участвующие в процессах метаболизма — превращения — лекарственных средств в организме. Найденные ОНП не имеют привязки к полу, но все-таки, как оказалось, именно он существенно влияет и на проявление, и на течение болезни, и на восприятие лекарств организмом пациента.
Женщины и мужчины хоть и болеют одними и теми же заболеваниям, но переносят их по-разному. И речь здесь идет даже не о частоте распространенности или склонности к заболеванию среди представителей определенного пола, а именно о тяжести их течения и разной эффективности лекарств у мужчин и женщин. Например, женщины тяжелее переносят болезни суставов (спондилоартрит) [15], а смертность и осложнения от сердечно-сосудистых заболеваний выше у мужчин [16]. Известно, что люди испытывают дискомфорт и страдания из-за заболевания, ограничивающего их жизнь. Однако есть и другие, которые вносят изменения, преобразующие жизнь, включая исцеление в психологической, социальной и духовной сферах, независимо от исхода болезни. Необходимо отметить, что в психофармакологии именно конечный результат — социальная адаптация пациента — очень сильно зависит от эффективности и безопасности препаратов. Ведь именно в этой сфере представлен широчайший спектр лекарственных препаратов с разнообразными и далеко не всегда до конца выясненными механизмами действия, способными вызвать массу побочных эффектов в связи с влиянием на центральную нервную систему. К данной категории относятся и нейролептики, которые до сих пор подвергаются тщательному изучению.
Словарь терминов
(При написании определений была использована PharmGKB).
Различные аллельные варианты гена могут существенно влиять на кодируемые ими белки и, далее, на фармакологический ответ. Сюда относятся: ферменты биотрансформации, транспортеры, молекулы-мишени, белки, которые сопряжены с молекулами-мишенями. Действие этих белков в совокупности формирует ответ на лечение. ОНП представляют собой либо замену, либо вставку, либо выпадение одного нуклеотида. Именно ОНП отвечают за изменение фармакологического ответа на лекарство в целом. Здесь возможны разные варианты развития фармакологического ответа: либо лекарство слишком мощно воздействует на пациента, что приводит к большей степени выраженности побочных эффектов, либо пациент склонен к развитию резистентности, то есть не восприимчив к действию данного лекарства, или же у пациента все параметры находятся в пределах обозначенной нормы. В первом случае врачи стараются подбирать лекарство с наименьшим спектром побочных эффектов или же значительно снижают дозировку. Во втором случае анализируют, к каким конкретно препаратам у пациента возможно развитие резистентности. И в третьем случае врачи просто подбирают препарат и прописывают дозировку по стандарту [1].
Основные генетические маркеры, связанные с изменением метаболизма нейролептиков
Метаболизм лекарств осуществляется в печени, в большей степени — различными подсемействами цитохрома Р450. Самыми важными являются: CYP2D6, CYP2C19, CYP2C9, CYP1A2, CYP3A4.
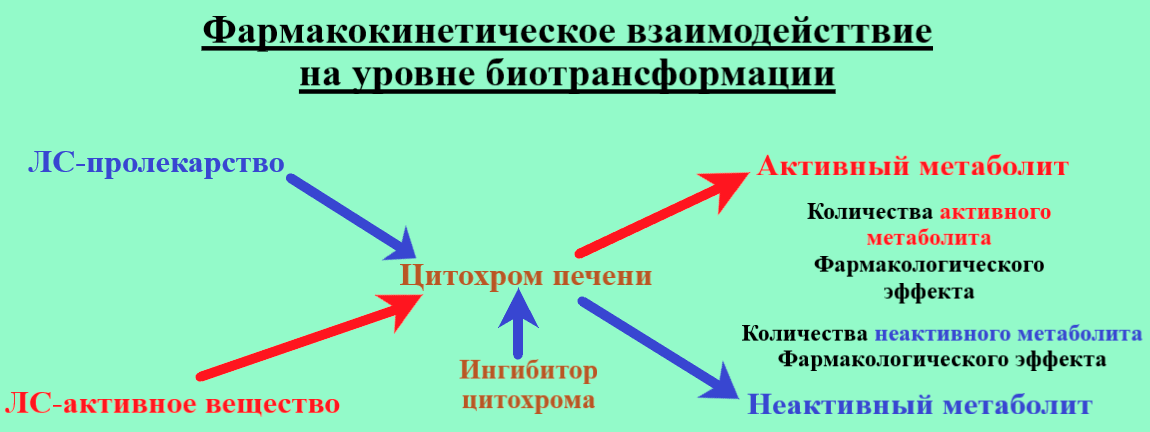
Рисунок 1. Фармакокинетическое взаимодействие на уровне биотрансформации
В транспорте многих лекарств участвует, в том числе и Р-гликопротеин, который кодируется геном MDR1. Этот транспортер помогает лекарствам проникать через гематоэнцефалический барьер — барьер между центральной нервной системой и кровеносной системой, — что очень важно, например, для нейролептиков и в целом для препаратов, применяемых в психиатрии.
Рассмотрим маркеры, которые в большей степени влияют на метаболизм и транспорт нейролептиков. [1]
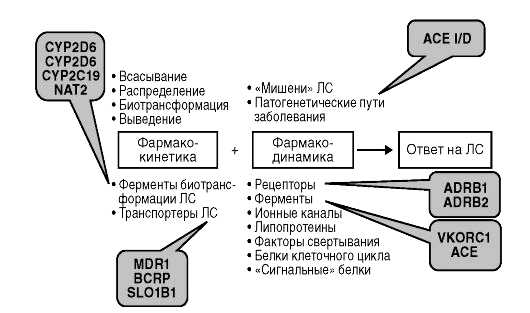
Рисунок 2. Модификации генов, которые влияют на действие и метаболизм лекарств
CYP2D6
CYP1A2
CYP3A4
Гены системы серотонина
Генетические особенности серотониновой системы тоже оказывают свое влияние на фармакологический ответ при приеме нейролептиков, а также на течение самого психического заболевания.
Так, если пациенты гомозиготны по 102-му положению гена 5-НТ2А, то подвержены более тяжелому течению шизофрении, большим количествам госпитализаций в клинику. Также отмечено, что такие пациенты более чувствительны к действию нейролептика рисперидона. Это должны взять во внимание лечащие врачи, поскольку такие пациенты считаются одними из самых тяжелых [12].
Фармакогенетическое тестирование
Для того чтобы обнаружить аллельные варианты генов, рассмотренных выше, необходимо провести фармакогенетическое тестирование, которое проводится только с согласия пациента или его представителя. Перед этим врач-психиатр подробно рассказывает о том, что такое фармакогенетическое тестирование, зачем и как оно проводится, для чего необходимо и что дадут результаты этого теста. В качестве биологического материала могут выступать кровь, слюна, соскоб буккального эпителия. Тестирование проводится в несколько этапов:
После получения результатов составляется подробный отчет, в который обязательно входит перечень и объяснение найденных аллельных вариантов, какие лекарственные препараты подходят пациенту, а какие — не нужно применять [1].
Половые особенности
Как уже упоминалось выше, не только аллельные варианты генов могут влиять на процессы фармакокинетики и фармакодинамики лекарств, но также огромный вклад вносят половые особенности [17]. Дело в том, что шизофрения протекает у мужчин и женщин по-разному (рис. 3). Если говорить о риске ее развития, то мужчины/женщины находятся в соотношении 1,4:1 [17]. Выделим некоторые яркие особенности, которые по отдельности присущи женщинам и мужчинам [17].
На рисунке 3 мы видим различия течения шизофрении у женщин и мужчин. Также видим, что для женщин при лечении шизофрении больше подходят типичные нейролептики (например аминазин и галоперидол), а для мужчин атипичные нейролептики (например оланзапин и клозапин). Таким образом, можно сделать вывод, что пол имеет большое значение при течении такого психического заболевания, как шизофрения. Это учитывается врачами-психиатрами при назначении нейролептиков.
Рисунок 3. Половые особенности при развитии шизофрении
Заключение
Как мы видим, такие характеристики, как генетические особенности и пол пациента, очень важны при назначении нейролептиков, ведь они влияют на метаболические процессы внутри организма и на течение психических заболеваний (рис. 4). Не раз было показано, что даже непсихотропные препараты, применяемые для лечения пациентов с шизофренией, могут существенно повлиять на качество их жизни и вернуть в социальную среду [18]. Получение новых знаний об особенностях организма пациента поможет врачам бороться с такими проблемами, как внезапные, непредсказуемые и тяжелые нежелательные реакции на препараты или отсутствие эффекта от лекарств. Это, в свою очередь, улучшает качество медицинской помощи пациентам и дает надежду на скорейшее их выздоровление.
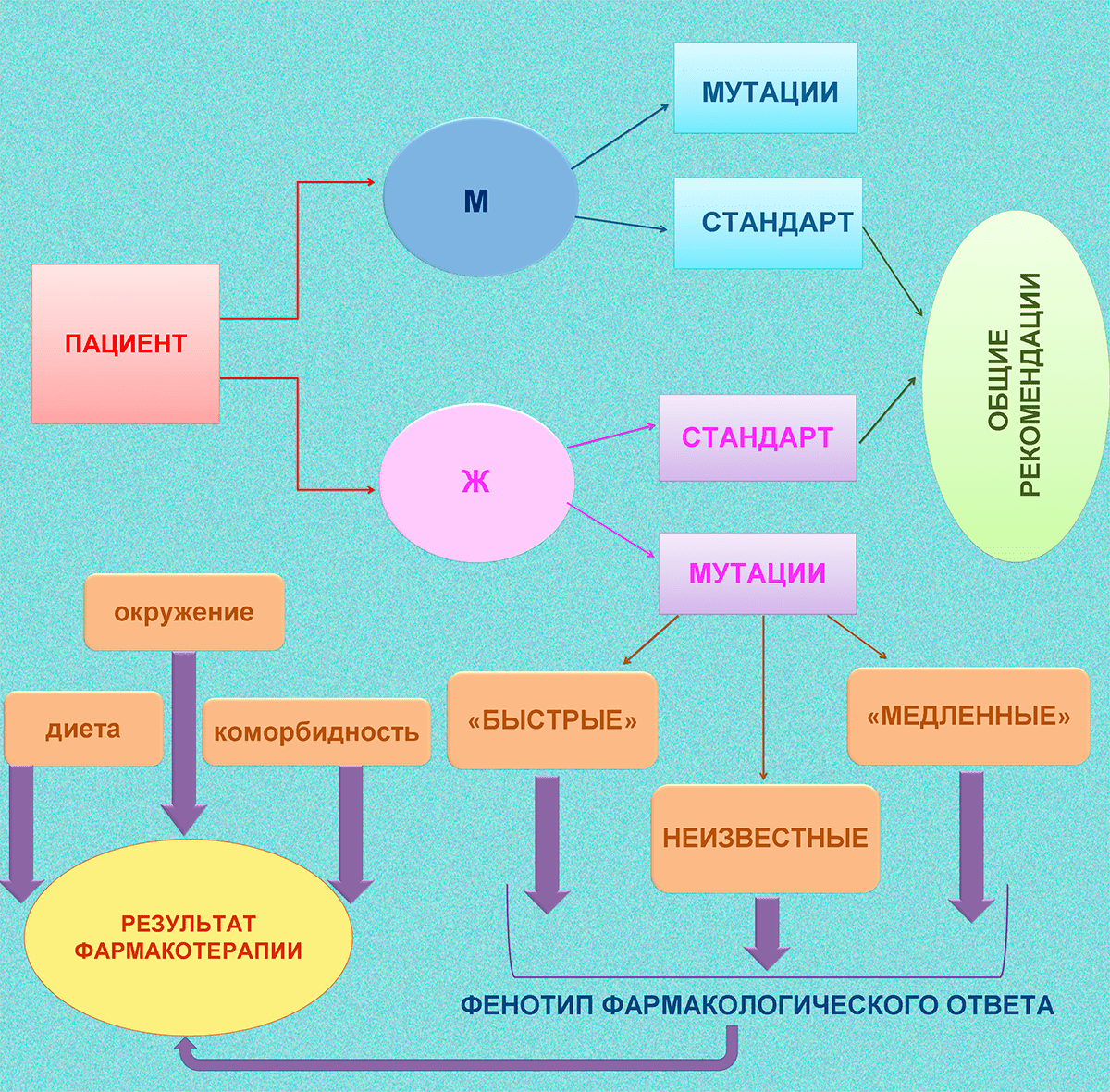
Рисунок 4. Общая схема влияния генетики и пола на фармакологический ответ. Эта информация необходима врачам-психиатрам при составлении плана лечения для пациентов с психическими заболеваниями, а именно шизофренией.