Научная электронная библиотека
1.2. Коллаген
Коллагены составляют основу структуры кожи, костей, хрящей, сухожилий, кровеносных сосудов и играют важную роль в сохранении нормальной структуры и функции соединительной ткани всех животных (Слуцкий, 1969, 1985; Риггз, Мелтон, 2000; Руденская, 2003).
Коллаген (К) – нерастворимый фибриллярный белок, первичная структура которого складывается из повторяющихся последовательностей триплетов аминокислот глицин-X-Y, где X и Y позиции чаще заняты, соответственно, пролином и гидроксипролином. Эти повторяющиеся последовательности позволяют трем коллагеновым полипептидам (называемым α-цепями) формировать полужесткие, очень стабильные трехспиральные молекулы (рис. 3). Они могут быть гомополимерными (три идентичные α-цепи) и гетерополимерными (две или три разные α-цепи). Под влиянием регулярно располагающихся остатков пролина и оксипролина цепь принимает форму ломаной спирали; это обусловливается жесткостью боковых групп пролина, а также тем обстоятельством, что пептидные связи, в образовании которых участвуют пролин и оксипролин, не могут образовать водородных связей. Остатки глицина образуют межцепочечные водородные связи, способствующие сохранению прочности структуры коллагена.


Рис. 3. Структура коллагена: а – электронная микрофотография коллагена соединительной ткани. Расстояние между повторяющимися структурными единицами равно 700 Å; б – конформация полипептидных цепей в трёхцепочечной молекуле тропоколлагена; в – ступенчатое расположение молекул тропоколлагена обусловливает появление в гидратированных волокнах коллагена повторяющихся структурных единиц, расстояние между которыми равно 700 Å (по Мусил и др., 1984)
Аминокислотные цепи коллагена обернуты друг вокруг друга и образуют «трехволоконный канат», где отдельные волокна связаны между собой водородными связями. Такая пространственная структура возможна, только если аминокислотная последовательность строго соблюдается.
В результате образуется трехволоконная фибриллярная молекула – тропоколлаген, обладающая большой прочностью на растяжение. Это название происходит от слова тропос – обращенный внутрь – из-за того, что коллагеновые волокна всех соединительных тканей, выстланы тропоколлагеновыми молекулами, соединенными «конец в конец» и «бок о бок» – в шахматном порядке. Гидроксильные группы некоторых остатков лизина и оксилизина участвуют в образовании связи между соседними молекулами тропоколлагена. Таким образом, формируется жесткое нерастяжимое волокно. Фибробласты синтезируют молекулы тропоколлагена и выбрасывают их в матрикс, и только здесь происходит сборка коллагеновых волокон (рис. 4).
Коллагены кожи содержат в больших концентрациях пролин и оксипролин (около 20 % от всех остальных аминокислот), глицин и аланин (свыше 50 % от содержания других аминокислотных остатков), ароматические и серосодержащие аминокислоты практически отсутствуют или содержатся в весьма малых количествах. Кроме того, коллаген является одним из немногих белков, содержащих оксипролин и оксилизин. Оксипролин и оксилизин образуются в молекуле проколлагена не в результате биосинтеза, а при гидроксилировании пролина и лизина, которое начинается в период трансляции коллагеновой мРНК на рибосомах (Неклюдов, 2003).
Рис. 4. Строение фибробласта и основные этапы синтеза коллагена. Г – аппарат Гольджи; Я – ядро; ШЭР – шероховатый эндоплазматический ретикулум; СП –секреторный пузырек; ТК – тропоколлаген; КВ – коллагеновое волокно
В настоящее время идентифицировано более 25 различных α-цепей, из которых формируется до 14 разных типов коллагеновых молекул, некоторые из них являются тканеспецифичными (Ленинджер, 1974; Риггз, Мелтон, 2000).
Таким образом, коллагены – это белки, которые:
б) могут состоять из трех цепей с повторяющимися последовательностями, обладающими способностью к сворачиванию в характерную тройную спираль. По меньшей мере, 19 белков определены в настоящее время как принадлежащие к коллагенам. 10 родственных им белков содержат коллагеноподобные домены.
Коллагеновые белки составляют около половины массы сухого вещества суставного хряща; вблизи суставной поверхности их концентрация приближается к 90 %. В других видах хрящевой ткани коллагены количественно преобладают над другими белками, обеспечивая прочность на растяжение и разрыв. (Слуцкий, 1985). Количественно преобладающим белком протеогликанового комплекса хрящевой ткани является коллаген второго типа (КII). Он в незначительных количествах обнаружен в других специализированных тканях, например, в стекловидном теле глаз некоторых видов животных. Хрящевой ткани присущ необычный полиморфизм коллагеновых компонентов, проявляющийся присутствием большого числа минорных коллагенов. Молекулярная формула КII хрящевой ткани имеет следующий вид: [α1(ΙΙ)]3, что означает наличие трех идентичных α1(II)-цепей, которые отличаются от α1(I)-цепей более высоким содержанием оксилизина. Столь высокая концентрация оксилизина способствует увеличению количества связанных с ним углеводов. По-видимому, такая структура обеспечивает большую сольватную оболочку коллагена типа II по сравнению с типами I или III. В процессе биосинтеза коллагена С-пропептиды соединяются между собой бисульфидными мостиками и после отщепления от молекулы образуют белок, который называется хондрокальцин, с м.м. около 100 000 Да (Слуцкий, 1985).
Коллаген одиннадцатого типа (КXI) составляет приблизительно 3 % хрящевого коллагена и образован двумя разными типами цепей (формула молекулы α1(XI)2 α2(XI)). Со старением организма его количество в хряще уменьшается в пользу коллагена пятого типа (КV) (Канунго, 1982; Риггз и Мелтон, 2000).
Для хрящевой ткани характерно наличие наибольшего количества минорных коллагеновых компонентов. Такой полиморфизм коллагенов позволяет считать минорные компоненты регуляторами адаптационной пластичности хряща, метаболизма хондроцитов и морфогенетических процессов (Слуцкий, 1985).
Содержание коллагена в различных тканях и органах сельскохозяйственных животных (КРС, свиньи) характеризуют следующие данные (% от массы сухого вещества): дерма – 80–90; ахиллово сухожилие – 86; костная ткань – 17,5–25; хрящи – 46–67; роговица и склера глаз – 70; мышцы – 10. При этом коллаген составляет от 25 до 33 % от общего количества белка (Титов, Апраксина, 1995). У костистых рыб коллагеновые белки преобладают в коже, сухожилиях, плавательном пузыре; у кольчатых червей и иглокожих в кожно-мускульном мешке; у моллюсков в кожных покровах и опорных хрящевых элементах.
Наиболее изучены свойства коллагенов в коже и мышечной ткани рыб. Коллаген кожи костистых рыб характеризуется частой встречаемостью молекул, состоящих из трех генетически различающихся α-цепочек, гетеротримера α1 α2 α3; среди изученных позвоночных животных цепочка α3 отмечена лишь у костистых рыб. В целом коллагены мышечной ткани костистых рыб, полученные методом электрофореза, идентичны соответствующим коллагенам типа I из кожи и имеют сходный аминокислотный состав. Однако коллагены мышечной ткани рыб более устойчивы к тепловой денатурации (более 100 °С), чем коллагены кожи, что объясняется более высокой степенью гидроксилирования пролина в мышечном коллагене. Термальная устойчивость мышечного коллагена определяется видом рыбы и по мере ее возрастания рыб можно расположить в следующем порядке: карп, угорь, скумбрия, сайра, кета.
В табл. 1 приведены данные о содержании коллагена и гексозаминов в соединительных тканях различных видов животных.
Составы субъячеек коллагена I типа из мышечной ткани и кожи являются идентичными у угря, скумбрии, сайры и карпа и отличаются у кеты. У последней коллаген кожи состоит из α1 α2 α3 гетеротримеров, а основная часть мышечного коллагена – из (α1)2α2 гетеротримеров (Богданов, Сафронова, 1993).
Содержание гексозаминов и коллагена в соединительной ткани животных
Чем различаются коллагены разных типов
• Основная функция коллагена состоит в обеспечении структурной опоры тканей
• Коллагены представляют собой семейство, состоящее более чем из 20 различных белков внеклеточного матрикса. Эти белки — наиболее распространенные в царстве животных
• Все коллагены организованы в тройные спирализованные «коллагеновые субъединицы», обладающие суперспиральной структурой и состоящие из трех отдельных полипептидов
• Коллагеновые субъединицы выходят из клеток и затем, во внеклеточном пространстве, собираются в более крупные фибриллы и волокна
• Мутации в коллагеновых генах вызывают множество патологических состояний, начиная от появления морщин до развития хрупкости костей и таких тяжелых заболеваний, как образование кожных волдырей
Семейство коллагенов включает более 20 белков, которые относятся к наиболее распространенным белкам клеток животных. У многоклеточных организмов коллагены существуют по крайней мере 500 млн лет. Почти все клетки животных синтезируют и секретируют по меньшей мере одну из форм коллагена.
Коллагены обеспечивают тканям структурную поддержку и существуют во множественных формах, организованных в различные структуры. Все белки семейства коллагенов характеризуются одним общим свойством: они собраны в тонкие (примерно 1,5 нм диаметром) тройные спиральные суперспирализованные структуры, состоящие из трех субъединиц коллагеновых белков, которые удерживаются вместе ковалентными и нековалентными связями.
где они связаны между собой другими белками внеклеточного матрикса, включая коллагены, связанные с фибриллами.
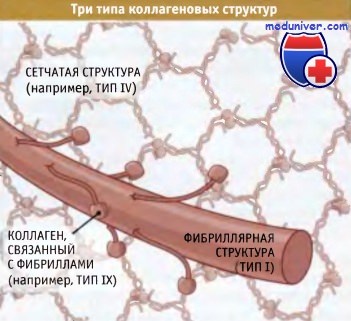
Суперспирализованные структуры бывают трех типов — фибриллярные, слоистые и связанные с фибринами:
• В фибриллярных коллагенах суперспирализованные спирали организованы в фибриллы или «канаты», которые обеспечивают прочность структуры вдоль единственнной оси (такая структура напоминает прочный стальной трос, образованный проволочными пучками). Когда эти фибриллы собраны в параллельно расположенные пучки, как в сухожилиях, они обеспечивают невероятную прочность структуры, которая способна противостоять усилиям, развиваемым мышцами, закрепленными на костях.
• Слоистые коллагены представляют собой сеть, состоящую из суперспирализованных спиральных структур. Они в меньшей степени устойчивы к мышечным усилиям, но гораздо лучше противостоят растяжению в нескольких направлениях. Сеть таких структур, например, характерна для кожи.
• Третий тип коллагена, известный как «фибриллярные связки», образует суперспирализованные спиральные структуры, связывающие коллагеновые фибриллы вместе.
Независимо от организации, коллагены образуют основную каркасную структуру внеклеточного матрикса. Такие входящие во внеклеточный матрикс белки, как фибронектин и витронектин, связываются с коллагенами и вплетены в структуры, образованные коллагеновым каркасом. Один из представителей семейства коллагенов представляет собой трансмембранный белок, который участвует в формировании межклеточных контактов.
Существует примерно 20 различных типов коллагена, большая часть которых может быть сгруппирована в четыре класса. Каждая из тройных спиралеобразных структур обозначается римской цифрой (I, II, III и т. д.). Каждая коллагеновая субъединица имеет обозначение как субъединица а, а ее типу присвоен номер (а1, а2, а3 и т. д.), после которого римской цифрой обозначен тип, в котором она находится. Например, основной фибриллярный коллаген хвоста (и других тканей) крыс относится к типу I и состоит из двух копий субъединиц а1(1) и одной копии субъединицы а2 (I).
На рисунке ниже представлена структура коллагеновых волокон. Три полипептидные субъединицы параллельно обернуты вокруг друг друга и образуют суперспирализованную спиральную структуру длиной 300 нм. Для коллагенов характерна повторяющаяся последовательность аминокислот, содержащая элемент глицин-X-Y, где X и Y могут представлять собой любую аминокислоту, но обычно это пролин и гидроксипролин соответственно.
Такая последовательность способствует плотной упаковке трех субъединиц и облегчает образование суперспиральной структуры. Субъединицы длиной 300 нм скрепляются вместе посредством ковалентных связей, которые образуются между N-концевым участком одной субъединицы и С-концевым участком примыкающей к ней. Суперспирализованные спиральные структуры располагаются параллельно, образуя между собой небольшие зазоры (64-67 нм). Эти зазоры обеспечивают характерный вид (исчерченность) фибрилл, видимый в электронном микроскопе.

характеру полимерных форм и по распределению в тканях. Некоторые группы включают коллагены нескольких типов.
Полностью собранные коллагеновые структуры (фибриллярные или сетчатые) по размерам оказываются гораздо больше, чем сами клетки; некоторые фибриллы могут достигать нескольких миллиметров длины. Таким образом, субъединицы коллагена синтезируются и секретируются в виде суперспирализованных спиральных структур, и окончательные этапы их сборки происходят вне клетки. Как показано на рисунке ниже, синтез коллагена и дальнейший его процессинг происходят на протяжении всего секреторного пути. При синтезе коллагеновые белки направляются в гранулярный эндоплазматический ретикулум (ЭПР) при участии частиц, распознающих сигнал и связанного с ними белкового аппарата.
Коллагеновые субъединицы синтезируются в виде крайне длинных полипептидов, которые называются проколлагены и содержат пропептиды, представляющие собой «хвосты», расположенные на амино- и карбоксильном концах.
После того как проколлагены попали в просвет ЭР, по мере транспорта из ЭР через аппарат Гольджи и в секреторные везикулы, они претерпевают серию модификаций. В процессе транспорта проколлагена через ЭР и аппарат Гольджи, к боковым цепям пролина и лизина, находящимся в средней части молекул проколлагена, добавляются гидроксильные группы (-ОН). При этом образуются гидроксипролин и гидроксилизин.
Эти модификации обеспечивают правильное образование водородных связей, которые скрепляют вместе три субъединицы в суперспирализованной спиральной структуре. Между амино- и карбоксиконцевыми частями пропептидов образуются дисульфидные связи, которые затем обеспечивают правильное расположение трех проколлагеновых субъединиц с образованием тройной спиральной суперспирализованной структуры. Затем спираль образуется спонтанно, в направлении от С-конца к N-концу.
Пропептиды препятствуют взаимодействию суперспирализованных спиралей друг с другом, тем самым предотвращая полимеризацию коллагена в клетке. Когда произошла секреция тройных спиралей проколлагена, ферменты, которые называются протеазы проколлагена, отщепляют пропептиды. Остающийся белок, известный под названием тропоколлагена, почти весь организован в тройную спираль и представляет собой основную структурную единицу коллагеновой фибриллы.
Фибриллы собираются просто: боковые цепи лизина в тропоколлагене модифицируются при действии фермента лизилоксидазы, образуя аллизины. Эти модифицированные лизины образуют ковалентные сшивки, которые обеспечивают полимеризацию тропоколлагенов. Лизилоксидаза представляет собой внеклеточный фермент, и эта стадия сборки фибрилл происходит только после выхода проколлагена из клетки. После сборки фибриллы могут объединяться, образуя большие пучки или волокна, характерные для фибриллярного коллагена.
Принимая во внимание всю важность коллагена в обеспечении структурной поддержки тканей, можно представить, какие тяжелые последствия для организма будет иметь нарушение процесса сборки фибрилл. Мутации в генах, кодирующих синтез коллагенов или ферментов, модифицирующих проколлаген, вызывают развитие множества генетических заболеваний, затрагивающих практически все ткани. Например, коллаген типа I представляет собой основной структурный белок костной ткани. Мутации в коллагеновых генах этого типа служат причиной незавершения остеогенеза, т. н. развития «болезни хрупких костей».
Мутации в коллагеновом гене типа IV приводят к нарушению сборки базальной ламины в большинстве эпителиальных тканей и к развитию такого кожного заболевания, как буллезный эпидермоз.
Клетки связываются с коллагеном посредством специфических рецепторов, называемых интегринами. Эти рецепторы обеспечивают возможность обратимого связывания клеток с коллагенами по мере их движения по внеклеточному матриксу. Интегриновые рецепторы также активируют пути передачи сигналов, так что связывание с коллагенами (и с другими белками внеклеточного матрикса) изменяет активность в клетке биохимических процессов и, таким образом, способствует контролю над ростом и дифференцировкой клеток.
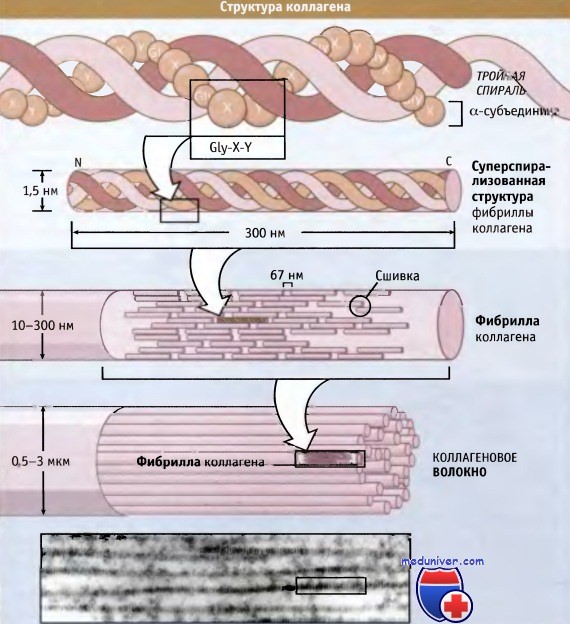
организация витой структуры в фибрилле (в середине) и фибрилл в коллагеновом волокне (внизу).
Наличие 67-нм зазора между соседними спиральными структурами обусловливает видимую в электронном микроскопе исчерченность фибрилл, составляющих волокно. 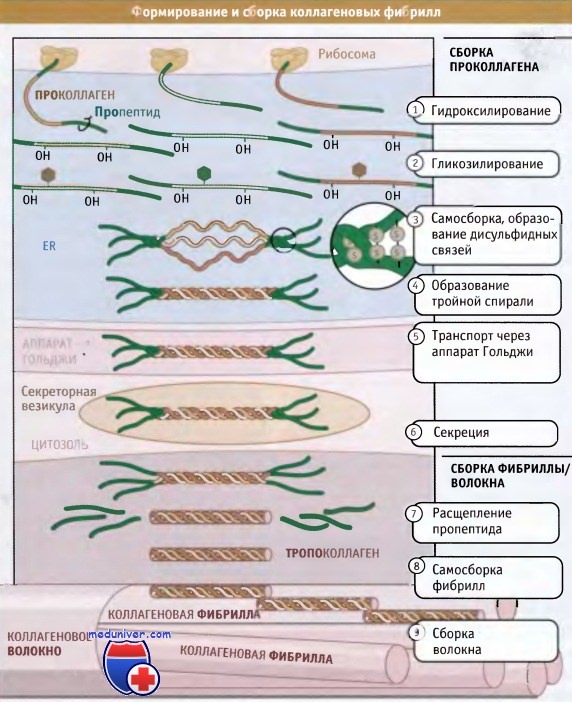
Однако сборка фибрилл происходит во внеклеточном пространстве после секреции тройных спиралей, обладающих витой структурой.
Для упрощения в тройных структурах не показаны гидроксильные группы и сахарные остатки. 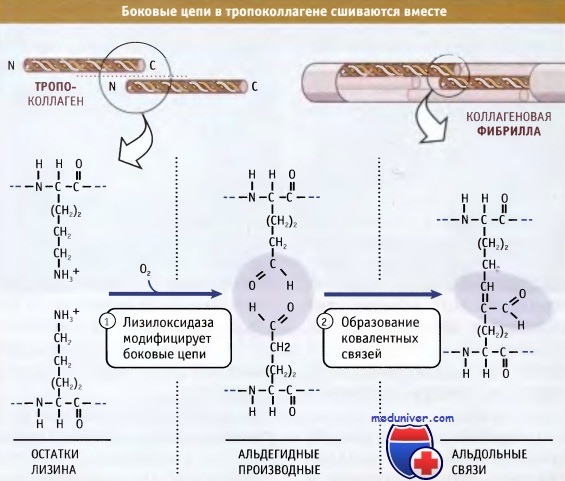
которые затем образуют между собой альдольную связь.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Какие бывают типы и виды коллагена?
Коллаген − это белок, состоящий из нескольких аминокислот, включая гидроксипролин, глицин, лизин, аргинин. Он является основой и строительным материалом для всех соединительных тканей в человеческом организме. Это вещество содержится в наших суставах, хрящах, связках, коже и ногтях, но постепенно его количество уменьшается в организме, и поэтому добавки и косметика с коллагеном стали настолько популярными.
Коллаген подразделяется на типы – делится по принципу пользы для организма, и виды – по принципу источника, из которого выделяют коллаген. Разберёмся в нюансах классификации этого важного для человека белка.
Существующие типы коллагена
I и III тип
Первый и третий тип часто ставят рядам, т.к. отвечают они за схожие функции. А именно – за эластичность кожи и обновление её клеток, водный баланс, уменьшение степени изменений, приходящих с возрастом, и усвоение питательных веществ. В продающихся коллагеновых добавках эти два типа тоже часто объединены вместе.
Первый тип является в человеческом организме основным и также находится в наших костях, сухожилиях, связках и дёснах. Третий – в мышцах и кровеносных сосудах. Но основная их функция в поддержании кожных покровов в нормальном состоянии.
II тип
Типы коллагена в продуктах
Коллаген можно получать не только из БАДов, но и из привычных нам продуктов питания.
Как принимать разные типы коллагена?
Дневная норма
Рекомендуемая профилактическая доза I и III типа коллагена − 5000 мг. Так вы улучшите состояние волос и эластичность кожи.
Терапевтическая доза I и III типа коллагена составляет 10000 мг. Такое количество стоит принимать при различных травмах и переломах. Принимать коллаген для терапевтического эффекта стоит 2-3 раза в день, т.к. за один раз усваивается только 5000 мг.
II тип коллагена стоит принимать только для терапевтического эффекта, например, при заболеваниях суставов – дозировка составляет 40 мг в сутки.
Сколько пить по времени?
Стандартный профилактический курс приёма коллагена – 2-3 месяца, всё индивидуально, нужно учитывать свой возраст и цели, преследуемые приёмом коллагена, с последующим трёхмесячным отдыхом. Потом курс следует повторить. При проблемах со здоровьем, суставами, менопаузе или возрастных изменениях курс лечения составляет 6 месяцев с последующими 2 месяцами отдыха.
Производители всегда прикладывают инструкции с рекомендуемой схемой и длительностью приёма именно их биологически активной добавки – прислушивайтесь к ним.
Как пить?
Существующие виды коллагена
Под видом, источником, коллагена подразумевается сырьё, из которого его получают. Коллаген по такому принципу делят на животный, морской и растительный.
Эффективность и биологическая доступность коллагеновой добавки полностью зависит от источника белка.
Животный
Коллаген животного происхождения (говяжий) является наиболее популярной разновидностью такого белка. Его получают путём обработки сырых шкур, суставов и хрящевой ткани крупных рогатых животных. Этот вид достаточно хорошо усваивается и обладает эффектом заживления ран, способствует регенерации и увлажнению. Стоимость этой добавки самая демократичная из всех трёх видов, но есть два недостатка:
Морской
Морской коллаген (его ещё именуют «рыбным») получают из чешуи морских рыб и других обитателей моря. По своему составу этот вид коллагена ближе всего к человеческому, поэтому он легче и лучше воспринимается нашим организмом. Основное преимущество морского коллагена заключается в том, что он может стимулировать производство собственного коллагена в организме и менее аллергенен, чем животный вид.
Минусы морского вида коллагена:
Откройте для своей кожи 8 пищевых продуктов, богатых коллагеном
Влияние коллагена, что важно?
Коллаген является основным компонентом, который составляет основу соединительной ткани организма: мышц, сухожилий, связок, кожи, хрящей, суставов и т.д. Это один из главных компонентов, отвечающий за ь прочность и эластичности всей соединительной ткани, в том числе и стенок кровеносных сосудов и сердца.
С возрастом выработка коллагена постепенно снижается. Примерно после 35-40 лет выработка коллагена в организме сокращается, что может вызывать проблемы (дряблость и провисание кожи, появление морщин). Кроме того, снижение выработки коллагена может привести к таким заболеваниям как: остеоартрит, боли в суставах и мышцах.
Преимущества коллагена для кожи
К основным преимуществам коллагена для кожи относятся:
Продукты, которые улучшают выработку коллагена в коже
Не секрет, что для того, чтобы организм получал все необходимые витамины и питательные вещества, питание должно быть разнообразным и сбалансированным. Употребление достаточного количества жидкости также влияет на выработку коллагена и гидратации кожи. Это самый простой и доступный способ поддерживать выработку коллагена.
Не существует никаких чудодейственных препаратов и средств для кожи, но есть те, которые способствуют повышению упругости кожи и позволяют ей выглядеть здоровой.
Мы составили список продуктов, которые способствуют выработке коллагена:
1. Животный белок: мясо и рыба
В белке животного происхождения (мясо, субпродукты, желатин животного происхождения) содержится большое количество коллагена.
Важно избегать полуфабрикатов.
Эксперты рекомендуют употреблять мясо красного цвета умеренно (не более одного раза в неделю).
Рыба, особенно лосось, тунец или форель с высоким содержанием омега-3 жирных кислот естественно повышает концентрацию коллагена (также являясь полезными для костей и суставов).
2. Фрукты и овощи
А фрукты богатые витамином С необходимы для производства коллагена: апельсин, киви, грейпфрут, манго, ананас и некоторых других. Например, лимон не стимулирует производство коллагена, но и действует, как антиоксидант.
3. Яйца
Яйца являются лучшей пищей для нашей кожи, ведь в них большая концентрация ценных белков и витаминов группы В, Е, аминокислот и серы).
4. Сухофрукты и орехи
Арахис, грецкие орехи, фисташки, миндаль также стимулирует выработку коллагена.
5. Молочные продукты
Молочные продукты (молоко, сыр, йогурт и т.д.) благотворно влияют на производство коллагена благодаря высокому содержанию белка.
6. Серные продукты
Нужно употреблять в пищу продукты, которые содержат серу в своём составе (чеснок, лук, сельдерей, огурцы, оливки, виноград) они тоже обеспечивают хороший уровень коллагена в организме.
7. Чай
Чай (зеленый, белый, черный или красный) является натуральным антиоксидантом, который предотвращает снижение коллагена в нашем организме.
8. Желе
Желатин в организме превращается в коллаген и это тоже ценный источник животного белка.
Масло Bio-Oil способствует улучшению эластичности вашей кожи
Употребляйте в пищу полезные продукты и не забывайте про ритуал красоты с использованием масла Bio-Oil утром и вечером для сохранения красоты и молодости вашей кожи.










