Актуальные вопросы тяжелой герпетической инфекции у взрослых
В настоящее время неуклонно увеличивается число больных рецидивирующей герпетической инфекцией, вызванной вирусами простого герпеса (ВПГ) 1 и 2 типа различной локализации. Наиболее распространенная локализация у взрослых лиц — аногенитальная и лабиальная
В настоящее время неуклонно увеличивается число больных рецидивирующей герпетической инфекцией, вызванной вирусами простого герпеса (ВПГ) 1 и 2 типа различной локализации. Наиболее распространенная локализация у взрослых лиц — аногенитальная и лабиальная. Многие вопросы патогенеза и терапии тяжелого и крайне-тяжелого течения герпесвирусной инфекции по-прежнему не решены.
Вид ВПГ относится к семейству Herpesviridae, подсемейству L-Herpesviridae, виду ВПГ. Различают два основных типа вируса — ВПГ 1 и ВПГ 2. Инфицирование возможно как одним, так и двумя типами возбудителя. ВПГ способен внедряться в различные клетки организма человека: в клетки кожи, слизистых оболочек урогенитального и желудочно-кишечного трактов (ЖКТ), дыхательных путей, центральной и периферической нервной системы, печени, эндотелия сосудов, а также в клетки крови — лимфоциты и др. [1]. Место постоянного обитания (пожизненного персистирования) ВПГ — паравертебральные сенсорные ганглии. ВПГ передается прямым контактным путем, возможна передача возбудителя контактно-бытовым и вертикальным путем (от матери к плоду), а также трансфузионным и парентеральным путями через инструменты при оперативных вмешательствах, стоматологических процедурах и т. д.
Как известно, большинство людей инфицированы ВПГ. Первичный иммунный ответ на инфекцию протекает латентно или с герпетическими высыпаниями с местной и общей воспалительной реакцией. У лиц с нормальным иммунным ответом размножение (репликация) ВПГ находится под иммунологическим контролем, и рецидивы бывают крайне редко или не возникают в течение всей жизни. В противовирусной защите организма участвуют факторы неспецифической защиты, уничтожающие или блокирующие вирусы: макрофаги и другие клетки-продуценты интерферонов (ИФН) α, β и γ, ряд интерлейкинов (ИЛ) (фактор некроза опухоли (ФНО), ИЛ-6 и др.), естественные киллеры и факторы, формирующие специфический иммунный ответ против конкретного вируса: цитотоксические Т-лимфоциты (ЦТЛ) (CD 8+ Т-лимфоциты) и В-лимфоциты, ответственные за продукцию специфических антител, блокирующих репликацию вируса и расположенные вне клетки вирусы. Для адекватного функционирования этих клеток и поддержания иммунного ответа необходима соответствующая продукция ИФН и ИЛ.
Под влиянием различных экзогенных и эндогенных факторов, повреждающих иммунную систему, возможно ослабление контроля над репликацией вируса и соответственно развитие рецидива. Рецидив ВПГ-инфекции могут спровоцировать другие инфекционные заболевания, переохлаждение, чрезмерная инсоляция, психические или физические стрессы, интоксикации различного генеза, в том числе употребление алкоголя, циклические изменения гормонального статуса (менструации), особенно при дисбалансе уровня гормонов у женщин, резкая смена климатических поясов и др.
При длительной хронической инфекции вирусы оказывают многостороннее неблагоприятное действие на иммунную систему человека. ВПГ прямо повреждают клетки иммунной системы (лимфоциты, макрофаги и естественные киллеры). Синтезируя белки-супрессоры и химерные белки, вирусы угнетают многие реакции иммунитета: ВПГ могут блокировать действие ИФН, нарушать распознавания инфицированных клеток и другие защитные реакции. Кроме того, высокая мутационная активность вирусного генома также способствует ускользанию вируса от иммунологического контроля.
Хроническая, часто рецидивирующая ВПГ-инфекция может провоцировать развитие аутоиммунных состояний (антифосфолипидный синдром, аутоиммунный тиреоидит, аутоиммунные васкулиты и др.). Кроме того, при интеграции ВПГ в генетический аппарат клеток возможна неопластическая трансформация клеток. Так, ВПГ является одним из факторов повышенного риска развития рака тела и шейки матки и других онкологических заболеваний. Также ВПГ-инфекция является одной из ведущих причин самопроизвольных абортов, преждевременных родов, рождения детей с патологией центральной нервной системы и внутренних органов. ВПГИ ассоциирована со многими «болезнями цивилизации» — атеросклерозом, ишемической болезнью сердца у лиц моложе 50 лет и др. Тяжелое течение ВПГИ может быть маркером онкологических заболеваний и СПИДа [7].
В зависимости от числа и выраженности рецидивов, выделяют легкое, среднетяжелое и тяжелое течение болезни (табл. 1).
При тяжелом течении ВПГ-инфекции возможно одновременное появление нескольких очагов поражения (например, в области половых органов, губ, крыльев носа), а также последовательное возникновение высыпаний разной локализации (один рецидив на фоне другого), продолжительность обострения при этом может достигать 16–20 дней. В месте высыпания больные ощущают жар, жжение, боль, напряжение и/или зуд кожи. На инфильтрированной коже появляется группа пузырьков, заполненных прозрачным содержимым. Пузырьки могут сливаться в сплошной многокамерный элемент. Прозрачное их содержимое затем мутнеет. Пузырьки в дальнейшем вскрываются, образуя мелкие эрозии, или подсыхают и превращаются в корочки. Возможно наслоение вторичной бактериальной инфекции. При рецидивах ВПГ часто поражает одни и те же участки кожи. Как правило, при тяжелом течении инфекции значительно ухудшается физическое и психическое состояние больных. У части пациентов в период рецидива увеличиваются или появляются слабость, лихорадка, озноб, миалгии, цефалгии, артралгии, раздражительность, нарушение сна, эмоциональная лабильность, также могут развиваться тяжелые депрессивные состояния, требующие медикаментозной коррекции. По данным органов здравоохранения США, ВПГ-инфекция аногенитальной локализации является примерно в 10% случаев причиной депрессий и суицидов. Тяжелое течение генитальной формы ВПГ-инфекции с частыми рецидивами приводит к нарушению нормальной половой функции пациента, болезнь нередко создает конфликтные ситуации в семье, на работе. Лечение больных с тяжелым течением ВПГ-инфекции представляет собой сложную задачу и должно включать как медикаментозную терапию, так и психологическую адаптацию пациента.
У больных с тяжелой ВПГ-инфекцией в большинстве случаев не наблюдается стойкого и значимого клинического эффекта в ответ на эпизодические курсы комбинированной терапии (противовирусные и иммунотропные средства, общеукрепляющие препараты). Как правило, такие больные меняют много лечебных учреждений в поисках адекватной помощи.
С течением заболевания появляется много побочных реакций на медикаменты или их непереносимость, в ряде случаев развивается устойчивость ВПГ к ацикловиру, ИФН a, другим средствам. Иммуностимуляторы, используемые эмпирически, могут приносить облегчение в период их приема, но во многих случаях они оказываются неэффективными и даже ухудшают клиническое течение болезни. Усугубляются проявления вторичного иммунодефицита, присоединяются другие инфекции, субдепрессивные состояния переходят в стойкие нарушения психики, теряется вера больных в выздоровление, в возможность современной медицины им помочь.
Для разработки современных подходов к лечению и контролю над ВПГ-инфекцией и более углубленного понимания патогенеза заболевания нами было изучено состояние различных звеньев противовирусной защиты и системы цитокинов у больных с тяжелым и крайне тяжелым течением ВПГ-инфекции аногенитальной и лабиальной локализации, а также степень инфицированности (системности заболевания) и частота сочетания с другими герпесвирусными инфекциями.
Обследовано 102 больных, страдающих тяжелой ВПГ-инфекцией более 2 лет (28 мужчин и 74 женщины, средний возраст — 34 ± 1,5 года) и имеющих частоту рецидивов более шести в год.
При этом у 60 больных наблюдалось от 6 до 11 рецидивов ВПГ-инфекции в год, а у 42 больных — от 12 до 20 рецидивов. У большинства пациентов преобладала аногенительная или смешанная локализация герпеса. Средняя длительность тяжелого течения заболевания составила 9,3 ± 1,2 года. Группу контроля составили 32 практически здоровых добровольца (14 мужчин и 18 женщин, средний возраст — 32 ± 1,6 года). Анализ ряда изучаемых параметров включал результаты обследования пациентов с легким течением заболевания (36 человек — 10 мужчин, 26 женщин, средний возраст — 33,4 ± 2,1 года, с частотой рецидивов 2,9 ± 0,8 в год). При рецидивах жалобы больных были характерными. Часто встречались депрессия, раздражительность, снижение памяти и другие нарушения физического и психического состояния и познавательных функций.
У многих больных в анамнезе были указания на повторные курсы противовирусной и/или иммунотропной терапии, оказывавшей неоднозначное влияние: или кратковременное положительное влияние на течение ВПГ-инфекции, или ухудшение и развитие рецидива на фоне или после отмены иммунокоррекции. Такие анамнестические данные отражают тяжесть иммунной недостаточности и неадекватность проводимой эмпирической терапии без оценки иммунного статуса и индивидуального подбора иммунокорректоров, а также восстановительной терапии — иммунореабилитации [5].
При обследовании больных с тяжелым течением ВПГ-инфекции выявлялись многие маркеры вторичного иммунодефицита в виде хронических инфекционно-воспалительных заболеваний различной локализации, со смешанным характером микрофлоры и в большинстве случаев ее устойчивостью к повторным курсам антибиотикотерапии. Из 102 больных хронической ВПГ-инфекцией тяжелого течения выявлены:
Эти данные свидетельствуют о необходимости комплексного подхода к лечению ВПГ-инфекции тяжелого течения с учетом осложнений вторичного иммунодефицита.
Кроме того, проводили ПЦР-исследование биологических материалов на наличие ДНК ВПГ 1 и 2 типа и других вирусов герпес-группы: цитомегаловируса, вируса герпеса человека (ВГЧ) 6 типа, вируса Эпштейна–Барр. Используемые нами программы амплификации позволяли выявлять ДНК вирусов на уровне, соответствующем активной их репликации. Наличие активной репликации вирусов подтверждали полуколичественным ПЦР-исследованием и серологическими тестами.
В результате исследования у больных с тяжелым течением ВПГ-инфекции обнаружены лабораторные признаки вторичного иммунодефицита.
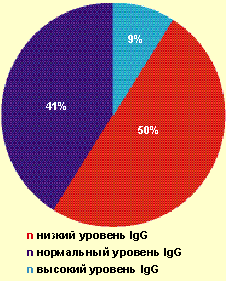 |
| Рисунок 1. Частота выявления различных значений IgG у больных с тяжелым течением ВПГ-инфекции |
Так, у большинства пациентов (91%) отсутствовало адекватное повышение продукции IgG в ответ на рецидив ВПГ-инфекции (рис. 1). При частоте рецидивов ВПГ-инфекции 6–11 рецидивов в год низкий уровень IgG выявлялся у 25% больных, при частоте — 12–20 рецидивов в месяц — уже у 64,3% больных. Более чем у 70% больных был повышен уровень ЦИК в 1,5–2,0 раза от показателей нормы. Известно, что длительная циркуляция ЦИК может приводить к отложению их на эндотелии сосудов и служить одним из факторов формирования аутоиммунной патологии.
У большинства больных с ВПГ-инфекцией тяжелого течения (70%) были обнаружены нарушения в системе естественной и/или специфической цитотоксичности (рис. 2) — снижение содержания зрелых активированных естественных киллеров CD16 + (менее 11%), Т-киллеров и/или ЦТЛ CD8 + (менее 27%). Важно отметить, что выраженное снижение уровня CD8 + (в состав которых входят также и супрессорные клетки) в большинстве случаев сочеталось с повышением уровня CD4 + и иммунорегуляторного индекса, что является фактором риска в отношении формирования аутоиммунных процессов. Как известно, системы естественной и специфической цитотоксичности играют ведущую роль в противовирусной защите.
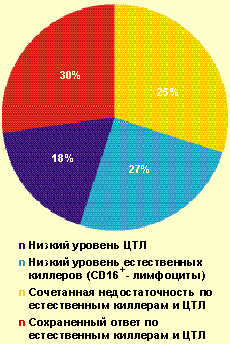 |
| Рисунок 2. Частота выявления нарушений в системе естественной и специфической цитотоксичности у больных с тяжелым течением ВПГ-инфекции (n = 102) |
Обнаруженные нарушения в системах цитотоксичности и их активационных маркерах при ВПГ-инфекции косвенно свидетельствуют о недостаточном уровне продукции Т-хелперами 1 типа ИЛ-2 — одного из важнейших звеньев цитокиновой сети, необходимого для полноценного противовирусного иммунного ответа.
При исследовании функционального состояния нейтрофилов у больных с тяжелым течением ВПГ-инфекции повышение спонтанного НСТ-теста было выявлено почти в половине случаев. Однако показатели стимулированного НСТ-теста и индекса стимуляции, напротив, были существенно снижены у большинства больных, что свидетельствует об истощении у них резервных способностей нейтрофилов.
Н. А. Дидковский, доктор медицинских наук, профессор
И. К. Малашенкова, кандидат медицинских наук
Ж. Ш. Сарсания, кандидат биологических наук
А. Н. Танасова, И. Н. Зуйкова, И. А. Зуйков, Н. М. Хитрик
НИИ физико-химической медицины, ММА им. И. М. Сеченова, Москва
Комплексный подход в лечении герпеса
Поделиться:
Самые частые проявления герпеса, с которыми сталкивается большинство людей, – это простуда на губах, генитальный герпес и ветряная оспа (ветрянка). Одной из причин проявления болезни может стать снижение иммунитета.
Поэтому при выборе лекарства от герпеса следует обращать внимание на то, как действует препарат: помогает устранить проявления герпеса или оказывает комплексное воздействие – противовирусное, иммуностимулирующее и противовоспалительное.
Сочетание этих свойств помогает воздействовать на болезнь сразу в нескольких направлениях и может способствовать уменьшению периода болезни и снижению частоты рецидивов.
Таким препаратом является «Циклоферон» в лекарственных формах линимент (5%) и таблетки.
Линимент «Циклоферона»
В зоне проявления высыпаний линимент «Циклоферона» создает иммунный барьер, препятствующий распространению инфекции. При этом «Циклоферон» (линимент) оказывает местное противовирусное действие, блокируя процесс размножения вирусов, и в то же время – местное противовоспалительное действие, облегчая симптомы проявления болезни (зуд, жжение).
При длительном или повторном применении у вируса герпеса не развивается устойчивость к «Циклоферону», что позволяет использовать препарат как «скорую» противовирусную помощь при каждом обострении герпеса.
Линимент «Циклоферона» легко впитывается и не оставляет следов на коже, равномерно распределяется по проблемным участкам, благодаря чему ускоряется процесс заживления поражённой поверхности. Линимент «Циклоферона» наносят тонким слоем на поражённый участок 1-2 раза в день в течение 5 дней до полного исчезновения симптомов заболевания. Линимент имеет жидкую структуру, что способствует более легкому нанесению препарата, равномерному распределению по пораженной поверхности кожи, улучшению впитываемости и большей биологической доступности лекарственных веществ. Однако следует проявлять осторожность при его хранении и транспортировке после вскрытия тубы.
При незначительных поражениях в области лица, протекающих легко, и редких рецидивах (1–2 раза в год) можно ограничиться наружным применением линимента «Циклоферона».
Если же герпес проявляется часто (3–6 раз в год) или причиняет сильные неудобства и боль, то необходимо обратиться к врачу. В таких случаях лечение может потребовать комплексного подхода, который сочетает системное применение пероральных и наружных средств. Например, таблеток «Циклоферона» внутрь по схеме приема и наружное использование линимента «Циклоферона». Схему приема и дозировку препарата назначает врач, исходя из индивидуальной клинической картины заболевания каждого пациента.
Комплексное сочетание двух лекарственных форм противовирусного препарата «Циклоферон» при лечении герпеса способствует сокращению периода болезни, повторных случаев проявления герпесвирусной инфекции (рецидивов), а также снижению риска осложнений.
Не только «простуда на губах»
«Циклоферон» линимент может быть рекомендован при появлении симптомов не только лабиального герпеса, но и при других формах герпесвирусных инфекций. Так, например, препарат может использоваться для лечения генитального герпеса у мужчин и женщин, а также при опоясывающем лишае и ветряной оспе.
Линимент «Циклоферона» разрешен к применению с 18 лет. Важно помнить, что появление герпеса требует обращения к врачу, потому что в каждом конкретном случае лечение индивидуально и зависит от формы инфекции, тяжести заболевания и частоты рецидивов.
ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ. ПЕРЕД ПРИМЕНЕНИЕМ ПРОКОНСУЛЬТИРУЙТЕСЬ СО СПЕЦИАЛИСТОМ.
Товары по теме: [product](ЦИКЛОФЕРОН 5% 5МЛ ЛИНИМЕНТ)
Памятка врачам при лечении герпеса
Введение
Простой герпес- группа заболеваний, этиологической причиной которой являются вирусы простого герпеса 1 и 2 типов. Хроническая герпесвирусная инфекция представляет традиционно трудную проблему, все еще далекую от своего решения. Это объясняется широкой распространенностью заболевания и недостаточной эффективностью, длительностью и дороговизной существующих методов лечения.
Доказана роль вирусов герпеса в развитии рака шейки матки, предстательной железы. Показано неблагоприятное, а порой фатальное влияние герпесвирусов на течение беременности и родов, патологию плода и новорожденных. Доказано возникновение аутоиммунизации при длительной персистенции герпесвирусов. Геном ВПГ может интегрировать с геномом вирусов и бактерий (ОРВИ, ВИЧ, грипп, аденовирусы…), вызывать их активацию с последующим прогрессированием инфекции. Вирусы герпеса индуцируют процессы атеросклероза; влияют на процесс психического развития человека; вызывают патологию нервных клеток во всех областях коры. Длительная персистенция вирусов герпеса обусловливает снижение не только биофункционального статуса организма человека, но, изменяя его психическую направленность, имеет серьезные социальные последствия.
Патогенез герпетической инфекции является иммуноопосредованным. Результаты проводившихся в последние годы исследований клеточных и гуморальных факторов иммунологического реагирования, элиминационых механизмов в ходе иммунного ответа свидетельствовали о первостепенном значении вышеуказанных механизмов защиты против вирусов герпеса.
Медико-биологическая и социальная значимость проблемы герпетической инфекции, недостаточная изученность многих вопросов патогенеза, открытие новых возможностей для повышения эффективности этиотропного и патогенетического лечения с применением иммуномодуляторов послужили основанием для проведения исследовательской работы коллективов Самарского диагностического центра и Клиники инфекционных болезней Самарского государственного медицинского университета. В предложенном пособии обобщен опыт авторов по диагностике и лечению герпетической инфекции.
С группой заболеваний, связанных с семейством герпесвирусов сталкиваются врачи различных специальностей. В таблице 1 (см. приложения) представлены данные по взаимосвязи этиологического фактора «вирус герпеса» и клинических диагнозов.
Этиология
Вирус простого герпеса (ВПГ) входит в семейство герпесвирусов, имеющих сходную структуру и общие антигены. Известно более 100 серологических групп, 8 из которых являются возбудителями инфекции у человека.
Синтез вирусных белков начинается через 2 часа после заражения, достигая максимума через 8 часов. Инфекционные вирионы появляются через 10 ч и достигают наивысших титров через 15 часов. Вирус размножается в ядре клетки, созревая путем почкования на ядерной мембране. В процессе формирования латенции герпесвирусы трансформируются в безоболочечные L- и PREP-частицы. На поверхности вируса, словно шипики, торчат гликопротеиды. Их длина составляет около 10 нм. Различают около 30 гликопротеидов и лишь при взаимодействии с 7 из них (Гликопротеиды B, C, D, E, F, G, X) иммунная система распознает вирус и вырабатывает к нему антитела.
Инактивируются вирусы простого герпеса под действием: рентгеновских и ультрафиолетовых лучей, спирта, органических растворителей, фенола, формалина, протеолитических ферментов, желчи, обычных дезинфицирующих средств. Режимы обеззараживания при вирусных инфекциях некоторыми дезинфицирующими средствами представлены в таблице 2.
Несколько слов о герпесе
Источник инфекции: вирусоносители (люди, не имеющие проЯвлений заболевания, например в виде пузырьковых зудящих высыпания на коже губ, носа, лица, по телу, в области половых органов) и больные различными формами заболеваний (в том числе с поражением внутренних органов, центральной нервной системы).
Прежде всего возможно прямое инфицирование плаценты и плода, особенно в 1 триместре при первичном инфицировании и приводит к развитию у плода микроцефалии или гидроцефалии, катаракты, глухоты, пороков сердца, желудчно- кишечного тракта, мочеполовой системы, скелета.
Инфицирование во 2 и 3 триместрах вызывает у плода увеличение печени и селезенки, анемию, желтуху, гипотрофию, пневмонию, менингоэнцефалит, сепсис. Восходящий путь инфицирования из шейки матки сопровождаетя развитием многоводия, невынашивания беременности, задержки внутриутробного развития, отечного синдрома.
Кроме того, возможно косвенное воздействие на плод, обусловленное лихорадкой, интоксикацией с последующим поражением фетоплацентарного комплекса.
Распространенность инфекции: Сероэпидемиологические исследования показали, что к 5-13 летнему возрасту уже 70-83% детей инфицированы вирусом простого герпеса, а в возрасте 50 лет и старше 90% населения имеют антитела к вирусам простого герпеса. Это означает, что практически все люди инфицированы вирусами простого герпеса.
Однако клинические проявления и потребность в лечении реально существует только у 20% инфицированных, 50% из которых имеют клинические проявления.
Особенностью течения современной герпесвирусной инфекции является формирование отдельных и множественных очагов инфекции с активными и латентными формами заболевания на фоне присоединения других заболеваний с половым инфицированием, которые выявляются в 25,6% случаев.
Патогенез. Особенности иммунологического реагирования
Оценка состояния иммунитета у больных с хронической герпесвирусной инфекцией показала, что в большинстве случаев имеется иммунологический дисбаланс.
Непродолжительное присутствие вируса в организме инфекционный процесс протекает в острой или бессимптомной форме.
Рецидивы находятся под иммунным контролем, состояние иммунного дефицита ведет к увеличению их частоты, более длительным периодам распространения вируса и пролонгированию симптомов.
Возникновение вирусной инфекции обусловлено конкуренцией вирусного и клеточного геномов. В основе “ускользания “ вируса от защитных факторов клетки лежит его мимикрия под необходимые для жизнедеятельности клетки частицы: факторы роста, питательные вещества, липопротеазы. Реактивируемая латентная герпесвирусная инфекция сенсорных нейронов периферических ганглиев является молекулярной основой рецидивов инфекции. Развитие вирусной инфекции происходит по схеме: адсорбция вируса, “ раздевание” его на поверхности клетки, проникновение ДНК в клетку, продукция нуклеиновых кислот и протеинов вируса для следующей генерации вируса, миграция новых вирионов из клетки в окружающую ткань. Инфицированная клетка погибает после продуцирования большого (от 100 до 1000) числа вирусов, но в некоторых клетках развивается персистентная инфекция.
Механизм развития латентной инфекции предсказан в 1929г. Goodposture. По мнению Stroop W.G., Baringer J., 1993г., механизм появления и развития персистенции вируса состоит из 5 условий:
Первая линия защиты при первичной инфекции представлена неспецифическими факторами резистентности: активация комплемента ускоряет мобилизацию и способствует направленному движению клеток к очагу воспаления. При этом С3 компоненту комплемента отводится первостепенная роль. Угнетение связывания С1 компонента комплемента может защищать клетки от лизиса классическим комплементным путем.
Тяжелое течение инфекции характеризуется выраженным дисбалансом системы ИФН: резко сниженная способность лейкоцитов к синтезу ИФН альфа-, бета, гамма.
При хронической вирусной инфекции на фоне снижения сывороточного ИФН отмечается более высокая способность лейкоцитов к продукции индуцированного ИФН альфа- и бета, гамма, что является основанием для назначения классических иммуномодуляторов с ИФН, индукторами интерферонообразования наряду с этиотропной терапией.
В случае выраженной депрессии активности ИФН- и иммунной систем (рецидив хронической инфекции, активная репродукция вируса), можно выявить существенное снижение сывороточного ИФН в сочетании с резким понижением индуцированной продукции лейкоцитами ИФН альфа, бета, гамма до 5-10% от уровня нормы. При этом возможна генерализация инфекции. Показана заместительная ИФН- терапия.
Классификация
Общепринятой классификации герпетической инфекции не существует. Предлагаемая Рахмановой А.Г. классификация систематизирует различные формы и варианты течения простого герпеса. Казанцевым А.П. в 1980г. была предложена классификация клинических форм генитального герпеса, согласно которой выделялись: герпетические поражения кожи, герпетические поражения полости рта и верхних дыхательных путей, генитальный герпес, герпетические кератиты и кератоконьюнктивиты, герпетические энцефалиты и менингоэнцефалиты, висцеральные формы герпетической инфекции, генерализованный герпес новорожденных. Самгин М.А., Халдин А.А., выделяют первичный и рецидивирующий герпес. Предложенные классификации не отражают тяжесть клинических проявлений, которые могут широко варьировать.
По Международной статистической классификации болезней и проблем, связанных со здоровьем (МКБ 10), заболевания, вызванные ВПГ, группируются следующим образом:
Клиническая классификация простого герпеса по Исакову В.А. и Ермоленко Д.К.(1991г.)
В зависимости от продолжительности присутствия вируса в организме:
С учетом механизма заражения
Формы простого герпеса с учетом распространенности процесса:
В зависимости от клиники и локализации патологического процесса
Классификация герпесвирусной инфекции по тяжести течения (Мокеева М.В., 2001г.)
Клиника простого герпеса
Диссеминированные формы: появление 2-х и более типичных очагов на отдаленных друг от друга участках кожи. При этом отмечается синхронность клинических проявлений.
Мигрирующая форма: изменение локализаций высыпаний при каждом новом рецидиве.
Геморрагическая форма: вместо серозного появляется геморрагическое содержимое пузырьков. Геморрагическая форма часто сочетается с последующим развитием некроза и изьязвлений, формированием рупиоидных слоистых корок и с последующим рубцеванием тканей.
Зостериформная разновидность. Расположение высыпаний в зоне проекции того или иного нерва. Типичная локализация: конечности, туловище, лицо. Выраженные симптомы невралгии и общей интоксикации ( повышение температуры тела, головная и мышечные боли).
Абортивное течение. Воспаление ограничивается развитием эритемы и отека, без формирования типичных пузырьков. Боль, жжение, дискомфорт в местах обычной для больного локализаций.
Отечная форма. Локализация: веки, губы, мошонка. Может развиваться слоновость. При уплотнении рогового слоя вместо пузырьков могут формироваться мелкие плоские папулезные элементы.
Первый клинический эпизод при существующей герпетической инфекции – менее интенсивна, чем при первом клиническом эпизоде, но более выражена, чем при рецидивирующей форме болезни.
Рецидивирующий генитальный герпес. Рецидивы возникают под воздействием стресса, переохлаждения, переутомления, гормонального цикла. Часты «предвестники» в виде парестезий, после которых выспаний может не быть. Дизурия редка. Возможны герпетический уретрит, лимфаденит.
Асимптомный генитальный герпес. Реактивация ВПГ без развитием симптомов.
Особенности клинического течения герпесвирусных инфекций, вызываемых ВПГ-1, ВПГ-2 у больных с иммунодефицитами. Частота и тяжесть реактивации герпетической инфекции в значительной степени зависят от причин, вызвавших иммуносупрессию. Наиболее часто реактивация отмечается у больных, перенесших трансплантацию костного мозга, почки, больных лимфомами, лейкозами. Особенности клинического течения заболевания являются: атипичное течение (например- язвенно- некротический стоматит у больных с герпесом на коже губ, распространение инфекции лицо, глотку, пищевод, появление высыпаний в промежности, перианальной области с развитием проктита, генерализованное поражение кожи), тяжелое течение (обширные поражения с выраженной болью с длительным периодом эпителизации, диссеминация на внутренние органы с развитием пневмоний, энцефалитов, гепатитов с высокой летальностью), присоединение вторичной инфекции (бактериальной, грибковой).
Лечение
Ряд исследователей указывают на следующие подходы к противовирусной терапии:
Диагностика
Лабораторные методы исследования используются для уточнения этиологии заболевания при атипичных формах инфекции, а также с целью дифференциальной диагностики с другими заболеваниями. Исследуют содержимое везикул, смывы с тканей и органов, мазки- отпечатки, соскобы, биологические жидкости и секреты (слизь, моча, секрет предстательной железы, пробы крови).
Профилактика герпетической инфекции
Обследовать и лечить половых партнеров. Избегать всех форм половой жизни во время обострения вплоть до полной эпителизации эрозий.
Диспансерное наблюдение
Приложения
Таблица 1. Разнообразие этиологии и клинических диагнозов при герпес-вирусных инфекциях
Врач
Локализация
Этиология
“Топический” диагноз
Дерматовенеролог
Инфекционист
Терапевт
Педиатр
Простой (острый или рецидивирующий) герпес кожи (диссеминированная, мигрирующая, геморрагическая, некротическая, зостериформная, эрозивно-язвенная, отечная, абортивная и другие формы), ветряная оспа, опоясывающий герпес, инфекционный мононуклеоз
ВПГ-1 и ВПГ-2, ВВЗ, ВЭБ
Стоматит, гингивостоматит, лимфаденит, лимфангиит
Герпетическая ангина (простая, отечная,геморрагическая, некротическая, эрозивно-язвенная и другие формы), лимфаденит, лимфангиит
ВПГ-1 и ВПГ-2, ВВЗ, ЦМВ
Герпетические дерматит век, блефарит, блефароконъюнктивит, конъюнктивит, кератит эпителиальный или стромальный, увеит, язва роговицы, постгерпетическая кератопатия, ирит, герпетический иридоциклит, хориоретинит, неврит и другие формы
ВПГ-1 и ВПГ-2, ВВЗ, ЦМВ
Первый клинический эпизод первичного генитального герпеса (ГГ), первый клинический эпизод при существующем ГГ, рецидивирующий ГГ (РГГ), асимптомный ГГ
ВПГ-1 и ВПГ-2, ВВЗ, ЦМВ
Постгерпетическая невралгия (ПГН), острые или рецидивирующие: энцефалит, вентрикулоэнцефалит, менингит, миелиты, полинейропатии, энцефаломиелорадикулоневрит
Лимфаденит, неходжкинская лимфома, саркома Капоши



