Коагулограмма: все, что нужно знать о свертывании
Свертывание крови – процесс многоступенчатый, сложный и, при этом, чувствительный к действию целого ряда факторов. При этом симптомы «неполадок», как правило, долго не дают о себе знать. И анализ на свертываемость часто выявляет нарушения «случайно». Так кому же следует держать гемостаз «под присмотром»? И как понять показатели тем, кто уже проходит лечение?
Кому показан анализ
Исследование свертываемости крови, в первую очередь, показано тем, кто:
Не стоит исключать из внимания и значимые факторы риска, как курение, лишний вес, малоподвижный образ жизни, возраст старше 40 лет, частые перелеты и другие.
Ну и, конечно же, такой анализ обязателен перед любой операцией, а также для тех, кто уже принимает «противосвертывающие» препараты.
О чем говорят показатели
Набор «стандартной» коагулограммы (50.0.H94.203) включает определение:
Но что означают эти показатели?
1. АЧТВ, или активированное частичное тромбопластиновое время
Оценивает скорость образования сгустка крови после добавления к плазме специальных реагентов, и измеряется в секундах.
Иными словами, АЧТВ демонстрирует эффективность остановки кровотечения за счет плазменных факторов свертывания (как раз тех, что образуются в печени).
При этом, удлинение (повышение) показателя сигнализирует о риске кровотечений, а укорочение – тромбоза.
А особенно «актуален» анализ для людей, принимающих прямые антикоагулянты (гепарин и другие).
2. Протромбиновое время (ПВ)
Это временной отрезок, за который происходит образование нитей фибрина, то есть собственно предшественника тромба.
Показатель измеряется в % от нормы, которая составляет 70-120%.
Чем выше этот показатель – тем выше скорость образования тромба, а значит – и риск тромбоза.
А уменьшение ПВ – сигнал о склонности к кровотечениям.
3. МНО
Такие «сложности» стали необходимостью в связи с тем, что МНО – базовый анализ для подбора и коррекции «противосвертывающих» препаратов (как например, варфарин). А данные, полученные на разной аппаратуре (в разных лабораториях) зачастую не давали возможности сравнения между собой.
Поэтому Международный комитет по стандартизации в гематологии и Международный комитет по тромбозу и гемостазу в 1983 году ввели в использование МНО.
И сегодня, его уровень для здорового человека находится на уровне 0,8-1.2. А для принимающих непрямые антикоагулянты – 2,0-4,0.
При этом, повышение МНО ассоциировано с риском кровотечений, а снижение менее 0,5 – может говорить о тромбозе.
4. Фибриноген
В отличие от предыдущих показателей, это непосредственно субстрат для образования тромба. То есть не показатель скорости, а вещество. Поэтому и нормы для фибриногена измеряются в граммах на литр.
Повышение фибриногена наблюдается не только при повышенном тромбообразовании, но и при многих воспалительных процессах (как способ организма ограничить распространение «причинного фактора» и разрушенных тканей). А также у тех, кто принимает оральные контрацептивы или имеет повышенный уровень эстрогенов, беременных, людей с повышенным холестерином и курящих.
А снижение показателя может говорить не только о риске кровотечений, но и о заболеваниях печени.
Разумеется, перечисленные показатели являются только «базой» для оценки «здоровья» свертывающей системы крови. И в случае обнаружения значимых отклонений могут понадобиться дополнительные маркеры.
Основы антикоагулянтного лечения острого венозного тромбоэмболизма
Ежегодно в мире у 0,1% населения регистрируется венозный тромбоэмболизм (ВТЭ). С практической точки зрения, по современным представлениям, ВТЭ объединяет венозный тромбоз (ВТр) — тромбообразование в венозном русле кровообращения и венозную эмболию — пер
Ежегодно в мире у 0,1% населения регистрируется венозный тромбоэмболизм (ВТЭ). С практической точки зрения, по современным представлениям, ВТЭ объединяет венозный тромбоз (ВТр) — тромбообразование в венозном русле кровообращения и венозную эмболию — перенос части тромба в вены, дистальнее кровотока. Наиболее часто ВТЭ оказывается представлен тромбозом глубоких вен голени (ТГВ) и тромбоэмболией легочной артерии (ТЭЛА).
ТЭЛА — это одно из самых катастрофических осложнений, которое внезапно обрывает жизнь многих больных, унося каждый год только в США 150–200 тыс. жизней [1]. Существенное влияние на снижение риска фатального исхода ТЭЛА оказывают своевременно начатые диагностика и лечение. Неадекватная антикоагулянтная терапия может послужить причиной развития посттромбофлебитического синдрома, рецидивирующего тромбоэмболизма и тромбоэмболической легочной гипертензии. Без антикоагулянтной терапии в 11–26% случаев ВТЭ может осложниться ТЭЛА со смертельным исходом [2]. Поэтому после постановки диагноза ВТЭ целью лечения являются устранение симптомов болезни, предупреждение увеличения размеров тромба, эмболизации и ретромбозов.
Стандартная практика лечения больных с ТГВ и ТЭЛА принципиально не различается, так как наличие самой эмболии иногда служит единственным признаком того, что у больного имеется латентно протекающий эмбологенный тромбоз.
Стартовая терапия
Терапия ВТЭ начинается с 4–7-дневного введения гепаринов (нефракционированного или низкомолекулярного).
В таблице 1 представлены варианты выбора гепаринотерапии для стартового лечения.
Нефракционированный гепарин (НФГ). Гепарин — непрямой ингибитор тромбина, для осуществления антикоагулянтного действия которого необходим ко-фак-тор — антитромбин III. Комплекс гепарин-антитромбин III инактивирует несколько факторов свертывания: тромбин (II), Xa, XIIa, XIa, IXa. Среди них наибольшей чувствительностью к инактивации отличаются факторы Xa и IIa (тромбин). Кроме антикоагулянтного эффекта, НФГ, соединяясь с остеобластами, активирует остеокласты, ускоряя потерю костной ткани [3].
Определить концентрацию НФГ в крови невозможно, так как в свободном состоянии в циркуляции он отсутствует, поэтому дозу препарата необходимо подбирать, ориентируясь на оценку гипокоагуляции, вызываемой им. Наиболее приемлемым является тест определения активированного частичного тромбопластинового времени (АЧТВ). Рекомендованное терапевтическое удлинение АЧТВ основано на экспериментальных данных, показавших, что клинический эффект достигается при таком терапевтическом уровне НФГ, который удлиняет АЧТВ в 1,5–2,5 раза.
НФГ не обладает специфическим связыванием с определенными плазменными или клеточными белками, что предопределяет его различное гипокоагулянтное воздействие на пациентов. У 25% больных с ВТЭ, несмотря на получаемые ими дозы НФГ — более 35 000 ЕД в сутки, удлинение АЧТВ не достигает терапевтических значений. Данный феномен связан с так называемой резистентностью к НФГ [4]. Большинство из «резистентных» пациентов имеют достаточный уровень НФГ в крови, но повышенную концентрацию прокоагулянтов [5]. Не так часто встречаются случаи, когда у пациентов не удлиняется АЧТВ и не поддерживается достаточная концентрация НФГ, несмотря на вводимые высокие дозы препарата. Данный эффект является следствием нейтрализации гепарина белками плазмы крови, эндотелиальными клетками и повышенным клиренсом гепарина. Редко резистентность к НФГ вызвана низким уровнем антитромбина III. Основными причинами дефицита антитромбина являются гепатит, цирроз печени, нефротический синдром, беременность, прием оральных контрацептивов, синдром диссеминированного внутрисосудистого свертывания, острое воспаление и др. С практической точки зрения в данных клинических случаях определяющим фактором эффективности лечения НФГ является доза препарата, а не показатели АЧТВ [6].
При назначении НФГ с лечебной целью следует отдавать предпочтение внутривенному непрерывному способу его введения, который позволяет поддерживать оптимальные значения АЧТВ на протяжении суток. Для стартового лечения ВТЭ НФГ вводится путем внутривенной постоянной инфузии (1200–1300 ЕД/ч или 18 ЕД/кг/ч) после болюсной дозы 5000 ЕД или 80 ЕД/кг [5].
Для подбора дозы гепарина в зависимости от показателей АЧТВ используются алгоритмы, предложенные Американской ассоциацией сердца [7]. Алгоритм, представленный в таблице 2, следует задействовать в тех случаях, когда используются одинаковые реактивы АЧТВ и контрольное АЧТВ находится в одинаковых пределах. Первая доза одинакова для всех больных, дальнейшая скорость инфузии (32 000 ЕД/24 ч) относится только к первым 6 ч лечения, по прошествии этого времени необходимо корригировать дозу в соответствии с номограммой, исходя из значений АЧТВ.
В других случаях может быть применена номограмма, приведенная в таблице 3, в которой использованы не абсолютные величины АЧТВ, а его изменения по отношению к контрольному АЧТВ, определенному конкретной лабораторией.
Большие кровотечения при данном терапевтическом подходе составляют 2% и зависят от дозы препарата, возраста пациента, функционального состояния почек и печени, недавно перенесенных операций, травм и инвазивных процедур, злоупотребления алкоголем, сопутствующей терапии — тромболитических препаратов, антагонистов тромбоцитарных гликопротеинов IIb/IIIa, ацетилсалициловой кислоты [5].
Метаанализ результатов клинических исследований показал, что подкожное применение НФГ для лечения венозных тромбозов сопоставимо по эффективности и безопасности с внутривенным путем введения при условии подбора адекватных доз и надлежащего лабораторного контроля. Поскольку биодоступность НФГ при подкожном пути введения ниже (30%), чем при внутривенном, начальные дозы НФГ должны быть больше. Обычный режим для подкожного метода лечения НФГ включает начальный внутривенный болюс 5000 ЕД, далее подкожно дважды в сутки с последующим подкожным введением 17 500 ЕД и коррекцией дозы на основании АЧТВ [4, 8]. Для подбора дозы в зависимости от веса пациента и величины АЧТВ используют алгоритм, приведенный в таблице 4, при этом контроль АЧТВ проводится через 6 ч и далее по указанному протоколу.
Имеются результаты единичных исследований, в ходе которых изучалась эффективность подкожного введения НФГ для лечения ТЭЛА. Однако с достаточной уверенностью рекомендовать данный метод терапии не представляется возможным из-за небольшого количества достоверных клинических данных [10].
Гепарины низкого молекулярного веса (ГНМВ).
ГНМВ различаются по физико-химическим, биологическим, фармакологическим свойствам и нейтрализующей активности в отношении активного фактора Х (Ха) и тромбина (IIа), т. е. соотношения анти-Ха/анти-IIа-активности. Указанная гетерогенность имеет практическое значение: одинаковые дозы различных препаратов ГНМВ оказывают неодинаковое действие на фактор Ха и, как следствие, вызывают различный антикоагулянтный эффект. В связи с этим невозможно экстраполировать эффективность лечебного действия одного из ГНМВ на другие. Практически это разные препараты. Для контроля над эффективностью и безопасностью лечебного действия ГНМВ метод АЧТВ не применим, так как он не отражает антикоагулянтную активность используемых препаратов.
С этой целью применяется оценка инактивации активного фактора Х [5]. Доза низкомолекулярных гепаринов выражается в условных единицах (ЕД/кг массы тела), отражающих антифактор Ха-активность препаратов, определенную фирмой-производителем. В рутинной клинической практике лабораторный контроль за эффективностью ГНМВ не производится. Следует помнить, что подобранные по весу дозы ГНМВ адекватны для больных, чей вес не превышает 150 кг. Данной категории больных, а также беременным и пациентам с нарушенной функцией почек целесообразно определять анти-фактор Ха-активность вводимого препарата.
Анализ результатов исследований по оценке эффективности и безопасности подкожного применения фиксированных доз ГНМВ для лечения больных с ВТЭ в сравнении с НФГ, вводимым внутривенно в дозах, подобранных по АЧТВ, показал, что ГНМВ столь же эффективны в лечении и предупреждении рецидивов ТГВ/ТЭЛА как и НФГ, но реже вызывают геморрагические осложнения [11]. Это открыло путь к успешному изучению лечения неосложненных ТГВ и субмассивной ТЭЛА в амбулаторных условиях. Подтверждено превосходство ГНМВ над НФГ (доказана эффективность для надропарина кальция (фраксипарина) и эноксапарина натрия (клексана), что улучшает качество жизни больных и снижает стоимость лечения [12]. Однако у лиц с массивной ТЭЛА и высоким риском кровотечений (пожилой возраст, недавнее хирургическое вмешательство, кровотечения в анамнезе, заболевания почек и печени) данный вариант терапии не приемлем [5].
При использовании гепаринов более 5–7 сут возможно развитие гепарининдуцированной тромбоцитопении, которая обычно развивается между 3-м и 15-м днями после начала лечения, с частотой в среднем 2,4% при терапевтическом применении гепарина и 0,3% при назначении его с профилактической целью.
Необходимо подозревать гепарининдуцированную тромбоцитопению всякий раз, когда у пациента развиваются необычные изменения в клинико-лабораторных показателях в течение или вскоре после терапии гепарином. К таковым относятся: уменьшение количества тромбоцитов менее 100 000 в 1 мкл либо на 50% и более от исходного уровня на 5–10-е сутки от начала введения гепарина.
Оральные антикоагулянты-антивитамины К (ОАК–АВК). Для предотвращения дальнейшего увеличения размеров тромба и вторичных тромбоэмболических осложнений применяются ОАК–АВК. В зависимости от химической структуры молекулы антикоагулянта различают производные монокумарина и дикумарина, циклокумарины и индандионы.
Наиболее широко в мире применяются производные монокумарина — варфарин (кумадин) и аценокумарол (синтром, никумадин, синкулар), что обусловлено их оптимальной продолжительностью действия и хорошей переносимостью. Варфарин является препаратом выбора, так как время его нахождения в организме больного обеспечивает более стабильное воздействие на процесс свертывания крови, чем во время терапии аценокумаролом. Назначение весьма популярных в России фенилина и пелентана ограничивается токсичностью первого и неустойчивым антикоагулянтным эффектом второго (табл. 5).
При использовании ОАК для предупреждения рецидива ВТЭ его дозу рекомендуется подбирать таким образом, чтобы поддерживать значение Международного нормализованного отношения (МНО) на уровне 2,0–3,0 [13]. Терапия варфарином в период ее проведения редуцирует риск ретромбозов на 90–95% [14]. ОАК обычно назначается пациентам с ВТЭ одновременно с гепаринами непосредственно после эпизода тромбообразования. При достижении уровня МНО более 2,0 гепарин можно отменить.
Терапию ОАК рекомендуется начинать с поддерживающих доз: 2,5–5 мг для варфарина, 0,75–3 мг для маркумара, 1–4 мг для синкумара. Более низкие стартовые дозы показаны лицам старше 60 лет, уроженцам Азии, в особенности лицам китайского происхождения, пациентам с нарушением функции почек и печени, артериальной гипертензией, застойной сердечной недостаточностью, а также при сопутствующей терапии препаратами, усиливающими антикоагулянтный эффект ОАК.
Перед приемом препарата необходимо оценить общий анализ крови, протромбиновое время, АЧТВ, общий анализ мочи, определить функциональное состояние печени и почек. При рецидивирующем венозном тромбозе целесообразно провести скрининг на предмет тромбофилий. Среди наследственных факторов наиболее распространенными являются: генетическая мутация фактора V свертывания крови (фактор V Лейдена), мутация 20210А гена протромбина, а также мутация гена метилентетрагидрофолатредуктазы, приводящая к развитию гипергомоцистеинемии. Препарат принимается 1 раз в день в фиксированное время после еды. Контроль МНО проводится через 10–12 ч после приема препарата. На протяжении первой недели определение МНО рекомендуется производить ежедневно, затем 1 раз в неделю. Следует подчеркнуть, что расчет МНО производится в плазме, т. е. в венозной крови.
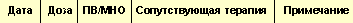 |
| Таблица 6. Дневник приема ОАК |
Перед началом терапии больному необходимо разъяснить особенности антикоагулянтной терапии ОАК. Пациент должен вести дневник по приведенному образцу (табл. 6), в котором отмечаются значения МНО, доза принимаемого препарата, сопутствующая терапия. Пациент должен сообщать врачу о любых заболеваниях, возникших во время лечения ОАК–АВК. Врачу рекомендуется вести специальную форму, в которой целесообразно записывать показания, по которым производится прием ОАК–АВК, планируемые значения МНО, предполагаемая продолжительность терапии, факторы риска кровотечения.
В таблице 7 приведен алгоритм подбора дозы в начале лечения варфарином [15]. Тактика лечения иными ОАК должна быть аналогичной под контролем МНО.
 |
| Таблица 7. Алгоритм стартового лечения варфарином |
После достижения необходимого уровня МНО алгоритм дальнейшего наблюдения должен быть следующим: первое определение МНО — через 5–10 дней, второе — через 2 нед, третье — через 3 нед, четвертое и все последующие — через 4 нед.
После диагностики тромбоза при определении длительности применения ОАК должны учитываться причины и выраженность тромбофилического состояния. Согласно существующим рекомендациям, терапия ОАК должна составлять не менее 3 мес у больных с симптоматическим тромбозом на фоне очевидных «обратимых» факторов, провоцирующих гиперкоагуляцию (травмы, операции и др.). Пациенткам с венозными тромбозами, возникшими на фоне гормональной заместительной терапии, лицам с «синдромом экономического класса» терапия продлевается до полугода. Не менее 1 года должны получать превентивное лечение ОАК пациенты со спонтанным венозным тромбозом [17, 18]. Больные с рецидивирующими венозными тромбозами, рецидивирующими тромбозами на фоне выявленных генетических тромбофилий нуждаются в постоянном приеме ОАК. Пациентам без эпизодов ВТЭ в прошлом, но с подтвержденным гетерозиготным дефицитом протеинов С и S, антитромбина III, с мутацией факторов V Лейден или протромбина G20210A некоторые специалисты [19] рекомендуют профилактическое назначение антикоагулянтов только при наличии выраженных приобретенных факторов риска тромбообразования, например при подготовке к оперативным вмешательствам. Такое лечение, по сообщениям этих авторов, предупреждает половину возможных тромбозов.
Применение ОАК при инвазивных процедурах. У пациентов группы низкого риска тромбоэмболий (венозный тромбоз более чем 3 мес назад, неосложненная системными тромбоэмболиями мерцательная аритмия) терапия ОАК прекращается за 3–4 дня до операции до достижения значений МНО менее 1,5. Если операция сопровождается риском тромбозов, кратковременно показаны профилактические дозы гепаринов, затем возобновление терапии ОАК.
У пациентов группы среднего риска тромбоэмболий ОАК отменяются за 4 дня до операции до достижения МНО 1,5. За 2 дня до операции назначаются либо низкие дозы НФГ (5000 ЕД подкожно) либо профилактические дозы ГНМВ. После операции — низкие дозы НФГ (или ГНМВ) и затем ОАК.
У пациентов группы высокого риска тромбоэмболий (венозный тромбоз менее 3 мес назад, рецидивы венозного тромбоза в анамнезе, протезы клапанов сердца в митральной позиции) ОАК отменяются за 4 дня до операции до достижения МНО 1,5. За 2 дня до операции назначаются терапевтические дозы гепаринов. Гепарины отменяются за 12–24 ч до операции.
Пациентам, у которых возникает необходимость удаления зуба, перед процедурой необходимо определить значения МНО. Если показатели остаются в пределах терапевтических значений, то процедуру можно проводить без коррекции терапии. Если значения МНО превышают 3,5, нужно пропустить один-два приема препарата. Следующие стоматологические процедуры не требуют коррекции дозы ОАК: пломбировка, установка коронки, мостов, чистка канала, снятие зубного камня [20].
Литература
Т. В. Козлова, доктор медицинских наук, доцент
Т. В. Таратута, кандидат медицинских наук
ММА им. И. М. Сеченова, Москва
Чем повысить ачтв в крови у женщин
Активированное частичное тромбопластиновое время, или АЧТВ, – время, за которое образуется сгусток крови после присоединения к плазме хлорида кальция и других реагентов. Оно отражает работу так называемого внутреннего пути и общего каскада свертывающей системы крови человека и является наиболее чувствительным показателем свертываемости крови.
Активированное парциальное тромбопластиновое время, кефалин-каолиновое время.
Синонимы английские
Partial Thromboplastin Time (PTT), Activated Partial Thromboplastin Time, aPTT, APTT.
Метод детекции бокового светорассеяния, определение процента по конечной точке.
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Активированное частичное тромбопластиновое время (АЧТВ) характеризует внутренний путь свертывания крови. АЧТВ представляет собой время, за которое формируется сгусток в образце плазмы крови, после добавления к ней специальных активаторов этого процесса. Таким образом оценивается степень воздействия факторов свертывания крови на образование тромба.
Продолжительность АЧТВ зависит от уровня высокомолекулярного кининогена, прекалликреина и факторов свертывания XII, XI, VIII и менее чувствительно при изменениях количества факторов X, V, протромбина и фибриногена. АЧТВ определяют по длительности образования кровяного сгустка после добавления в пробу крови кальция и парциального тромбопластина. Увеличение длительности АЧТВ связано с повышенным риском кровотечений, уменьшение – с тромбозом. Данный показатель отдельно используют для контроля терапии прямыми антикоагулянтами (гепарином).
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
Увеличение АЧТВ указывает на склонность к кровотечению: свертывание крови длится дольше обычного, что часто говорит о недостаточности одного из коагуляционных факторов или о воздействии какого-либо ингибитора на способность организма к тромбообразованию.
Что может влиять на результат?
Тест АЧТВ

Сдать тест АЧТВ и получить достоверные результаты с расшифровкой анализа можно в Лаборатории патологий гемостаза в МЖЦ, – базовой клинике МГМУ им. Сеченова.
Стоимость исследования на АЧТВ*
Расчет стоимости лечения Все цены
* Принимаются пациенты старше 18 лет.
Когда назначают АЧТВ-тест
АЧТВ входит в состав анализов крови на гемостаз, которые сдают при планировании беременности. Тест назначают и при генетической расположенности к тромбозам, спонтанных кровотечениях неясного генеза, диагностике гемофилии, лечении инфаркта, в ходе пред- и послеоперационных обследований.
По результатам анализа определяют наличие ингибиторов свертывания – признаков системной красной волчанки и антифосфолипидного синдрома, тяжелых аутоиммунных патологий. Также АЧТВ-тест используют с целью контроля гепариновой терапии.
Специалисты
врач-гемостазиолог, кандидат медицинских наук
акушер-гинеколог, гемостазиолог, кандидат медицинских наук
Преимущества анализа
АЧТВ – узконаправленное исследование, диагностирующее несколько патологий гемостаза. Коагуляционный механизм гемостаза обеспечивает «запечатывание» повреждений в сосудах фибриновыми сгустками и подвержен влиянию факторов свертывания крови.
При помощи АЧТВ-теста можно обнаружить дефицит основных факторов, влияющих на свертываемость:
Как сдают тест АЧТВ
Кровь сдают до полудня, натощак. За день до исследования следует прекратить прием медикаментозных препаратов, влияющих на свертываемость крови, отказаться от жирной пищи и алкоголя.
Кровь для анализа берут из вены, добавляют в нее антикоагулянт (цитрат натрия), активатор (каолин), фосфолипиды и хлорид кальция. Результаты исследования выдают на следующий рабочий день после сдачи крови.
Расшифровка
За норму по тесту принимают 24-35 секунд. В организме будущих мам происходят физиологические изменения гемостаза, поэтому показатель АЧТВ при беременности снижен до 17-20 секунд. Тип патологии определяют, основываясь на укорочении или удлинении АЧТВ.
Что значит, если АЧТВ выше нормы
Удлинение АЧТВ является признаком дефицита факторов свертывания крови: 8-го при гемофилии А, 9-го при гемофилии В, 11-го при гемофилии С, а также болезни Виллебранда – унаследованной склонности к спонтанным кровотечениям.
При повышении маркера проводят дополнительные тесты на волчаночный антикоагулянт и антифосфолипидный синдром, а если пациент получает инъекции гепарина – корректируют дозу препарата.
Что значит, если АЧТВ ниже нормы
Укорочение активированного частичного тромбопластинового времени свидетельствует о риске развития тромбозов – закупорки сосудов, или тромбоэмболии – отрыва тромба и попадания его в циркулирующую кровь. По низкому АЧТВ определяют первую фазу диссиминированного внутрисосудистого свертывания.
При неправильном заборе венозной крови, загрязнении пробы также наблюдается снижение маркера – в таких случаях анализ делают повторно.
Где сдать анализ на АЧТВ в Москве
Сдать АЧТВ-тест и получить консультацию опытного гемостазиолога можно в Медицинском Женском Центре на Земляном валу. Наша Лаборатория патологий гемостаза располагает высокоточными анализаторами крови, качественными реактивами и расходными материалами, что гарантирует достоверность результатов исследования.
Вместе с АЧТВ-тестом, у вас есть возможность сдать близкие к нему анализы: 2-ТЭГ, расширенную гемостазиограмму, тесты на ВА и АФС, Антитромбин, а также определить анти-Ха активность гепарина в крови. В экспериментальной лаборатории МЖЦ занимаются не только диагностикой: мы исследуем и практикуем новые методики лечения гематологических заболеваний.
В одной из частных лабораторий вы еще одна статистическая единица, а у нас – пациент, которому готовы помочь лучшие доктора Москвы.