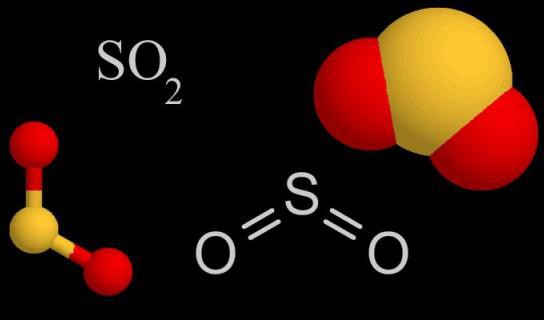
Сернистый газ — физические свойства, получение и применение
Сернистый газ имеет молекулярное строение, аналогичное озону. Атом серы, находящийся в центре молекулы, связан с двумя атомами кислорода. Этот газообразный продукт окисления серы не имеет цвета, издает резкий запах, при изменении условий легко конденсируется в прозрачную жидкость. Вещество хорошо растворимо в воде, обладает антисептическими свойствами. В больших количествах получают SO2 в химической промышленности, а именно в цикле сернокислотного производства. Газ широко используется для обработки сельскохозяйственных и пищевых продуктов, отбеливания тканей в текстильной промышленности.
Систематические и тривиальные названия вещества
Необходимо разобраться в многообразии терминов, относящихся к одному и тому же соединению. Официальное название соединения, химический состав которого отражает формула SO2, — диоксид серы. ИЮПАК рекомендует использовать этот термин и его английский аналог — Sulfur dioxide. Учебники для школ и ВУЗов чаще упоминают еще такое название — оксид серы (IV). Римской цифрой в скобках обозначена валентность атома S. Кислород в этом оксиде двухвалентен, а окислительное число серы +4. В технической литературе используются такие устаревшие термины, как сернистый газ, ангидрид сернистой кислоты (продукт ее дегидратации).
Состав и особенности молекулярного строения SO2
Молекула SO2 образована одним атомом серы и двумя атомами кислорода. Между ковалентными связями имеется угол, составляющий 120°. В атоме серы происходит sp2-гибридизация — выравниваются по форме и энергии облака одного s и двух p-электронов. Именно они участвуют в образовании ковалентной связи между серой и кислородом. В паре О—S расстояние между атомами составляет 0,143 нм. Кислород более электроотрицательный элемент, чем сера, значит, связывающие пары электронов смещаются от центра к внешним углам. Вся молекула тоже поляризована, отрицательный полюс — атомы О, положительный — атом S.
Некоторые физические параметры диоксида серы
Оксид четырехвалентной серы при обычных показателях окружающей среды сохраняет газообразное агрегатное состояние. Формула сернистого газа позволяет определить его относительную молекулярную и молярную массы: Mr(SO2) = 64,066, М = 64,066 г/моль (можно округлять до 64 г/моль). Этот газ почти в 2,3 раза тяжелее воздуха (М(возд.) = 29 г/моль). Диоксид обладает резким специфическим запахом горящей серы, который трудно перепутать с каким-либо другим. Он неприятный, раздражает слизистые покровы глаз, вызывает кашель. Но оксид серы (IV) не такой ядовитый, как сероводород.
Под давлением при комнатной температуре газообразный сернистый ангидрид сжижается. При низких температурах вещество находится в твердом состоянии, плавится при –72…–75,5 °C. При дальнейшем повышении температуры появляется жидкость, а при –10,1 °C вновь образуется газ. Молекулы SO2 являются термически устойчивыми, разложение на атомарную серу и молекулярный кислород происходит при очень высоких температурах (около 2800 ºС).
Растворимость и взаимодействие с водой
Диоксид серы при растворении в воде частично взаимодействует с ней с образованием очень слабой сернистой кислоты. В момент получения она тут же разлагается на ангидрид и воду: SO2 + Н2О ↔ Н2SO3. На самом деле в растворе присутствует не сернистая кислота, а гидратированные молекулы SO2. Газообразный диоксид лучше взаимодействует с прохладной водой, его растворимость понижается с повышением температуры. При обычных условиях может раствориться в 1 объеме воды до 40 объемов газа.
Сернистый газ в природе
Значительные объемы диоксида серы выделяются с вулканическими газами и лавой во время извержений. Многие виды антропогенной деятельности тоже приводят к повышению концентрации SO2 в атмосфере.
Сернистый ангидрид поставляют в воздух металлургические комбинаты, где не улавливаются отходящие газы при обжиге руды. Многие виды топливных ископаемых содержат серу, в результате значительные объемы диоксида серы выделяется в атмосферный воздух при сжигании угля, нефти, газа, полученного из них горючего. Сернистый ангидрид становится токсичным для человека при концентрации в воздухе свыше 0,03 %. У человека начинается одышка, могут наступить явления, напоминающие бронхит и воспаление легких. Очень высокая концентрация в атмосфере диоксида серы может привести к сильному отравлению или летальному исходу.
Сернистый газ — получение в лаборатории и в промышленности
3. При взаимодействии меди с концентрированной серной кислотой выделяется не водород, а диоксид серы:
Современные способы промышленного производства сернистого ангидрида:
Основные химические свойства диоксида серы
Сернистый газ является активным соединением в химическом плане. В окислительно-восстановительных процессах это вещество чаще выступает в качестве восстановителя. Например, при взаимодействии молекулярного брома с диоксидом серы продуктами реакции являются серная кислота и бромоводород. Окислительные свойства SO2 проявляются, если пропускать этот газ через сероводородную воду. В результате выделяется сера, происходит самоокисление-самовосстановление: SO2 + 2H2S = 3S + 2H2O.
Процесс окисления серы в диоксиде до шестивалентного состояния в ангидриде серной кислоты — каталитический. Получившееся вещество энергично растворяется в воде, реагирует с молекулами Н2О. Реакция является экзотермической, образуется серная кислота, вернее, ее гидратированная форма.
Практическое использование сернистого газа
Основной способ промышленного производства серной кислоты, для которого нужен диоксид элемента, насчитывает четыре стадии:
Ранее почти всю двуокись серы, необходимую для производства серной кислоты в промышленных масштабах, получали при обжиге пирита как побочный продукт сталеплавильного производства. Новые виды переработки металлургического сырья меньше используют сжигание руды. Поэтому основным исходным веществом для сернокислотного производства в последние годы стала природная сера. Значительные мировые запасы этого сырья, его доступность позволяют организовать широкомасштабную переработку.
Диоксид серы находит широкое применение не только в химической промышленности, но и в других отраслях экономики. Текстильные комбинаты используют это вещество и продукты его химического взаимодействия для отбеливания шелковых и шерстяных тканей. Это один из видов бесхлорного отбеливания, при котором волокна не разрушаются.
Диоксид серы обладает отличными дезинфицирующими свойствами, что находит применение в борьбе с грибками и бактериями. Сернистым ангидридом окуривают хранилища сельскохозяйственной продукции, винные бочки и подвалы. Используется SO2 в пищевой промышленности как консервирующее и антибактериальное вещество. Добавляют его в сиропы, вымачивают в нем свежие плоды. Сульфитизация
сока сахарной свеклы обесцвечивает и обеззараживает сырье. Консервированные овощные пюре и соки тоже содержат диоксид серы в качестве антиокислительного и консервирующего агента.
Диоксид серы (Е220)

Применение диоксида серы в производстве продуктов
Зачем добавляют диоксид серы в процессе производства разнообразной продукции.
Е220 (диоксид серы) активно применяют в производстве мясных изделий, а также в процессе заготовок фруктов и овощей, в процессе производства разнообразных напитков, в том числе вина. Производство вин – это самая популярная сфера применения диоксида серы. В процессе производства мясных изделий Е220 используют для обработки мяса – предотвращает появление на сырье бактерий. Сульфиты обладают незначительным побочным действием – они не допускают изменения цвета мяса, и покупатели не могут подлинно оценить свежесть продукта. В процессе заготовок фруктов и овощей консервант Е220 применяют с целью промежуточного консерванта, им обрабатывают фрукты и овощи до непосредственной переработки. Следовательно, после переработки в готовой продукции будет содержаться минимум Е220 и бактерий. Сернистая кислота часто используется для обработки сухофруктов, с целью лучшей сохранности и приобретения товарного вида.
Перед непосредственной транспортировкой практически все виды цитрусовых обрабатываются данным консервантом. Также стоит помнить, что процесс производства разнообразных безалкогольных напитков и пива, тоже не обходится без использования сернистого ангидрида.
Применение консерванта в производстве соков не допускает развития в процессе хранения плесени и уксуснокислых бактерий.
Диоксид серы в качестве профилактического средства активно используется для обработки складов с фруктами и овощами, для чистки емкостей, используемых для хранения разнообразных напитков и вин.

Диоксид серы в вине
О том, что диоксид серы активно используют в процессе приготовления вин, знает, наверное, каждый, и в этом нет ничего удивительного. На сегодняшний день только в дорогостоящих, так называемых биодинамических винах, нет сульфитов. Вино без диоксида серы более дорогостоящее и обладает меньшим сроком годности. По каким причинам есть Е220 в вине? Применение консерванта на первоначальных процессах позволяет предотвратить процессы окисления, стабилизируя микрофлору сусла. Если использовать данную добавку в допустимых нормах, неблагоприятного влияния на организм она оказывать не будет. По каким-то причинам многие любители вин уверены, что головную боль, появляющуюся после употребления данного напитка, провоцирует именно консервант Е220. Данную теорию можно считать верной только тогда, если в процессе производства напитка было использовано большую дозу консерванта.
Сегодня норма диоксида серы в вине составляет триста миллиграмм на одну тысячу миллилитров вина. Те производители, которые ставят перед собой цель, удовлетворить потребителя, стараются в свою продукцию добавлять максимум двести/двести пятьдесят миллиграмм консерванта на килограмм.
Диоксид серы не оказывает влияние на вкусовые качества напитка.
Диоксид серы – вред
Ни от кого не скрывается тот факт, что Е220 (сернистый газ) – это соединение химического типа с третьим классом опасности. Давайте подробнее рассмотрим влияние на человека консерванта Е220. У людей, которые максимально чувствительны к разнообразным консервантам, при употреблении большой дозировки или при частом употреблении продуктов с наличием Е220 могут проявиться самые разнообразные побочные эффекты, среди которых стоит отметить: тяжесть в желудке, мигрень, диарею, замедление речи, насморк аллергический, отек легких в острой стадии, тошноту, головокружение, сильный аллергический кашель, удушье, рвоту с желчью и т.д. Консервант диоксид серы обладает еще одним достаточно серьезным побочным эффектом – это разрушение белков и витамина В1 в организме.
Людям, страдающим астмой, нужно максимально осторожно подбирать продукты с содержанием сульфитов, а также продукты, которые были предварительно данным консервантом обработаны, так как данное химическое соединение может спровоцировать появление серьезных аллергических реакций. Следует, непосредственно перед совершением покупки максимально внимательно изучить этикетку, в особенности обратить внимание на состав от производителя. Перед употреблением обработанных сульфидами фруктов, овощей или сухофруктов их необходимо тщательно промыть под проточной водой. После положить в емкость с водой (девяносто пять-сто градусов по Цельсию) и продержать там от пяти до десяти минут. Именно используя горячую воду можно быстро и без дополнительных затрат провести процедуру десульфитации (очень часто данный метод используют на производстве). Существует масса (норма) количества диоксида серы (с учетом часто употребляемых продуктов) – сто миллиграмм на килограмм продукта (норма суточная). Если не превышать указанную норму, негативное влияние на организм человека Е220 оказывать не будет.
Диоксид серы: опасное вещество или полезная добавка?
Покупатели часто спрашивают нас о таком веществе, как диоксид серы — главным образом потому, что он почти всегда указывается в составе вина, как консервант. Людей интересует, зачем он нужен в напитке, вреден ли он? Тема «диоксида серы» на самом деле очень интересна, особенно учитывая, что он встречается также в сухофруктах, соках, лимонадах, изделиях из картофеля и других продуктах. Маркируется вещество кодом Е220.
Диоксид серы с точки зрения химии 
Для консервирования вина сернистый газ использовали еще в древней Греции — горящей серой окуривали изнутри амфоры, в которые потом наливали вино. Интересно, что и в наше время один из способов получения SO2 — такое же сжигание серы, как и многие века назад. Другой способ — обжиг сульфидных руд. Очистка газа производится путем его сжижения или поглощением холодной водой, а затем десорбцией при нагреве.
Свойства диоксида серы

Небольшое количество диоксида серы — от 40 до 200 мг/л, не вызывает гибель культурных дрожжей, «отвечающих» за преобразование виноградного сока в вино, тогда как уксуснокислые бактерии и вызывающие плесень грибки замедляют рост или погибают. Все это делает сернистый ангидрид консервантом, особенно востребованным именно в виноделии. О том, что без его применения сложно сделать качественные и обладающие большим потенциалом хранения вина, писал еще знаменитый химик Луи Пастер, посвятивший виноделию несколько серьезных исследований. Интересно, что лучшего консерванта для вина, чем диоксид серы, не сегодняшний день так и не придумали.
Так вреден ли диоксид серы для человека?
Только в больших количествах, а также аллергикам и астматикам. Вещество разрушает В1 и дисульфидные мостики в белках, что, естественно, вредит здоровью. Легкое отравление двуокисью серы может вызвать насморк, кашель, першение в горле, хрипоту, боль в животе, расстройство пищеварения, головную боль.
В случае более сильного отравление возможны затруднения речи, глотания и дыхания, рвота и отек легких. Правда, отравиться диоксидом серы, содержащимся в вине или пищевых продуктах, не аллергику и не астматику сложно — его используют в чрезвычайно малом количестве, не оказывающем негативного влияния на здоровье. Если же вдруг вы купили некачественное вино или еду, в которой количество сернистого ангидрида превышает допустимые нормы, вы почувствуете резкий запах серы. В этом случае продукт лучше не употреблять.
Есть мнение, что именно от диоксида серы в вине после употребления этого напитка может болеть голова. Это неверно. Точнее, готова от диоксида может болеть только у аллергиков, а у остальных от вина голова болит по другим причинам. Это доказывает хотя бы тот факт, что, например, в 100 гр сушеной кураги содержится в разы больше SO2, чем в таком же количестве вина, но от кураги голова обычно не болит.
Еще один факт: вин без сернистого ангидрида не бывает! Даже так называемые органические и биодинамические вина, зачастую производящиеся вообще без добавок, содержат его в минимальном количестве, так как он вырабатывается в процессе дрожжевого брожения.
Вывод: диоксид серы помогает сохранить свежими и внешне привлекательными многие продукты и напитки. В качественных продуктах его настолько мало, что он не может нанести вред здоровому, не страдающему аллергией или астмой человеку.
Как сернистый газ может повлиять на человека
Совсем недавно я рассказывала про наши возмутительные кислотные дожди, от которых нет спасенья. А сегодня хочу подробнее остановиться на их компонентах, то есть газах, которые влияют на кислотность дождей. Как я уже говорила, основные компоненты – это два оксида серы, их часто называют сернистый газ и серный газ.
Давайте рассмотрим их по очереди.
Газ номер 1
Итак, у сернистого газа, как и у многих химических веществ типа соды и галуберовой соли, есть много названий:
Это бесцветный газ с резким запахом. Для тех, кому нужны подробности насчет запаха – зажгите спичку и сразу же понюхайте (будьте осторожны!): то, что вы почувствуете – и есть запах образующегося оксида серы (IV). Кстати, кто жжет спички в туалете, знайте, что избавлением от «туалетного» запаха вы обязаны именно оксиду серы (IV).
Естественно, это вещество ядовито. Признаков отравления несколько:
В общем, все то, что жители нашего многострадального города знают не понаслышке.
Ну а если говорить о совсем уж больших концентрациях, то они приводят к удушью, отеку легких и смерти.
Где мы с ним встречаемся
В природе этот газ встречается, в основном, как один из компонентов вулканических газов. А в жизни человека – как продукт сжигания топлива (например, угля для ТЭЦ), в состав которого входит сера, либо как продукт переработки руды, содержащей серу. Именно поэтому чаще всего страдают от диоксида серы города с металлургическими предприятиями.
Попробую объяснить на совсем простом примере.
Вы ездите на машинах, автобусах, электричках – все это сделано из железа. А вы не задумывались, откуда оно берется? В чистом виде оно в природе существует в мизерном количестве, которого не хватит для всего мира. Поэтому его нужно выплавлять из минералов, руды.
Например, есть железосодержащая руда под названием пирит – это вещество, которое состоит из железа и серы. Для получения железа пирит обжигают, сера и железо переходят в соединения с кислородом, которые и отправляются на дальнейшую переработку. Вот так и получается, что оксид серы – это результат металлургических процессов.
В дальнейшем его улавливают насколько это возможно, так как это довольно ценный продукт и разбрасываться им – экономически невыгодно. И то, что уловили, отправляют на получение серной кислоты, без которой многие химические производства просто не смогут работать. Именно поэтому ее называют «хлебом» химической промышленности.
Естественно, я объясняю все максимально упрощенно, так что, если среди вас, мои читатели, есть профессиональные химики или металлурги, то прошу не кидать в меня тапками
Едем дальше. Дымит завод, производит железо и прочие металлы. Попутно улавливает оксиды серы, но что-то уловить не получается по разным причинам (от экономии на фильтрах до элементарной халатности), поэтому часть их мы получаем в виде бонуса: хочешь – бери, не хочешь – все равно бери. Либо дыши, либо ходи под кислотным дождем.
Об этом я уже писала, повторяться не буду. Хочу рассказать о некоторых интересных и полезных моментах использования сернистого ангидрида. А вы думали, что кроме вреда от него совсем нет пользы? Зря. Смотрите, где его применяют.
Применение
Во-первых, в производстве серной кислоты, архи необходимой почти всей химической промышленности.
Во-вторых, им окуривают склады и овощехранилища, чтобы избавиться от вредных бактерий. Кстати, я вспоминаю, как когда-то давно мои родители жгли в погребе чистую серу именно для того, чтобы избавиться от плесени. Помогло, кстати.
Сжиганием серы, кстати, раньше часто окуривали виноградники, именно чтобы избавиться от всяких паразитов. Как сейчас с этим, честно скажу, не знаю. Кто в курсе – напишите в комментариях, делают так сейчас или нашли уже какой-то другой способ.
Также им вместо хлора отбеливают шерсть, так как хлор просто разрушит ее. Это же касается и натурального шелка.
Ну а самое интересное, на мой взгляд, а для многих, и злободневное – это использование в качестве консерванта (Е220), так как тот газ обладает отличными бактерицидными свойствами.
Самый распространенный потребитель сернистого газа – винодельческая промышленность. Его добавляют в вина, чтобы стабилизировать нежелательные окислительные процессы, ну и заодно избавиться от вредных микроорганизмов. Это же касается и пива.
Кроме того, это вещество используется как консервант на промежуточных стадиях получения джемов, фруктовых и ягодных пюре. Естественно, все это нормируется ГОСТами. Например, на 1 литр вина допускается не более 300 мг сернистого газа.
В свежевыжатые соки также добавляют сернистый газ – он тормозит развитие болезнетворных бактерий и предотвращает уксусное брожение и образование плесени.
Практически не обходится без обработки сернистым ангидридом и производство сухофруктов – они лучше хранятся и имеют более аппетитный товарный вид.
В мясном производстве это вещество также хорошо зарекомендовало себя как успешный борец с вредными бактериями. Правда, тут есть еще один нюанс – обработанное им мясо выглядит ярким, свежим, что может ввести покупателя в заблуждение.
Именно поэтому в некоторых странах сейчас запрещают использование этого консерванта для мяса – так как это может попасть под статью о фальсификации товара.
В общем если подвести итог применения сернистого газа как консерванта, то вот список продуктов, в которых он чаще всего используется:
Вот такое интересное вещество. Не только вред, но и польза.
Газ номер 2
Еще одно интересное вещество, которое влияет на кислотность дождей, это «брат» сернистого газа – серный газ. Обратите внимание на названия: сернИСТый и серный. Это не одно и тоже. Поэтому если слышите, что какой-то журналист пытается рассказать об этих двух газах как об одном, знайте, что вам просто морочат голову. Не давайте себя запутать.
Кстати, в отличие от сернистого, словосочетание «серный газ» употребляется редко. Чаще все же говорят «серный ангидрид». Вот еще названия:
В отличие от своего «младшего брата» это уже не газ, а легко летучая жидкость с не менее резким запахом. Также токсичное вещество.
Это уже – продукт химической промышленности, чисто рукотворное вещество. Основное его применение – получение серной кислоты. Кроме того, частично этот оксид может, как и предыдущий, образовываться при сжигании серы (если вы вдруг решите провести обеззараживание помещения таким способом). Правда, его в данном случае образуется совсем немного.
Для химиков это вещество очень интересно и полезно, так как является очень гигроскопичным (то есть сильно впитывает в себя влагу). Ну а для всех остальных – просто знайте, что это – основное вещество, из которого делают серную кислоту.
Как вам сегодняшняя статья? Знаю, что не-химики часто приходят в ужас от разных химических названий и, особенно, формул. Так что я постаралась рассказывать максимально упрощенно. Просто для того, чтобы «знать врага в лицо» и не бояться его – ничего страшного в этом нет.
Если вам интересно еще о чем-то узнать, пишите в комментариях, я всегда отвечу.
Внимание! Сейчас участились комментарии, которые я удаляю и не отвечаю на них. Поэтому обращаю ваше внимание на Правила комментирования, ссылка на которые указана красными буквами возле поля ввода комментария. Это чтобы не было негодующих вопросов о том, почему я не отвечаю на некоторые вопросы.
Что еще я хотела сказать?
Поздравляю всех с началом лета и с прошедшим вчера Днем эколога. Иногда его еще называют День защиты окружающей среды. Ну а себя поздравляю с Днем рождения моего сына, ему вчера исполнилось пять лет
Всем хорошего настроения и солнечной погоды!