Аримидекс®
Инструкция
Торговое название
Международное непатентованное название
Лекарственная форма
Таблетки, покрытые оболочкой, 1 мг
Состав
Одна таблетка содержит
вспомогательные вещества: лактозы моногидрат, повидон, натрия крахмала гликолят, магния стеарат, вода очищенная,
состав оболочки: макрогол 300, гипромеллоза, титана диоксид (Е 171).
Описание
Таблетки круглой формы, двояковыпуклые, покрытые оболочкой белого цвета, с гравировкой А (оканчивающаяся справа стрелкой) на одной стороне и Adx 1 на другой.
Фармакотерапевтическая группа
Противоопухолевые препараты. Гормонов антагонисты. Ферментов ингибиторы.
Фармакологические свойства
Фармакокинетика
Всасывание анастрозола быстрое, максимальная концентрация в плазме достигается в течение 2 часов после приема внутрь (натощак).
Пища незначительно уменьшает скорость всасывания, но не его степень, и не приводит к клинически значимому влиянию на равновесную концентрацию препарата в плазме при однократном приёме суточной дозы Аримидекса®. Анастразол выводится медленно, период полувыведения из плазмы составляет 40-50 часов.
Равновесная плазменная концентрация анастрозола приблизительно от 90 до 95% достигается через 7 дней применения.
Фармакокинетика анастрозола не зависит от возраста у женщин в постменопаузе.
У мальчиков с пубертатной гинекомастией анастрозол всасывается быстро, выводится медленно с периодом полувыведения около 2 дней. Фармакокинетические параметры у мальчиков сопоставимы с таковыми у женщин в постменопаузе. Клиренс анастрозола у девочек ниже, чем у мальчиков, а воздействие больше. Период полувыведения анастрозола у девочек составляет приблизительно 0,8 дней.
Связь с белками плазмы крови – 40 %.
Анастразол экстенсивно метаболизируется у женщин в постменопаузе. С мочой выделяется менее 10 % дозы в неизмененном виде в течение 72 часов после приема препарата. Метаболизм анастрозола осуществляется N-деалкилированием, гидроксилированием и глюкуронизацией. Метаболиты выводятся преимущественно с мочой. Триазол, основной метаболит, определяемый в плазме и моче, не ингибирует ароматазу.
Клиренс анастрозола после перорального приема при циррозе печени или нарушении функции почек не изменяется.
Фармакодинамика
Аримидекс® не обладает прогестагенной, андрогенной и эстрогенной активностью.
Аримидекс® в суточных дозах до 10 мг не оказывает эффекта на секрецию кортизола и альдостерона, следовательно, при применении Аримидекса® не требуется заместительного введения кортикостероидов.
Показания к применению
— адъювантная терапия раннего гормоноположительного рака молочной железы у женщин в постменопаузе
— лечение распространенного рака молочной железы у женщин в постменопаузе
— адъювантная терапия раннего гормоноположительного рака молочной железы у женщин в постменопаузе после терапии тамоксифеном в течение 2-3 лет
Способ применения и дозы
Взрослые, включая пожилых:
по 1 мг внутрь 1 раз в сутки.
Почечная и печеночная недостаточность: коррекция дозы не требуется.
Побочные действия
— сухость влагалища, влагалищные кровотечения (в основном в течение первых недель после смены предшествующей гормональной терапии на Аримидекс®)
— выпадение волос (алопеция)
— синдром запястного канала (в основном наблюдается у пациенток с факторами риска к данному заболеванию)
— увеличение активности АЛТ, АСТ и щелочной фосфатазы
— увеличение активности гамма-глутамилтрансферазы и уровня билирубина
— гиперкальциемия (возможно увеличение уровня паратиреозного гормона)
— синдром щелкающего пальца
— кожный васкулит (включая некоторые случаи пурпуры Шенлейна-Геноха)
В таблице ниже представлена частота возникновения нежелательных явлений, предварительно указанных в ходе исследования приема Аримидекса® и Тамоксифена по отдельности или совместно, после промежуточного наблюдения через 68 месяцев, независимо от причинной связи, и выявленных у пациенток, получающих экспериментальное лечение и в течение 14 дней после окончания экспериментального лечения.
Таблица 2.Нежелательные явления, предварительно указанные в ходе исследования приема Аримидекса® и Тамоксифена по отдельности или совместно
Боли в суставах\тугоподвижность суставов
Переломы позвонков, шейки бедра или костей запястья
Переломы костей запястья или костей запястья/ лучевой кости
Переломы шейки бедра
Болезнь коронарных артерий
Любое венозное тромбоэмболичеcкое осложнение
Хронические венозные тромбоэмболические осложнения, включая эмболию легких
Ишемические цереброваскулярные нарушения
После промежуточного наблюдения через 68 месяцев частота возникновения переломов составила 22 на 1000 пациенто-лет и 15 на 1000 пациенто-лет в группах, принимающих Аримидекс® и тамоксифен соответственно. Наблюдаемая частота возникновения переломов у пациенток, принимавших Аримидекс® не выходит за рамки пределов, заявленных для соответствующей возрастной группы пациенток в постменопаузе. Частота возникновения остеопороза составила 10,5% у пациентов принимавших Аримидекс® и 7.3% у пациентов принимавших Тамоксифен.
Не было определено, отражает ли частота возникновения переломов и остеопороза, выявленная у пациентов, принимавших Аримидекс®, в ходе исследования приема Аримидекса® и Тамоксифен по отдельности или совместно защитный эффект тамоксифен, специфическое действие Аримидекса® и то и другое.
Противопоказания
— повышенная чувствительность к анастрозолу или другим вспомогательным компонентам препарата
— беременность и период лактации
— у женщин в пременопаузе
— выраженная почечная недостаточность (клиренс креатинина менее 20 мл/мин)
— умеренная или выраженная недостаточность функции печени (безопасность и эффективность не установлена)
— сопутствующая терапия тамоксифеном и/или терапия эстрогенсодержащими препаратами
— детский и подростковый возраст до 18 лет (безопасность и эффективность у детей не установлена)
Лекарственные взаимодействия
Ферменты, обуславливающие метаболизм анастрозола выявлены не были. Циметидин, являющийся слабым неспецифическим ингибитором ферментов системы цитохрома Р450, не оказывает влияния на концентрации анастрозола в плазме. Влияние сильных ингибиторов цитохрома Р450 неизвестно.
Обзор базы данных по безопасности, полученных в ходе клинических исследований, не выявил сведения, подтверждающие наличие клинически значимого взаимодействия у принимавших Аримидекс® пациенток, которые дополнительно получали другие обычно назначаемые лекарственные препараты. Также не были выявлены клинически значимые взаимодействия с биcфосфонатами.
Следует избегать совместного приема Аримидекса® с тамоксифеном или одновременного назначения терапии с применением эстрогена, поскольку это может ослаблять фармакологическое действие Аримидекса®.
Особые указания
Снижая уровень циркулирующего эстрадиола, Аримидекс® может вызывать снижение минеральной плотности костной ткани с последующим увеличением возможности переломов костей. Данное возможное повышение риска переломов костей должно контролироваться в соответствии со стандартными рекомендациями по лечению и контролю состояния костной системы у женщин в постменопаузе в менопаузе в начале лечения и регулярно после его окончания. При необходимости, следует начать и тщательно отслеживать лечение или профилактику остеопороза. Дальнейшую потерю минеральной плотности костной ткани, вызванную приемом Аримидекса®, у женщин в постменопаузе может остановить специфическое лечение, например, назначение бисфосфонатов (см. раздел «Побочные действия»). В случае сомнений по поводу наступления менопаузы ее следует определять с
помощью биохимического анализа (уровни лютеинизирующего гормона (ЛГ), фолликулостимулирующего гормона (ФСГ) и/или эстрадиола). Данные в поддержку применения Аримидекса ®с аналогами рилизинг-фактора лютеинизирующего гормона отсутствуют.
Следует избегать совместного приема Аримидекса с тамоксифеном или одновременного назначения терапии с применением эстрогена, поскольку это может ослаблять фармакологическое действие Аримидекса®.
При применении Аримидекса® чаще, чем при терапии тамоксифеном, наблюдались ишемические заболевания, однако статистической значимости при этом не отмечено.
Эффективность и безопасность применения Аримидекса® в пременопаузе не изучались.
Исследования влияния Аримидекса® при приеме пациентками, страдающими раком молочной железы с умеренной или тяжелой печеночной недостаточностью не проводились. Пациенткам с умеренной и тяжелой печеночной недостаточностью следует принимать Аримидекс® с осторожностью. Лечение должно быть основано на соотношении пользы и риска для каждой конкретной пациентки.
Исследования влияния Аримидекса® при приеме пациентками, страдающими раком молочной железы, с тяжелой почечной недостаточностью не проводились (СКФ
Аримидекс (анастразол, веро-анастразол)
Ответы на частозадаваемые вопросы. Данный документ не является заменой для инструкции к препарату. Препарат нельзя назначать самостоятельно. Данный препарат назначает только врач.
Что такое аримидекс?
Каков механизм действия аримидекса?
Аримидекс (анастрозол) блокирует действие фермента, который синтезирует эстрадиол (женский половой гормон) — ароматазу. Известно, что после окончания менструаций, функция яичников прекращается, и они перестают выделять эстрадиол. Функцию выделения женских половых гормонов после окончания менструаций берут на себя надпочечники (располагаются над почками). Надпочечники относятся к эндокринной системе организма.
Аримидекс (анастрозол, веро-анастразол) использует один из основных методов гормонотерапии — снижение уровня эстрадиола (женский половой гормон). Известно, что аримидекс снижает уровень эстрадиола на 80%.
Почему так важен низкий уровень эстрадиола (женского полового гормона)?
Почему аримидекс (анастрозол,веро-анастразол) используется у женщин только при прекращении менструального цикла?
Аримидекс (анастрозол, веро-анастразол) не блокирует выделение женских половых гормонов яичниками, поэтому у женщин с сохраненной менструальной функцией он бесполезен.
Усиливает ли аримидекс действие тамоксифена?
Несмотря на то, что препараты имеют разнонаправленное действие, эффективность друг друга они не усиливают. Эффективность тамоксифена такая же как схема «тамоксифен + аримидекс (анастрозол)».
Показания к назначению аримидекса
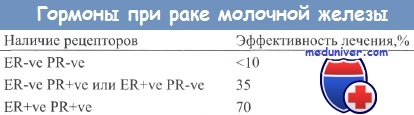
Аримидекс используется только при наличии чувствительности опухоли к гормонотерапии (положительные рецепторы к эстрогенам и прогестерону ), у женщин в менопаузе в следующих случаях:
Противопоказания
Побочные эффекты
Со стороны эндокринной системы: приливы, сухость влагалища, истончение волос.
Со стороны пищеварительной системы: снижение аппетита, тошнота и рвота, понос, незначительный подъем уровня холестерина и др.
Со стороны нервной системы: сонливость, головная боль
Со стороны кожи: сыпь
Другие: слабость, снижение подвижности в суставах,
Чем аримидекс отличается от тамоксифена?
Аримидекс отличается механизмом действия и, конечно же, меньшим объемом побочных эффектов. Аримидекс не вызывает повышение риска развития рака матки, не вызывает повышение риска развития тромбов в венах (основные осложнения тамоксифена). В целом количество осложнений у аримидекса меньше, чем у тамоксифена.
Чем аримидекс отличается от фемары (экстразы, летрозола)?
Практически отличий между аримидексом и фемарой (экстраза, летрозол) нет. Механизм действия этих препаратов одинаков.
Дмитрий Андреевич Красножон, специально для сайта «Все о раке молочной железы» (www.breast-cancer.ru). Последняя редакция 12 декабря 2014 года
Copyright © Д.А.Красножон, 2008-2022. Копирование материалов разрешено только с указанием авторства
Аримидекс или анастрозол что лучше
Выбор гормонов для лечения метастазов рака молочной железы
В большинстве случаев обследования больных с локализованными опухолями приходит к выводу, что болезнь носит преимущественно системный характер, и метастазы разовьются позже. Обнаружение многочисленных метастазов, часто спустя годы после проведения мастэктомии, а также в течение многолетнего наблюдения за больными подтверждает этот вывод.
По данным классических исследований Бринкли и Хейбитл, общая выживаемость больных раком молочной железы через 25 лет после лечения составляет только 20%. Даже среди пациенток, которым мастэктомия была сделана своевременно («ранние» операбельные случаи), выживаемость составляет лишь 30%.
Обычно появление метастазов приводит к смертельному исходу в пределах трех лет, хотя в случаях, когда лечение оказывается эффективным, пациентки могут жить дольше. Вероятность метастазирования опухоли сильно зависит от степени вовлечения подмышечных лимфатических узлов в патологический процесс, что определяется при гистологическом анализе образцов, взятых во время операции.
Существует взаимосвязь между количеством пораженных подмышечных лимфатических узлов и вероятностью распространения метастазов.
Со времени проведения первой операции терапевтической овариэктомии, проведенной Битсоном в 1896 г., стало очевидно, что при изменении гормонального статуса организма в случаях распространенного опухолевого процесса, по крайней мере для одной трети пациенток достигается симптоматический эффект.
Использовались различные методы: удаление яичников или их облучение (иногда называемое «создание искусственной менопаузы»), лечение эстрогенами, антиэстрогенами и антагонистами гонадотропин-рилизинг-гормона (например, гозерелином). Этот гормон регулирует секрецию лютеинизирующего гормона (LHRH).
Также применяли анаболические стероиды, глюкокортикоиды и прогестерон, проводили удаление надпочечников или гипофиза и назначали ингибиторы ароматазы (анастрозол или летрозол).
Стандартный подход основан на менструальном статусе пациентки. Для большинства больных с метастазирующими опухолями в пременопаузе и перименопаузе используется хирургическое удаление яичников или их облучение. Однако с появлением антагонистов гонадотропин-рилизинг-гормона эти процедуры стали применять реже.
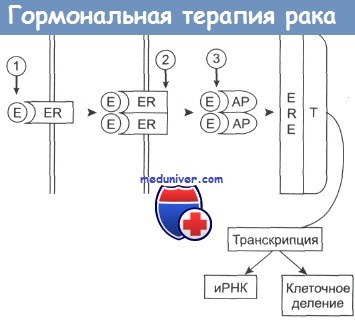
Комплекс приобретает активность (АР) и присоединяется к эстроген-зависимым структурам (ERE) клеточного ядра.
Происходит активация таких белков, участвующих в транскрипции (Т), как РНК-полимераза II, что приводит к синтезу белка и делению клетки.
Гозерелин вызывает снижение уровня эстрогенов в плазме крови (1); фульвестран (2) предотвращает процесс димеризации рецептора и его активацию; тамоксифен (3) связывается с активным комплексом, подавляя его способность инициировать транскрипцию.
Антагонисты обеспечивают стойкое снижение уровня эстрогенов и вызывают у пациентки состояние менопаузы, которое длится в продолжении примерно двух месяцев с начала применения гозерелина. Препарат назначается ежемесячно в виде внутримышечных инъекций. Вместе с тем в качестве альтернативы снова стал популярным такой хирургический метод, как лапароскопическое удаление яичников.
Это достаточно безопасная и несложная операция, после которой пациентка на одну ночь остается в стационаре. Следует отметить, что перед операцией больные проходят тщательный отбор по критерию гормональной чувствительности опухоли, и тем, для кого не предполагается проявление лечебного эффекта, операция не проводится.
Для пациенток с опухолью в постменопаузе широко применяется тамоксифен, поскольку он практически не проявляет побочных эффектов. Препарат действует как антиэстроген, но, вероятно, оказывает и прямой цитотоксический эффект. В течение почти 20 лет тамоксифен использовался в качестве стандартного препарата адъювантной терапии.
Тамоксифен назначается перорально в ежедневной стандартной дозе 20 мг. Он обладает медленным кумулятивным действием. Побочные эффекты редки, однако могут наблюдаться приливы, тошнота, гиперкальциемия, тромбоцитопения, удержание жидкости и расстройство менструального цикла. После приема препарата большинство пациенток прибавляют 1-2 фунта в весе и некоторые отмечают ухудшение состояния кожи, волос и ногтей.
Гораздо более существенный эффект получен при назначении гормонотерапии пациенткам с гормонально зависимыми опухолями, в то время как при лечении гормонально независимых опухолей благоприятный эффект наблюдался лишь в редких случаях. Прогноз в случаях гормонально зависимых и независимых опухолей отличается. Для больных с гормонально-зависимыми опухолями характерен более длительный безрецидивный период и большая выживаемость.
Совместное определение показателей ER и PR обеспечивает более точный прогноз в отношении чувствительности опухоли к гормонотерапии, чем это оказывается возможным при оперировании только показателем ER. Больные с PR-положительными опухолями также характеризуются более длительным безболезненным периодом.
На эффективность гормонотерапии сильно влияет характер распространения метастазов. Костные метастазы проявляют некоторую чувствительность к гормонам, хотя после лечения пациентки живут в среднем около 12-15 месяцев. Тем не менее некоторые больные с гормоночувствительными опухолями и с костными метастазами живут дольше, иногда несколько лет.
В большинстве случаев, при рецидиве опухоли, развившейся в пременопаузе, применяется гозерин (или его аналоги) или лапароскопическая овариэктомия (или облучение яичников). Эти меры эффективны для гормонально чувствительных опухолей. При опухолях в периоде постменопаузы обычно назначают тамоксифен, если пациентки раньше не получали этот препарат в качестве средства адъювантной терапии.
В любом случае можно ожидать, что выживаемость больных составит по крайней мере 30%. Экзогенные гормоны назначают до тех пор, пока не наступит эффект. В дальнейшем гормональную терапию продолжают только тем пациенткам, у которых проявился эффект первичного лечения. Предложены новые противоопухолевые препараты, относящиеся к группе ингибиторов ароматазы.
К числу их относится анастрозол, который блокирует биосинтез предшественников эстрогенов и их последующие превращения в тканях. Анастрозол действует при пероральном применении. Он хорошо переносится больными, так же как и другие родственные соединения, благодаря чему эти препараты быстро заняли место тамоксифена, который оказался неэффективным в лечении пациенток с гормонозависимыми опухолями, развивающимися в период постменопаузы. Рекомендуемая ежедневная доза препарата составляет 1 мг.
Если после первичного лечения возникает рецидив, то назначают другие препараты, например анаболические стероиды, прогестогены и глюкокортикоиды. Анаболические стероиды более эффективны у пациенток с опухолями, развившимися в постменопаузе, и, по-видимому, их особенно необходимо применять в случаях обнаружения костных метастазов.
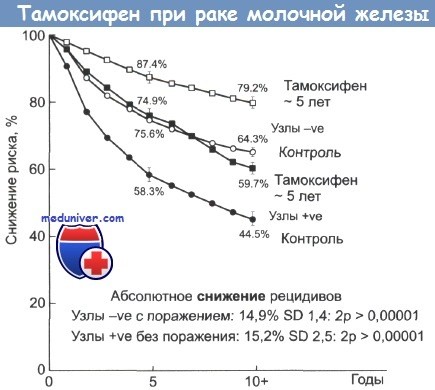
Светлые значки — пациентки без признаков поражения лимфатических узлов; затемненные значки — пациентки с признаками поражения лимфоузлов.
Благоприятный эффект достигается примерно у 20% пациенток, однако недостатком применения стероидов является вирилизация. Удобным для применения является нандролон деканоат (Deca-Durabolin), который назначается в виде внутримышечных инъекций в дозе 50-100 мг каждые 3-4 недели. Если гормонотерапия раньше давала положительные результаты, то можно применять прогестогены. Наиболее часто используется ацетат медроксипрогестерона (МРА, Provera), который обычно назначают перорально в дозе 100 мг три раза в день.
Однако его применение ограничено из-за развития побочного эффекта — прибавления в весе. Такой же эффективностью обладает другое производное прогестерона — мегестрол-ацетат (Megace).
Широко обсуждается вопрос выбора метода лечения первого рецидива опухоли. Следует в этом случае использовать гормональный метод или же химиотерапию с использованием цитотостатиков? Если принимать во внимание количественные показатели, то выбирать надо между гормонотерапией (эффективна в 30% случаев) и комбинационной химиотерапией (эффективность которой в два раза выше). Однако это упрощенное решение вопроса, ответить на который на самом деле сложно.
Реакция опухоли на гормоны обычно носит более продолжительный характер, и у пациентки наблюдаются минимальные токсические проявления. При химиотерапии развивается более кратковременный эффект, который сопровождается токсическими и психологическими осложнениями. Большинство клиницистов в Великобритании в качестве средства первичного лечения предпочитают использовать гормональную терапию. Выбор облегчается все более широким применением метода анализа состояния рецепторов эстрогенов: гормональная терапия должна проводиться только среди пациенток с ER-положительными опухолями. Недавно предложен препарат фульвестрант (Faslodex), подавляющий функции рецепторов эстрогенов. Он может применяться у пациенток с гормоноустойчивыми опухолями, которые развились в постменопаузе. Одним из основных преимуществ этого препарата, по сравнению с агонистом эстрогенов, тамоксифеном, является отсутствие побочных эффектов. Он также не опустошает пул эстрогенов в женском организме, что происходит при применении ингибиторов ароматазы.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Аримидекс : инструкция по применению
Состав
действующее вещество: anastrozole ;
1 таблетка, покрытая оболочкой, содержит 1 мг анастрозола;
вспомогательные вещества: лактоза моногидрат, повидон, натрия крахмала (тип А), магния стеарат пленочная оболочка: гипромеллоза, макрогол 300, титана диоксид (Е 171).
Лекарственная форма
Таблетки, покрытые пленочной оболочкой.
Основные физико-химические свойства: круглые, белые, двояковыпуклые таблетки, покрытые пленочной оболочкой. Таблетки выгравированы.
Фармакологическая группа
Антагонисты гормонов и родственные средства. Ингибиторы ароматазы. Код АТХ. L02B G03.
Фармакологические свойства
Механизм действия и фармакодинамические эффекты
Аримидекс является мощным и Высокоизбирательно нестероидным ингибитором ароматазы. У женщин в постменопаузе эстрадиол в основном продуцируется путем преобразования в периферических тканях андростендиона в эстрон с помощью комплекса фермента ароматазы. Эстрон далее превращается в эстрадиол. Снижение уровня эстрадиола оказывает терапевтический эффект у женщин, больных раком молочной железы. У женщин в постменопаузе прием Аримидексу в суточной дозе 1 мг приводил к снижению уровня эстрадиола на 80%, что было подтверждено высокочувствительным аналитическим тестом.
Аримидекс не имеет прогестагенной, андрогенной или эстрогенной активности.
Клиническая эффективность и безопасность
Распространенный рак молочной железы
Терапия первой линии для женщин в постменопаузе с распространенным раком молочной железы
Два двойных слепых контролируемых клинических исследования с подобным дизайном (исследование 1033IL / 0030 и исследования 1033IL / 0027) проводились с целью оценки эффективности Аримидексу сравнению с тамоксифеном как препаратом первой линии для лечения местно-распространенного или метастатического рака молочной железы с положительными или неизвестными показателями рецепторов гормонов у женщин в постменопаузе. В общем 1021 пациентку были рандомизированы для применения Аримидексу в дозе 1 мг один раз в сутки или тамоксифена в дозе 20 мг один раз в сутки. Главными конечными результатами в обоих исследованиях были время до прогрессирования опухоли, частота объективного ответа опухоли и безопасность.
Оценка главных конечных показателей исследования 1033IL / 0030 продемонстрировала, что Аримидекс имел статистически значимое преимущество над тамоксифеном по времени до прогрессирования опухоли (отношение рисков (ОР) 1,42; 95% доверительный интервал (ДИ) [1,11; 1,82], медиана времени до прогрессирования 11,1 и 5,6 месяцев для Аримидексу и тамоксифена соответственно, р = 0,006) частота объективного ответа опухоли была одинаковой для Аримидексу и тамоксифена. Исследование 1033IL / 0027 продемонстрировало, что частота объективного ответа опухоли и время до прогрессирования опухоли для Аримидексу и тамоксифена были подобными. Оценка вторичных конечных показателей подтвердила оценку главных конечных показателей эффективности. Достаточно низкий уровень смертности в группах лечения обоих исследований не позволил сделать выводы о различиях показателей общей выживаемости.
Терапия второй линии для женщин в постменопаузе с распространенным раком молочной железы
Аримидекс изучался в ходе двух контролируемых клинических исследований (исследование 0004 и исследования 0005) с участием женщин в постменопаузе с распространенным раком молочной железы, у которых заболевание прогрессировало после лечения тамоксифеном распространенного рака молочной железы или рака молочной железы на ранней стадии. В общем 764 пациентки были рандомизированы для применения Аримидексу в дозе 1 мг или 10 мг один раз в сутки или мегестрол ацетата в дозе 40 мг четыре раза в сутки. Время до прогрессирования и частота объективного ответа были основными показателями эффективности. Также определяли частоту случаев пролонгированного (более 24 недель) стабильного заболевания, частоту прогрессирования и общую выживаемость. В обоих исследованиях значимых различий между группами лечения по любому из параметров эффективности выявлено не было.
Присадка лечения инвазивного рака молочной железы с положительными показателями рецепторов гормонов на ранних стадиях
В ходе крупного исследования ИИИ фазы проводилось с участием 9366 женщин в постменопаузе с операбельным раком молочной железы, которых лечили в течение 5 лет (см. Ниже), Аримидекс статистически преобладал тамоксифен относительно показателя выживаемости без болезни. Значительно большие преимущества по сравнению с показателем выживаемости без болезни наблюдались в пользу Аримидексу сравнению с тамоксифеном в проспективное определенной популяции с положительными показателями рецепторов гормонов.
Суммарная таблица конечных показателей, полученных в ходе исследования АТАС: анализ после завершения лечения, длившегося 5 лет
Аримидекс (Arimidex) инструкция по применению
Владелец регистрационного удостоверения:
Произведено:
Первичная упаковка:
Упаковано:
Вторичная упаковка:
Контакты для обращений:
Лекарственная форма
Форма выпуска, упаковка и состав препарата Аримидекс
| 1 таб. | |
| анастрозол | 1 мг |
Вспомогательные вещества: лактозы моногидрат, повидон, карбоксиметиленкрахмал натрия, магния стеарат, вода очищенная.
Состав оболочки: макрогол 300, гипромеллоза, титана диоксид, вода очищенная.
Фармакологическое действие
Аримидекс не обладает прогестагенной, андрогенной и эстрогенной активностью.
Аримидекс в суточной дозе до 10 мг не оказывает эффекта на секрецию кортизола и альдостерона (следовательно, при применении препарата не требуется заместительного введения кортикостероидов).
Фармакокинетика
После приема внутрь анастрозол быстро всасывается из ЖКТ. C max в плазме достигается в течение 2 ч (натощак). Пища несколько уменьшает скорость, но не степень всасывания. Небольшие изменения скорости всасывания не приводят к клинически значимому влиянию на С ss препарата в плазме при ежедневном приеме 1 таб. Аримидекса.
Анастрозол связывается с белками плазмы на 40%. Приблизительно 90-95% от С ss достигается после 7 дней приема препарата. Нет сведений о кумуляции препарата и зависимости фармакокинетических параметров анастрозола от времени и дозы.
Анастрозол метаболизируется путем N-деалкилирования, гидроксилирования и глюкуронизации. Триазол, основной метаболит, определяемый в плазме, не ингибирует ароматазу.
Фармакокинетика в особых клинических случаях
Определяемый клиренс анастрозола после перорального приема у добровольцев со стабилизированным циррозом печени или нарушением функции почек не отличается от клиренса, определяемого у здоровых добровольцев.
Фармакокинетика анастрозола не зависит от возраста у женщин в постменопаузе.
Показания препарата Аримидекс
Режим дозирования
Пациентам с легкими и умеренно выраженными нарушениями функции почек не требуется коррекции дозы.
Пациентам с легкими нарушениями функции печени не требуется коррекции дозы.
Таблетку следует проглотить целиком и запить водой. Рекомендуется принимать препарат в одно и то же время суток.
Побочное действие
Противопоказания к применению
Препарат не назначают женщинам в пременопаузе.
Применение при беременности и кормлении грудью
Препарат противопоказан к применению при беременности и в период лактации (грудного вскармливания).
Применение при нарушениях функции печени
Пациентам с легкими нарушениями функции печени не требуется коррекции дозы.
Противопоказан при умеренной или выраженной печеночной недостаточности (безопасность и эффективность не установлены).
Применение при нарушениях функции почек
Пациентам с легкими и умеренно выраженными нарушениями функции почек не требуется коррекции дозы.
Противопоказан при почечной недостаточности тяжелой степени (клиренс креатинина менее 20 мл/мин).
Применение у детей
Особые указания
У женщин с рецептор-отрицательной опухолью к эстрогенам эффективность Аримидекса не была продемонстрирована, кроме тех случаев, когда имелся предшествующий положительный клинический ответ на тамоксифен.
В случае сомнений в гормональном статусе пациентки менопауза должна быть подтверждена определением половых гормонов в сыворотке крови.
Нет данных о безопасности применения Аримидекса у пациентов с выраженными нарушениями функции печени или у пациентов с почечной недостаточностью тяжелой степени (КК менее 20 мл/мин).
В случае сохраняющегося маточного кровотечения на фоне приема Аримидекса необходима консультация и наблюдение гинеколога.
Препараты, содержащие эстрогены, не следует назначать одновременно с Аримидексом.
Снижая уровень циркулирующего эстрадиола, Аримидекс может вызывать снижение минеральной плотности костной ткани.
У пациенток с остеопорозом или с риском развития остеопороза минеральная плотность костной ткани должна оцениваться методом денсиометрии (например, DEXA сканированием) в начале лечения и в динамике. При необходимости должны быть начаты лечение или профилактика остеопороза под тщательным наблюдением врача.
Нет данных об одновременном применении анастрозола и препаратов аналогов ГнРГ.
Неизвестно, улучшает ли анастрозол результаты лечения при совместном использовании с химиотерапией.
Данные по безопасности при длительном лечении анастрозолом пока не получены.
При применении Аримидекса чаще, чем при терапии тамоксифеном, наблюдались ишемические заболевания, однако статистической значимости при этом не отмечено.
Эффективность и безопасность Аримидекса и тамоксифена при их одновременном применении вне зависимости от статуса гормональных рецепторов сравнимы с таковыми при использовании одного тамоксифена. Точный механизм данного явления пока не известен.
Использование в педиатрии
Безопасность и эффективность применения препарата у детей не установлены.
Влияние на способность к управлению транспортными средствами и механизмами
Некоторые побочные эффекты Аримидекса, такие как астения и сонливость, могут отрицательно влиять на способность к выполнению работы, требующей повышенной концентрации внимания и быстроты психомоторных реакций. В связи с этим рекомендуется при появлении этих симптомов соблюдать осторожность при управлении автомобилем или движущимися механизмами.
Передозировка
Описаны единичные клинические случаи передозировки препарата. Разовая доза Аримидекса, при которой развиваются угрожающие жизни симптомы, не установлена.
Лечение: специфического антидота не существует. При необходимости проводят симптоматическую терапию: индуцирование рвоты (если больной в сознании), общая поддерживающая терапия, наблюдение за больным и контроль за функцией жизненно важных органов и систем. Возможно проведение диализа.
Лекарственное взаимодействие
Клинические исследования по лекарственному взаимодействию с антипирином и циметидином указывают на то, что совместное введение Аримидекса с другими препаратами вряд ли приведет к клинически значимому взаимодействию, обусловленному цитохромом P450.
Клинически значимое лекарственное взаимодействие при приеме Аримидекса одновременно с другими часто назначаемыми препаратами отсутствует.
На данный момент нет сведений о применении Аримидекса в комбинации с другими противоопухолевыми препаратами.
Препараты, содержащие эстрогены, не следует назначать одновременно с Аримидексом, т.к. они уменьшают фармакологическое действие последнего.
Не следует назначать тамоксифен одновременно с Аримидексом, поскольку он может ослабить фармакологическое действие последнего.
Условия хранения препарата Аримидекс
Список Б. Препарат следует хранить в недоступном для детей месте при температуре не выше 30°C.
Сравнительная оценка фармацевтического качества препаратов анастрозола
Полный текст:
Аннотация
Ключевые слова
Раскрытие информации о конфликте интересов:
Авторы заявляют об отсутствии конфликта интересов.
Информация о статье:
Депонировано (дата): 05.06.2018
Все авторы прочитали и одобрили окончательную рукопись статьи.
Информация о рецензировании:
«Качественная Клиническая Практика» благодарит анонимного рецензента (рецензентов) за их вклад в рецензирование этой работы.
Комментарий редакции:
В случае возникновения разночтений в тексте или расхождений в форматировании между pdf-версией статьи и её html-версией приоритет отдаётся pdf-версии.
Для цитирования:
Белоусов Ю.Б., Соколов А.В., Зырянов С.К., Лелишенцев А.А., Камаев А.В., Зверков Ю.Б. Сравнительная оценка фармацевтического качества препаратов анастрозола. Качественная Клиническая Практика. 2010;(1):16-21.
ВВЕДЕНИЕ
Рак молочной железы (РМЖ) в настоящее время – это наиболее часто диагностируемое онкологическое заболевание у женщин в Европе и США. Предполагается, что за период с 2001 по 2010 год будет выявлено 5 миллионов новых случаев этого заболевания. К сожалению, несмотря на все достижения в диагностике и лечении РМЖ, более 50% пациентов погибают от распространённого РМЖ. Большая часть опухолей молочной железы имеет рецепторы к эстрогенам и, соответственно, рост этих опухолей может быть стимулирован эстрогенами. У женщин в постменопаузе основным источником циркулирующих эстрогенов является андростендион, синтезируемый надпочечниками. В периферических тканях (например, в жировой ткани) при участии фермента ароматазы он превращается в эстрон и в дальнейшем, в эстрадиол [1].
Таким образом, лечение гормонозависимых опухолей молочной железы должно быть направлено на снижение уровня эстрогенов, что может произойти вследствие овариоэктомии у женщин в пременопаузе или использования антиэстрогенных препаратов как в пре-, так и в постменопаузе.
Первые представители класса ингибиторов ароматазы не нашли достаточно широкого применения в медицинской практике вследствие неселективности своего действия и необходимости парентерального введения. Ситуация с использованием препаратов, обладающих сходным механизмом, изменилась с появлением нового нестероидного ингибитора ароматазы анастрозола. Препарат не обладает прогестогенной, андрогенной и эстрогенной активностью. В суточных дозах до 10 мг анастрозол не оказывает влияния на секрецию кортизола и альдостерона, следовательно, при применении анастрозола не требуется заместительного введения кортикостероидов.
Анастрозол применяется при адъювантном лечении ранних стадий эстроген-положительного РМЖ, а также для лечения распространённого РМЖ у женщин в постменопаузе.
В проведённых клинических исследованиях установлено, что эффективность анастрозола прямо коррелирует с принимаемой дозой. Так, в исследовании фармакокинетики, проведённом на здоровых женщинах с сохранённой репродуктивной функцией, показано, что изменение синтеза гормонов гипофиза при применении данного препарата происходит практически линейно при эскалации принимаемой дозы с 5 до 20 мг [2].
Аналогичные зависимости установлены во влиянии приёма препарата на уровень сывороточного эстрадиола у женщин в постменопаузе. Чрезвычайно важным является тот факт, что снижение уровня циркулирующего эстрадиола отмечалось только на 6 день от начала приёма анастрозола. Таким образом, можно полагать, что одним из факторов, обусловливающих эффективность проводимой терапии, является кумулятивная доза препарата.
В исследовании, проведённом с участием 14 женщин в постменопаузе, у которых диагностированы распространённые формы РМЖ с наличием рецепторов к эстрогенам, было установлено, что применение анастрозола сопровождается снижением концентрации эстрогенов и внутри опухоли. Через 15 недель приёма анастрозола оказалось, что внутриопухолевые концентрации эстрадиола, эстрона и эстрона сульфата достигли значений в 11,1, 16,7 и 26,6%, соответственно, от базового уровня. У трёх пациенток уровень перечисленных гормонов был ниже предела детекции [3]. Нельзя не отметить, что анастрозол обладает достаточно благоприятным профилем безопасности. Из неблагоприятных побочных реакций, которые развиваются часто, можно отметить «приливы» жара, артралгию, сухость влагалища. Приём препарата может вызвать снижение минеральной плотности костной ткани в связи со снижением уровня циркулирующего эстрадиола, тем самым, повышая риск возникновения остеопороза и перелома костей.
Учитывая высокую эффективность препарата в лечении РМЖ, становится понятным интерес фармацевтических компаний к производству генерических копий анастрозола. По данным на 10.02.2010 г., в РФ зарегистрированы 1 оригинальный препарат и 3 воспроизведённых препарата анастрозола [4]. Учитывая растущую обеспокоенность пациентов, широкой медицинской общественности, регуляторных органов, связанную с зачастую неудовлетворительной клинической эффективностью при применении генериков, было решено провести выборочный сравнительный фармакохимический анализ лекарственных форм анастрозола различных производителей с целью изучения их фармацевтической эквивалентности.
Для достижения цели были поставлены следующие задачи:
В качестве объектов исследования были избраны лекарственные препараты анастрозола, выпускаемые различными производителями: «Аримидекс» – таблетки, покрытые плёночной оболочкой, №28, содержащие активное вещество анастрозол в количестве 1 мг, производства компании «АстраЗенека Фармасьютикалс ЛП.», США; «Анастера®» – таблетки, покрытые плёночной оболочкой, №28, содержащие активное вещество анастрозол в количестве 1 мг, производства компании «Лаборатория Блипак С.А.», Аргентина; «Веро-Анастрозол®» – таблетки, покрытые плёночной оболочкой, №28, содержащие активное вещество анастрозол в количестве 1 мг, производства компании ОАО «Верофарм», Россия.
Все выбранные образцы были закуплены в розничной аптечной сети в количестве, достаточном для проведения данного исследования в соответствии с требованиями Государственной Фармакопеей (ГФ).
Проведённые исследования выполнены сотрудниками Испытательной лаборатории ООО «Национальное агентство клинической фармакологии и фармации» в полном соответствии с требованиями нормативной документации и требованиями ГФ выпуск XI, с использованием современного оборудования.
Объекты исследования
1. Таблетки «Аримидекс®», покрытые оболочкой, №28, 1 мг производства компании «АстраЗенека Фармасьютикалс ЛП.», США. Серия: DF 960, произведены: 02 2006, годен до: 02 2011.
Состав: 1 таблетка, покрытая оболочкой содержит:
активное вещество: анастрозол 1 мг;
вспомогательные вещества: лактозы моногидрат, повидон, карбоксиметилен крахмал натрия, магния стеарат, вода очищенная
состав оболочки: макропол 300, гипромеллоза, титана диоксид, вода очищенная.
2. Таблетки «Анастера®», покрытые плёночной оболочкой, №28, 1 мг, производства компании «Лаборатория Блипак С.А.», Аргентина. Серия: ANO12A, произведены: 05/09/08, годен до: 09/2010.
Состав: 1 таблетка, покрытая плёночной оболочкой содержит:
активное вещество: анастрозол 1 мг;
вспомогательные вещества: лактозы моногидрат, крахмал кукурузный, повидон (поливинилпирролидон К-30), карбоксиметилкрахмал натрия, магния стеарат, опадрай II белый, гипролоза (гидроксипропилцеллюлоза) 28-40%, лактозы моногидрат 21-40%, макропол (полиэтиленгликоль 4000) 8-14%, титана диоксид (Е171) 20-30%.
3. Tаблетки «Веро-Анастрозол®», покрытые плёночной оболочкой, №28, 1 мг, производства компании ОАО «Верофарм», Россия. Серия: произведены: 10808, годен до: IX 10.
Состав: 1 таблетка, покрытая плёночной оболочкой, содержит:
активное вещество: анастрозол 1 мг;
вспомогательные вещества: крахмал кукурузный, лактоза (сахар молочный), повидон (поливинилпирролидон), карбоксиметилкрахмал натрия (прмогель), магния стеарат,
состав оболочки: гипромеллоза (гидроксипропилметилцеллюлоза), повидон (поливинилпирролидон), полисорбат (твин-80), тальк (магния гиброкси-силикат), титана диоксид.
Представленные образцы были исследованы на соответствие требованиям нормативной документации (НД), причём, для корреляции полученных данных, исследования проводили по НД фирмы производителя и разработчика данного препарата – компании «АстраЗенека Фармасьютикалс ЛП.», США.
Результаты и обсуждение
Исследование представленных на анализ образцов на подлинность подтверждалась методом высокоэффективной жидкостной хроматографии (ВЭЖХ) по сопоставлению на хроматограммах времен удерживания анастрозола стандартного и испытуемого растворов.
Определение средней массы и отклонений в массе проводили по методике и в соответствии с требованиями ГФ XI, вып. 2, стр. 156. Результаты данного теста представлены в табл. 1.
Таблица 1. Результаты определения средней массы таблеток и отклонения от средней массы
Объект
Средняя масса
20 таблеток, мг
Отклонение в массе отдельных таблеток, мг
Сравнительный фармакоэкономический анализ применения анастрозола, летрозола и экземестана при адъювантной терапии рака молочной железы
Полный текст:
Аннотация
Актуальность. В данной статье отражены результаты анализа эффективности затрат, сравнивающего альтернативные схемы гормональной терапии рака молочной железы (РМЖ) ингибиторами/инактиваторами ароматазы. Цель: сравнительная фармакоэкономическая оценка терапии анастрозолом, летрозолом и экземестаном пациенток с I–II стадиями РМЖ в условиях российской системы здравоохранения. Методология: Марковское моделирование, анализ эффективности затрат. Результаты. При анализе эффективности затрат инициальной адъювантной терапии при РМЖ наиболее экономически эффективным препаратом является летрозол. При анализе эффективности затрат при переключении с продолжением терапии тамоксифеном при РМЖ наиболее экономически эффективным препаратом является экземестан. Вывод. Все три препарата: анастрозол, летрозол и экземестан более чем в 2 раза меньше установленного «порога готовности платить», поэтому могут быть рекомендованы для включения в список ЖНВЛП (кроме анастрозола, который уже присутствует там) и для применения в системе государственного возмещения.
Ключевые слова
Раскрытие информации о конфликте интересов:
Авторы заявляют об отсутствии конфликта интересов.
Информация о статье:
Депонировано (дата): 06.06.2018
Все авторы прочитали и одобрили окончательную рукопись статьи.
Информация о рецензировании:
«Качественная Клиническая Практика» благодарит анонимного рецензента (рецензентов) за их вклад в рецензирование этой работы.
Комментарий редакции:
В случае возникновения разночтений в тексте или расхождений в форматировании между pdf-версией статьи и её html-версией приоритет отдаётся pdf-версии.
Для цитирования:
Белоусов Д.Ю., Афанасьева Е.В., Зырянов С.К. Сравнительный фармакоэкономический анализ применения анастрозола, летрозола и экземестана при адъювантной терапии рака молочной железы. Качественная Клиническая Практика. 2012;(2):45-55.
Введение
Рак молочной железы (РМЖ) – занимает первое место среди злокачественных новообразований у женщин и является одной из главных причин смертности женского населения во всём мире. Заболеваемость РМЖ увеличивается с возрастом. Как правило, опухоли возникают после 35-40 лет, пик заболеваемости регистрируют у женщин в возрасте 60-65 лет [14].
В России в структуре заболеваемости злокачественными новообразованиями РМЖ занимает 1-ое место (18,1%). Распространённость РМЖ в 2011 г. на 100 000 населения – 369,5 человек. В 2011 г. выявлено 57 379 больных РМЖ женщин, из них 55 184 поставлено на учёт. Удельный вес больных с диагнозом, подтверждённым морфологически, от числа больных с впервые в жизни установленным диагнозом РМЖ – 96,6%. Удельный вес больных с опухолевым процессом I стадии от числа больных с впервые в жизни установленным диагнозом РМЖ – 18,5%, II стадии – 46,5%, III стадии – 24,8%, IV стадии – 9,1% [19].
Радикальное лечение РМЖ получило 36 469 женщин [19], в том числе:
Пятилетняя выживаемость в 2011 г. составила 57,6%. Индекс накопления контингентов больных с РМЖ – 9,5. Одногодичная летальность с момента установления РМЖ – 8,7% [19].
Как уже было сказано выше, среди женщин с впервые выявленным РМЖ в 65% случаев диагностируют I-II стадии заболевания [19]. Преобладающее большинство этих больных, после завершения хирургического этапа лечения, нуждается в проведении адъювантной лекарственной терапии. Одними из основных критериев выбора метода лекарственной терапии (использование цитостатиков, средств гормонотерапии) служит наличие или отсутствие экспрессии рецепторов эстрогенов, прогестерона и Her2-new в ткани опухоли, а так же состояние менструальной функции у женщины. Перечисленные факторы являются не только прогностическими, но и предсказательными в отношении чувствительности опухолевых клеток к тому или иному виду лечения и, в частности, гормонотерапии.
До настоящего времени ингибиторы/инактиваторы ароматазы третьего поколения служат краеугольным камнем гормонотерапии метастатического рака молочной железы, а сегодня всё шире используются для проведения адъювантной терапии у больных операбельным раком молочной железы в менопаузе. Последнее стало возможным после анализа результатов трёх крупных рандомизированных исследований, показавших, что использование ингибиторов/инактиваторов ароматазы III поколения: анастрозола, летрозола, экземестана в монорежиме или последовательно, после завершения 2-5 лет терапии тамоксифеном увеличивает длительность безрецидивного периода в сравнении с использованием тамоксифена [1, 2, 10-12].
Полученные данные кардинально изменили подходы к адъювантной гормонотерапии больных РМЖ в менопаузе.
Современные принципы адъювантной гормонотерапии больных РМЖ были сформулированы на совещании экспертов, состоявшемся в марте 2007 года в St. Gallen. А именно:
Изменение ранее существовавшей клинической практики проведения адъювантной терапии у больных РМЖ в менопаузе вызвало целый ряд вопросов у клиницистов:
Если обратиться к результатам ранее завершённых клинических исследований, нестероидные ингибиторы ароматазы III поколения (анастрозол и летрозол) и стероидный инактиватор (экземестан) снижают уровень эстрогенов в сыворотке крови более чем на 98%. Поэтому мы предположили, что любой из препаратов равно эффективен в режиме адъювантной терапии при гормоночувствительном РМЖ, любой режим терапии (моно или последовательно) в равной мере снижает абсолютный риск рецидива и риск смерти, и нет различий в побочных эффектах между лекарственными препаратами.
Очевидно, что для окончательного суждения о преимуществах или недостатках того или иного препарата и режиме его назначения, эффективности и безопасности терапии, сходстве и различиях между ингибиторами/инактиваторами ароматазы необходимы дальнейшие исследования. В современных условиях одним из основных критериев выбора схемы лечения, наряду с клинической эффективностью, переносимостью и безопасностью, является анализ эффективности затрат (cost effectiveness analysis / CEA). Любое различие по показателю «затраты-эффективность» (cost effectiveness ratio / CER) может оказаться существенным аргументом в пользу выбора того или иного лекарственного препарата и режима его назначения, поскольку даже при условиях схожей противоопухолевой эффективности ингибиторов/инактиваторов ароматазы, различные режимы терапии могут отличаться между собой по показателю CER.
В настоящее время в Российской Федерации требуется проведение оценки клинической и экономической эффективности медицинских технологий (ОМТ). Это является результатом осознания того, что решения, связанные с распределением ресурсов в стране с бюджетной системой финансирования здравоохранения, должны быть подкреплены информацией о стоимости лечения и об относительной эффективности медицинского вмешательства.
В данной статье отражены результаты анализа эффективности затрат, сравнивающего альтернативные схемы гормональной терапии рака молочной железы ингибиторами/инактиваторами ароматазы.
Цель исследования
Целью данной работы являлась сравнительная фармакоэкономическая оценка терапии анастрозолом, летрозолом и экземестаном пациенток с I-II стадиями РМЖ в условиях российской системы здравоохранения.
Задачи исследования
Популяция больных
Женщины, находящиеся в менопаузе, с I-II стадией рака молочной железы, находящиеся на гормональной адъювантной терапии ингибиторами/инактиваторами ароматазы.
Методология исследования
При проведении фармакоэкономического анализа был использован применяемый в РФ Отраслевой стандарт «Клинико-экономического исследования» [17]. Были использованы следующие методы экономического анализа:
Марковское моделирование. Для прогнозирования вероятности развития событий при лечении РМЖ и ассоциированных с ними прямых медицинских затрат за определённый период времени при использовании различных терапевтических стратегий была разработана Марковская модель, которая выбрана из-за длительного течения РМЖ. Её структура позволяет следующее:
Модель представлена на рис. 1 и табл. 1, продолжительность цикла модели 1 год (всего 5 циклов), включает следующие состояния [5]:
Рис. 1
Марковская модель прогрессирования рака молочной железы
Таблица 1
Матрикс Марковской модели рака молочной железы с переходом из одного состояния в другое
Для проведения клинико-экономического анализа разработан алгоритм принятия возможных решений при развитии рецидива заболевания (рис. 2).
Рис. 2
Алгоритм принятия возможных решений при развитии рецидива РМЖ («древо» решений)
Стоимость прямых медицинских затрат. По Стандарту оказания медицинской помощи больным со злокачественными новообразованиями молочной железы [20] были рассчитаны прямые медицинские затраты на использование медицинских ресурсов при оказании медицинской помощи больным РМЖ на:
Прямые медицинские затраты. Для расчётов ценовых показателей стоимости медицинских услуг мы использовали Прейскурант на оказание медицинских услуг клиник ПМГМУ им. И.М. Сеченова [18], ФГБУ «Российский научный центр рентгенорадиологии» за 2012 г. г. Москва [24]; цены на препараты сравнения были рассчитаны как средние розничные в аптеках г. Москвы [13].
Показатель эффективности затрат. Так как у сравниваемых стратегий разные показатели эффективности и затрат был проведён анализ показателя эффективности затрат (cost—effectiveness ratio – CER). Наиболее фармакоэкономически приемлемым считался наименьший показатель CER, который рассчитывался по следующей формуле:
CER = DC ÷ Ef, где
DC – прямые медицинские затраты (равно CoI – стоимости болезни);
Ef – эффективность (действенность), выраженная в показателях безрецидивной выживаемости (DFS – disease—free survival).
Вероятность перехода в состояние и эффективность препаратов. Вероятность перехода из одного состояния здоровья в другое и эффективность сравниваемых препаратов оценивалась по результатам контролируемых клинических исследований: ATAC [10, 11], ARNO 95 [6], BIG 1-98 [1, 2, 12], IES [3], на которых и обосновывался данный модельный фармакоэкономический анализ.
Вероятность перехода из одного состояния в другое
Исследование ATAC – оценка эффективности терапии анастрозолом по сравнению с тамоксифеном в качестве инициальной адъювантной терапии I-II стадии РМЖ (табл. 3) [10, 11].
Таблица 3
Вероятность перехода в исследовании ATAC из одного состояния в другое [10, 11]
Консультации: задать вопрос
На вопросы отвечает победитель номинации»ЛУЧШИЙ ОНКОЛОГ» Скворцов Виталий Александрович, высшей категории ГКОД, кмн, хирург-онколог, маммолог, пластический хирург
ВОПРОС: Здравствуйте, доктор. В ноябре 2019 обнаружен рмж. С50. 2 1ст т1сn0m0., хирургическое лечение: мастэктомия+сторожевые лу. Гистология: инфильтративная дольково-протокавая карцинома g2, 3л/у без атипии, ER+, Pgr+, HER2neu3+, ki67 21%. С декабря 12 паклитаксел каждяе 7 дней, Трастузумаб каждые 21 день. Сейчас сделала уже 10 Герцептина. Химиотерапевт спросил, почему не принимаю противогормональные препараты? Мне их не назначали ещё. Нужно ли начинать принимать, в начале лечения вроде бы говорил, что после Трастузумаба. Я в растерянности. Менструации прекратились 5 месяцев назад, мне 51 год. Подскажите, пожалуйста.
ОТВЕТ: Здравствуйте! Вам надо начать принимать Тамоксифен 20 мг ежедневно, необязательно ждать окончания лечения Трастузумабом. Тамоксифен и Трастузумаб могут приниматься одновременно.
ВОПРОС: Добрый вечер! Мне прописан анастрозол, но сейчас в продаже нет данного препарата, чем его можно заменить?
ОТВЕТ: Здравствуйте! Это препарат из группы ингибиторов ароматазы и существуют аналоги: летрозол, экземестан. В данном случае надо обратиться к своему лечащему врачу, и доктор Вам пропишет другой препарат. Самостоятельно нельзя менять препарат. Насколько мне известно в аптеках есть анастрозол в свободной продаже.
ОТВЕТ: Здравствуйте! Обсудите этот вопрос с лечащим врачом. Если Вы плохо переносите данный препарат и у Вас от этого препарата побочные выраженные изменения, то перейти на тамоксифен можно, но только после обсуждения данного перехода с лечащим врачом.
ОТВЕТ: Здравствуйте! Нестандартное у вас назначение. Мне кажется, что Вам назназанчили ингибиторы ароматазы с учетом N, обычно ингибиторы нананчаются при поражении лимфоузлов. В данном случае у вас 4 лимфоузла с лечебным патоморфозом, это значит (это были метастазы) у вас скорее всего N2, а не N1. Возможно, Вы еще привыкаете к экземестану, поэтому еще и сохраняются эти побочные эффекты, думаю скоро пройдут. Я не знаю почему Вам не назначили тамоксифен! Вы сдавали анализы крови на менопаузу, Золадекс полностью выключил яичники? Заменять на тамоксифен можно, но по согласованию с врачом, очень жалко отменять этот препарат, так как Вы себя заведомо лишаете этого препарата. Думаю побочные эффекты скоро пройдут. К сожалению, эти побочные эффекты не снять.
ВОПРОС: Здравствуйте, Виталий Александрович! После лечения РМЖ (последняя химия была 7 февраля) принимаю с 1 марта анастразол. До начала лечения анастразолом анализы ФСГ-121, Эстрадиол-5, Прогестерон-0,08. Сейчас после пяти месяцев приема анастразола ФСГ-137,7, Эстрадиол-5, Прогестерон-0,1. Очень беспокоюсь почему эстрадиол на прежнем уровне и не снижается? Что мне делать? УЗИ молочных желез: гипоэхогенная зона неправильной формы без четких контуров 2+1,8см (послеоперационные изменения), а также расширенные протоки. Заключение: эхографические признаки п/о изменений. В ноябре собираюсь делать ПЭТ/КТ всего тела.
ОТВЕТ: Здравствуйте! В норме при приеме анастрозола у Вас уровень эстрадиола не должен привывать 37, а у Вас он на уровне 5-7, то есть для Вас это хорошо. Главное чтобы этот уровень не был выше 37. Также зависит от лабораторных норм. Обсудите этот вопрос со своим лечащим доктором.
ВОПРОС: Здравствуйте, Виталий Александрович. У меня РМЖ 2А стадия гормонозавистмый, проведена операция мастэктомия правой груди (удалены подмышечные лимфоузлы справа), с метастазом в 1 из 14 удаленных лимфоузлов. Прошла лучевую терапию, назначенную консилиумом. Получила 2 укола бусерелина, принимаю тамоксифен. 1) Должна переходить на анастрозол, но не уверена, что «уснули» яичники. Сдала анализы на гормоны, но там только эстрадиол в постменопаузе, другие гормоны в каких-то других фазах (оставила у гинеколога результаты для расшифровки, она не смогла мне сразу сказать спят ли мои яичники?). Или ещё третий укол поставить, а потом снова сдать анализы на гормоны? Я правильно понимаю, все три гормона должны соответствовать постменопаузе? И только после этого начать принимать анастрозол. 2) Радиолог пишет в рекомендациях, чтобы химиотерапевт со мной решили вопрос о замене хирургической кастрации на хирургическую. Что предпочтительно и менее травматично для женщины: уколы бусерелина в течение двух лет или вырезать яичники, если мне 45 лет? Беременность не планирую.
ОТВЕТ: Здравстуйте! В Вашем случае лучше перейти на ингибиторы ароматазы (анастрозол или летрозол), это международная схема. Для Вас есть выгода в переходе на ингибиторы.
ВОПРОС: Добрый день! 45 лет. 5 лет назад удалена матка и яичники (не рак). 11.02.2020 результаты трепан-биопсии: инвазивная карцинома неспецифического типа G2, с очагами протоковой карциномы in situ. Результаты ИГХ исследования: ER 90%, PR 5%, Ki67 30%, HER2neu/c-erb-B2 отрицательный (1+) 22.02.2020 результат пункции л/у подкрыльцовой области справа: Mts карциномы. ПЭТ-КГ никаких изменений кроме л/у справа не обнаружено. Стадия 2Б. Пройдено 4 курса с антрациклинами и 4 введений с таксанами. 02.09.2020 проведена операция, предстоит лучевая терапия. Подскажите в моём случае (при удалённой матке и яичниках) какие препараты и на какой период Вы бы назначили для эндокринотерапии? Какие обследования и с какой периодичностью необходимо проводить?
ОТВЕТ: Я бы назначил Вам ингибиторы ароматазы, потому что вы в хирургической менопаузе. Процедуры обследования стандартные, прописанные приказами, но я рекомендую вам как молодой женщине выполнять компьютерную томографию грудной клетки, брюшной полости, малого таза и остеосцинтиграфию 1 раз в год.
ОТВЕТ: Здравствуйте! В данном случае лечение назначено корректно. У любого препарата может быть побочные эффекты. В данном случае если они незначительны, то их можно какое то время потерпеть, они со временем уменьшаться. Анастрозол есть во всех аптеках. Этот препарат легко доступен. Смена препарата происходит строго по рекомендации врача. Обратитесь к своему онкологу, и он Вам, если необходимо, сменит препарат. Препаратов для смены анастрозола много, но только после обсуждения этого вопроса с Вашим врачом.
ВОПРОС: Добрый вечер. Принимаю фарестон 60мг, гинеколог назначил buserelin, можно ли его применять одновременно с основной терапией?
ОТВЕТ: Здравствуйте! Данный препарат Бусерелин выключает работу яичников, при приеме Фарестона не противопоказано при одновременном введении Бусерелина. Это комбинация препаратов наоборот входит в схему лечения рака молочной железы у женщин с сохранённым циклом.
ВОПРОС: Виталий Александрович! Добрый день! Скажите, пожалуйста, у меня вопрос можно ли вместо Тамоксифена принимать Фарестон, или все-таки лучше принимать Тамоксифен? Меня зовут Елена возраст 50 лет, диагноз рак инвазивный неспецифицированный протоковый левой молочной железы сТ4bN0M0 (урТ1сN1M0)? IIIB стадия вторично-отечная форма, GII, люминальный тип В, Her2-негативный (РЭ-7 баллов, РП-6 баллов, Her2/neu-, Ki67 30%) Неоадьювантная полихимиотерапия 4 курса АС + 4 курса Паклитаксел. Операция 02.09.2020: радикальная мастэктомия слева с сохранением обеих грудных мышц. Дистанционная лучевая терапия на оставшуюся часть левой молочной железы СОД= 50Гр (по РБЭ). И еще недавно смотрела Ваш эфир, где Вы сказали что если женщина худая, то отсроченная реконструкция не благодарное дело, т.е. очень сложно сделать реконструкцию? А как понять, только при осмотре возможна ли реконструкция? Спасибо!
ОТВЕТ: Здравствуйте! Если менопауза подтверждена, то принимать Фарестон можно, но лучше остаться на тамоксифене или вообще перейти на ингибиторы ароматазы, но при подтверждении, что у Вас менопауза. Я могу выполнить реконструкцию любому человеку, но просто худой женщине это делать самому хирургу сложнее и приходится иногда использовать вместе с имплантами и лоскуты со спины, но сделать, конечно, можно! Все нюансы решаются на консультации.
ВОПРОС: Добрый вечер, Виталий Александрович! У меня вопрос по приему тамоксифена. Операция по удалению молочной железы была 19.02.20. Диагноз Т1NOMO, затем химиотерапия, на фоне химиотерапии закончились месячные. И в августе начале прием тамоксифена, сделала изи матки эндометрий был 2мм. Сейчас пошла на осмотр в связи с кровянистыми выделениями, эндометрий стал 4мм и киста на яичнике! Это за 5 месяцев. Я очень боюсь теперь за матку! С уважением, Наталья.
ОТВЕТ: А в чем проблема? Обсудите вопрос с гинекологом. Это же очень мало 4мм. Совсем мало. На фоне приема Тамкосифена могут быть кровянистые выделения. Необходимо продолжить прием Тамоксифена. Обсудите вопрос с лечащим онкологом и, возможно, он посчитает Вам заменить тамоксифен на другой препарат.
ВОПРОС: Здравствуйте, я принимала анастразол 5 лет. Доктор предложил продлить прием еще на 2 года, так как какие-то новые стандарты. Я была не готова и самостоятельно бросила прием анастразола, прошло пол года, могу ли я заново начать прием анастразола или не имеет смысла?
ОТВЕТ: Здравствуйте! Нет смысла, просто надо продолжить наблюдение в прежнем режиме и соблюдать все обследования один раз в год.
ВОПРОС: Добрый день! Скажите, пожалуйста, почему при гормонозависимом РМЖ кому-то отключают яичники, а кому-то нет. Мне 38 лет, назначен тамоксифен без отключения яичников.
ОТВЕТ: Многое зависит от стадии, обычно в данном возрасте отключают яичники тоже, но при 1 а стадии не отключают, а при всех остальных стадиях по российским стандартам яичники отключают.
ОТВЕТ: Здравствуйте! По всем рекомендациям Вам показаны уколы в течение 5 лет, т.е надо продолжить уколы Золадекса и далее. Консилиум должен переназначить Вам данные уколы до 5 лет.
ВОПРОС: Добрый день, 49 лет. РМЖ Т2N0MO, радикальная мастэктомия с удалением Лу. Неr2-3+, Ki65-80%,Эр100% Пр70%, G3. Прошла адъювантную химиотерамию. Назначили тамоксифен через 2 недели после последнего доцетаксела. Через две недели после после начале его приема на госпитализации укололи бусерелин вм и трастазумаб вв. Другой доктор сказал, что это неправильно и надо было сначала калоть бусерелин и через 2 недели добавлять тамоксифен 20 мг. Чем мне это может грозить? Говорят, что риск высокий и прогноз не очень хороший, хоть и лимфоузлы чистые. Спасибо Вам за помощь!
ОТВЕТ: Здравствуйте! Вы все сделали правильно и тамоксифен можно принимать как одновременно с данными препаратами и, тем более, никак не зависит от инъекций бусерелина. Очередности не существует. Вот прием ингибиторов ароматазы зависит от уколов Бусерелина.
ВОПРОС: РМЖ. удалена левая молочная железа 2019 г! Прошла 4 химии АС, после 2 химии пропали и по сей день нет! Кололи бусерелин и назначили тамоксефен на 5 лет! В данный момент делаю реконструкцию 1 этап, закачиваем эспандр физ раствором, готовилась к апрелю на 2 этап замены эспандера на имплант! Пошла самостоятельно на узи, так как нормальных врачей нет, эндаметрий 18мм и и на левом яичнике кистозное образование большого размера! Что делать и опасно ли эндометрий 18 мм?
ОТВЕТ: Здравствуйте! Это нехорошо, но и неопасно, так как на фоне приема тамоксифена и бусерелина это нормально. Проконсультируйтесь с онкогинекологом, и он Вас успокоит или по каким-либо причинам отправит на диагностическое выскабливание. Это пограничный уровень для выскабливания. Хотя некоторые гинекологи отправляют на выскабливание уже при 6-8 мм.
ОТВЕТ: Здравствуйте! Вам 44 года и первая стадия. Это требует назначения тамоксифена, но назначение золадекса на усмотрение врача, если он видит у Вас факторы риска! Все индивидуально, обсудите вопрос с лечащим врачом!
ВОПРОС: Добрый день, подскажите. пожалуйста, в больнице пока нет летрозола. Можно ли заменить на анастрозол. Врач сказал что можно, но говорят что это разные препараты.
ВОПРОС: Добрый день, вопрос о критичности в пропуске приема Летрозола 2 5 мг в течение 4х дней. В связи с тем, что не смогла купить препарат пропустила прием препарата в течение 4-х дней. Прошу уточнить, как по Вашему мнению, насколько это опасно. Спасибо.
ОТВЕТ: Здравствуйте, это абсолютно неопасно, но лучше этого не делать! Пропуск с при адъювантном лечении до 7 дней некритичен.
ВОПРОС: Добрый день, я принимаю Анастрозол по 1 мг, не помню выпила таблетку или нет))))) Что делать в этом случае?
ВОПРОС: Здравствуйте, Виталий Александрович! Прохожу лечение по поводу гормонозависимоного рака: 1,5 года пью тамоксифен, делаю уколы золадекс (сделала 5 уколов). У меня появился сладкий привкус во рту. Может ли это быть связано с лечением, в аннотации к золадексу один из видов побочки нарушение толерантности к глюкозе. Сталкивались ли с этим в своей практике? Анализ на сахар нормальный. Может посоветуете дополнительные обследования, на что обратить внимание. С уважением к Вам и Вашей работе.
ОТВЕТ: Вам не могли назначить Анастрозол без Золадекса, так как должна быть стойкая менопауза. Обсудите этот вопрос со своим доктором. Или у вас подтверждена менопауза? Если у вас менопауза, то тамоксифен заменить на анастрозол возможно.
ВОПРОС: Здравствуйте. Меня зовут Валерия. 36 лет. Рак левой молочной железы T2N1М0. 12. 2015 г. хирургическое лечение-радикальная мастэктомия слева по Мадден, инвазивная неспецифицированная карцинома МЖ G2. ИГХ: ER-4, PR-6, Her2+++, Ki67-20%. Химиотерапия 8 курсов, герцептин 1 год, золодекс + тамоксифен (с 08.2016 по 10.2020 (4 года) далее назначили золодекс + анастрозол. После начала приёма анастразола (Селана) начался лимфостаз с оперированной стороны и боль в лучезапястном суставе, в следующем месяце в аптеке дали анастрозол другого российского производителя, отек уменьшился боль прошла. Но через 3 месяца от начала приема, появились следующие проблемы: в течение дня внезапно начинает повышаться пульс, на этом фоне появляется отдышка и присоединяется паническая атака, сначала это были разовые приступы раз в неделю, сейчас это происходит каждый день, зная что все симптомы ведут к ПА, я научилась справляться не доводя до нее, в течение дня у меня несколько приступов тахикардии и постоянное чувство тревоги. Пробовала менять на испанский препарат, эффект тот же, прошла обследования, ЭХО сердца, гормоны щитовидной железы, все в норме. 10 дней я не пила анастрозол, все симптомы прошли, потом по согласованию с врачом начала пить летрозол и через 4 дня приема все симптомы снова вернулись. По назначению невролога принимаю противотревожные препараты, не помогает. Скажите, пожалуйста, как быть в такой ситуации, такое состояние значительно ухудшает качество жизни, невозможно нормально работать и жить. Есть ли альтернативные варианты гормонотерапии, можно ли снова вернуться к тамоксифену? Спасибо за ответ.
ОТВЕТ: Здравствуйте! Вот прочитал я все и у меня складывается мнение, что здесь что-то не так: ингибиторы ароматазы не вызывают всего того, что с Вами происходит, это какая-то другая причина. Больше наверное психосоматическая. Надо подобрать терапию против вашего тревожного состояния, обычно это вызывает все приступы.Также вариант уже перестать принимать препарат, так ка у вас уже 5 лет антигормонльная эндокринотерапия ингибиторами ароматазы. На тамоксифен не рекомендовано переходить.
ОТВЕТ: Учитывая Ваш молодой возраст, стадию и фенотип рака я бы назначил Золадекс на 5 лет, а Тамоксифен пока на 7 лет.
ВОПРОС: В 2015 году была операция, рак левой молочной железы, без метастазов. Гистологическое исследование: инфильтрирующая карцинома 2 ст злокачественности в л/у без метастазов. 6 курсов химиотерапии, приём летрозола в течении 5 лет. Прошло 5 лет, доктор отменил приём летрозола резко. А подруге постепенно, принимая через день. Кто прав?
ОТВЕТ: Отмена проводится сразу же, без снижения дозы. Просто прекращаете пить и дозу снижать не надо. Нет такого и нигде не прописано, после указанного срока отменяется препарат резко.
ОТВЕТ: Отключение яичников может быть лекарственным путем или же хирургическим, это Вы должны обсудить с лечащим врачом что лучше для Вас. Лечение правильное, и я согласен. Но вам 46 лет и у вас 1 стадия и в данном случае Вы вообще не в группе риска и яичники можно не отключать согласно рекомендациям Минздра РФ, тем более после химиотерапии они у Вас сейчас, скорее всего, не работают все еще.
ОТВЕТ: Сколько Вам лет? В принципе если у Вас еще менопаузы нет, то надо продолжить прием тамоксифена, фарестон не стоит. Если вам больше 40 лет, то и отключать при такой ранней стадии яичники не стоит, а вообще отключают на 5 лет.
ВОПРОС: Здравствуйте, Виталий Александрович. Помогите, пожалуйста, расшифровать результат анализа и подскажите, правильно ли назначено лечение. Рак левой молочной железы Т2N0M0, Ki6720%. Люминальный тип В. Инвазивная карцинома молочной железы 3ст злокачественности. Операция была проведена в декабре 2020г, до операции прошла 8 курсов химиотерапии (4 доксирубицин и 4 доцетаксел). Теперь назначено пить анастразол в течении 5лет. С него сильно болят суставы. Химиотерапевт решил заменить его на тамоксифен. Скажите, пожалуйста, стоит ли на него переходить? Мне 51 год. В 2018 была операция по удалению матки.
ОТВЕТ: Если в данном случае прием ингибиторов ароматазы невыносим, то можно перейти на тамоксифен, если все же это нет так для вас болезненно, то лучше остаться на данном препарате. Но любой переход на другой препарат по согласованию с Вашим лечащим врачом. Лечение Вам назначено адекватное.
ОТВЕТ: У Вас люминальный тип В, то есть гормонозависимый. Аримидекс конечно же эффективен, только надо быть на 100% уверенной, что у Вас не работают яичники, укол люкрина должен выключить Ваши яичники. Это можно легко проверить: сдать кровь на эстрадиол и фсг. Ещё раз обсудите этот вопрос с лечащим врачом!
ВОПРОС: Добрый день, Виталий Александрович. Мне 48 лет. В ноябре 2019 году поставлен диагноз Инвазивный неспецифицированный рак G2. ER 95% 5+3=8б, PR 70% 5+3=8 б; HER2 неполное мембранное окрашивание более 10 % опухолевых клеток, 1+, сверхэспрессия негативная; Ki 67-65%. Наибольшим размером1,1 см. in situ компонент солидного крибриформного типов. Лимфоваскулярной и периневральной инвазии не выявлено. Края резекции вне опухоли. В 1 из 2-х сигнальных лимфоузлов метастаз, в дополнительно присланных 6 аксиллярных лимфоузлов без метастазов. Проведена секторальная резекция левой молочной железы. pT1cpN1a (1/8) pMn/a. Рак левой молочной железы cT1N0M0/pT1cN1aM0/ Проведено 4 курса АПХТ по АС, 4 курса АМХТ Доцетакселом, затем курс лучевой терапии на левую молочную железу и региогарные лимфатические узлы и эндокринотерапия тамоксифеном по 20 мг. в течении 5 лет. Вопрос: Удалили матку и яичники для снижения рисков в 2020 г. в ноябре. Принимала 6 мес. тамоксифен по 20 мг после химиотерапии и лучевой терапии. Перешла на фаристон- принимаю 6 мес. Но он слишком дорогой, поэтому хочу перейти на аримидекс. Возможно ли это при моем диагнозе и при том, что удалены матка и яичники? PS: Месячных нес с апреля 2019 года.
ОТВЕТ: Перейти возможно, но любая смена препарата строго по решению консилиума и это строго. Вы принимали антиэстроген, а хотите перейти на ингибиторы ароматазы, это разные группы! Возможно лучше перейти на тамоксифен, этот препарат из одной группы, обсудите вопрос с лечащим врачом.
ОТВЕТ: Лечение в Вашем случае согласно рекомендациям только прием тамоксифена и все! Но если консилиум Вам рекомендовал и уколы Золадекс, значит, для этого были какие-то показания, обсудите это с лечащим врачом в НИИ Петрова. Я не вижу оснований для приема Золадекса по Вашим документам. Возможно, вы что-то не предоставили, не вся информация.
ВОПРОС: Добрый день. T2N0M0, Ki 67- 67%. Грудь удалили, вставили имплант. 4 курса химиотерапии Доцетаксел 125мг + Циклофосфамид 1000мг закончила 14.09.21. Сегодня 27.09.21 иду колоть Золадекс 3,6. У меня такой вопрос: когда начинать принимать Армидекс? Можно начинать принимать сразу после укола (в этот же день) или надо через несколько дней, после анализа на гормоны, чтоб убедиться, что яичники отключились? Матка удалена уже давно, по уровню гормонов у меня начало вхождения в менопаузу. И еще вопрос: Не целесообразней ли колоть Золадекс 10,8, чтоб сразу на 3 месяца отключать? Заранее спасибо за ответ!
ОТВЕТ: Аримидекс необходимо начинать только после подтверждения менопаузального уровня гормонов! Это может быть достигнуто минимум через месяц после первого укола или даже больше! Дозировка тоже может быть и на 3 месяца, главное, чтобы это назначил и согласуйте все дозировки вместе с доктором!
ОТВЕТ: Если Вам яичники не нужны, то можно и удалить яичники. Если же у вас есть планы на и вы вомжоно захотите вернуться к менструациям, то лучше колоть Золадекс. По эффекту это одинаково, что кастрация операцией или же уколы. Риски до конца все равно не исключить.
ОТВЕТ: Здравствуйте! Вам в принципе показано отключение яичников, это можно сделать хирургически, заодно и кисту удалите, так и лекарственно и снизится уровень эстрадиола! Прием тамоксифена не влияет на уровень эстрадиола!
ВОПРОС: Здравствуйте, доктор. Мне 39 лет, инвазивная карцинома молочной железы неспецифического типа G3, люминальный тип В, HER2 негативный, эстроген 5 (TS), прогестерон 0, her2=1+, ki=80, в 04.2021 кожесохранная мастэктомия левой МЖ, отсроченная реконструкция МЖ, затем закончились 4 АПХТ по схеме АС и 12 паклитаксел. По результатам УЗИ и КТ все чисто. Назначили анастразол 1 мг ежедневно и гозерелин 3,6 мг 1 раз в 28 дней на 5 лет, верно ли лечение? Что меня ждёт?
ОТВЕТ: У вас абсолютно правильное лечение и я согласен! Можно было начать лечение и с тамоксифена с Гозерелином. но раз Вы начали принимать анастрозол, то уже надо остаться на нем (анастрозоле). Что вас ждет?Что вы имеете ввиду? Вас ждет прием анастрозола и Гозерелина в течение 5 лет и ремиссия, наблюдение у онколога.
ВОПРОС: Здравствуйте, Виталий Александрович! В конце сентября мне сделали операцию по удалению м/ж, Рак, узловая карцинома Т1N0М0. После операции обнаружили тромб в ноге. Были назначены уколы эноксапарина 28 дней, затем три месяца Ксарелто. Так же назначен Тамоксифен. Можно ли сочетать приём этих двух препаратов? Ксарелто пью утром, Тамоксифен вечером. Правильно ли это? Спасибо!
ОТВЕТ: Здравствуйте! Они абсолютно совместимы и прием этих препаратов разрешен. Но в любом случае любой прием препаратов надо согласовывать с лечащим врачом.
ВОПРОС: Здравствуйте доктор. У меня рмж с 2018, секторальная резекция, люминальный А, ki67-5%, пр-8, эр-7, 8 химий и 25 лучей. 3 года тамоксифен, поменяли на золадекс и анастразол в связи нарастанием эндометрия. Сдала кровь на кальций. Норма 2,5 а у меня 2,7. Врач выписал аквадетрим и омега 3. Больше никаких анализов не назначил. У меня к Вам вопрос, правильно ли назначил доктор лечение?
ОТВЕТ: Я полностью согласен с назначением врача, если эта смена препарата была связана с нарастанием многократным эндометрия. Смена препарата строго по согласованию с врачом.
ОТВЕТ: Все же такие вопросы надо обсуждать с лечащим врачом и гинекологом. Кровянистые выделения это не повод для смены препарата. Надо обсудить тактику введения с гинекологом. Возможно достаточно обойтись диагностическим выскабливанием. Удаление матки в данном возрасте тоже является способом лечения и удаление матки и яичников заменит уколы Золадекса.
ВОПРОС: Мне 46 лет. В октябре 2021 была проведена органосохранная операция на груди. Т2M0N0, эстроген и прогестерон по 25%, Her2 1+, ki67-17%. Пройдены 4 курса красной химии. Менструации до операции шли регулярно и во время химии не прекратились, только после последней была задержка в две недели. Назначен тамоксифен и золадекс, которые я ещё не начала принимать. Надо ехать на облучение, и я заболела коронивирусом. Вопрос в том, когда надо начинать ставить золадекс после облучения или сразу как только вылечусь от коронивируса? Тамоксифен после лучевой пить сказали, а про укол все говорят по-разному.
ОТВЕТ: Я бы Вам рекомендовал продолжить прием тамоксифена ежедневно и не стоит вам менять тамоксифен на ингибиторы пари раке in situ и, тем более, отключать яичники. При раке in situ это лишние меры. но стоит все же обсудить окончательно все детали и смены препарата с лечащим врачом и тем более смена препарата происходит только решению онкологического консилиума.
ОТВЕТ: В данном случае необходимо продолжить лекарственную терапию ингибиторами ароматазы, т.к риск прогрессирования все же есть. У вас на лицо побочные эффекты приема ингибиторов ароматазы и они не столь критичны. Обсудите все же дальнейший прием с лечащим врачом, я бы продолжил в течение года точно с последующей оценкой при дообследовании.
ОТВЕТ: В Вашем случае необходимо отключать яичники, т.к у Вас есть один из факторов при котором назначается отключение яичников, обсудите это вопрос с лечащим врачом.
ВОПРОС: Добрый вечер Виталий Александрович. Мне 46 лет. Инвазивный протоковый рмж T1cN0M0. G2. ER-положит, PR-высокие.HER 3+ Ki67-21%. В августе прошлого года секторальная резекция, затем 12 пакли+герцептин, 25 лучей. Сейчас тамоксифен (с 13 января) и продолжаю герцептин. До рмж были регулярные. После 2 курса химиотерапии пропали и нет по сей день. Имеется киста яичника 4 см лет 8 уже. Получила на этой неделе результаты анализов: эстрадиол-1,5 пг/мл, ФСГ-66,45 МЕ/л. Вопрос: нужно ли в моем случае принимать золадекс? Если читать практические рекомендации RUSSCO, то вроде при наличии по крайней мере одного фактора неблагоприятного прогноза, а в моем случае это HER2 3+, его надо принимать. Не опоздала ли с началом его приема? (химию закончила в конце ноября, лучи закончила в 12 января).
ОТВЕТ: В данном случае учитывается уровень гормонов, но пока вы находитесь в менопаузе, можно попробовать пересдать гормоны и посмотреть есть ли рост через 8 недель. Добавить Золадекс или его аналоги всегда можно и позже, тем более, Вы принимаете тамоксифен, который не требует обязательного отключения функции яичников!
ОТВЕТ: Здравствуйте! В данном случае у Вас проявления вхождения вас в менопаузу и у вас приливы, и это обычно переносится тяжело. В Вашем случае надо пробовать все препараты, главное, чтобы они не содержали эстрогены. Опытном путем можно подобрать себе препарат и советуйтесь с лечащим врачом и гинекологом.
ОТВЕТ: Здравствуйте! Какая стадия заболевания? Какой возраст? Была ли операция и какая если была? Есть ли сопутствующая патология? Предоставьте мне информацию, и я смогу Вам ответить на Ваш вопрос.
ВОПРОС: РМЖ 2А, гормонозависимый. Радикальная мастэктомия в феврале 2022г. Возраст 43 года, менопаузы нет, назначили бусерелин и анострозол. Можно ли мне принимать таблетки, если ещё не закончились?
ОТВЕТ: В данном случае нельзя принимать анастрозол, надо подтвердить менопаузу анализом крови: кровь на ФСГ и эстрадиол, чтобы после уколов была менопауза и после этого только можно начинать принимать анастрозол. Обсудите этот момент с лечащим врачом. Доктор должен был обсудить с Вами данный этап.
Материалы конгрессов и конференций
40 съезд Американского общества клинической онкологии (ASCO)
5-8 июня 2004 года, Новый Орлеан, США
ASCO 2004: рак молочной железы
Тюляндин С.А.
ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России
В гормонотерапии рака молочной железы происходит «ползучая революция»: прежний фаворит тамоксифен повсеместно уступает дорогу целому семейству ингибиторов ароматазы. Первоначально летрозол (Фемара) и анастрозол (Аримидекс) продемонстрировали свое преимущество над тамоксифеном при проведении первой линии гормонотерапии у больных метастатическим раком молочной железы в постменопаузе с положительными рецепторами эстрогенов 3. На съезде ASCO впервые были представлены результаты сравнения третьего представителя из группы ингибиторов ароматазы – экземестана с тамоксифеном при проведении первой линии гормонотерапии у больных метастатическим раком молочной железы. Экземестан (Аромазин), в отличие от анастрозола и летрозола, относится к группе необратимых стероидных ингибиторов ароматазы. В исследовании EORTC 382 больные получали тамоксифен или экземестан в дозе 25 мг ежедневно постоянно до признаков прогрессирования заболевания [4]. Основным критерием эффективности был показатель времени до прогрессирования. При среднем сроке наблюдения 29 месяцев медиана времени до прогрессировании составила 9,9 мес. в группе экземестана и 5,8 мес. в группе тамоксифена (р.=0.03 Wilcoxon test). У больных принимавших экземестан достоверно чаще наблюдали объективные противоопухолевые эффекты (46% и 31%). Таким образом, предварительные данные свидетельствуют о преимуществе назначения экземестана (как и других ингибиторов ароматазы) при проведении первой линии гормонотерапии у больных метастатическим раком молочной железы в постменопаузе с положительными рецепторами стероидных гормонов.
Cameron и соавторы попытались сравнить эффективность экземестана и анастрозола при лечении 121 больной метастатическим раком молочной железы с метастазами в висцеральные органы (печень, легкие) [5]. Результаты исследования представлены в таблице 1 и свидетельствуют о равной эффективности сравниваемых препаратов.
Таблица 1.
Результаты сравнения экземестана и анастрозола.
| Экземестан | Анастрозол | |
|---|---|---|
| Число больных | 61 | 60 |
| ПР + ЧР | 25% | 25% |
| ПР + ЧР + стабилизация | 38% | 38% |
| Медиана времени до прогрессирования | 4.0 мес. | 4.5 мес. |
ПР – полная регрессия, ЧР – частичная регрессия.
Доказав свое преимущество при проведении первой линии, ингибиторы ароматазы перенесли соревнование на этап проведения адъювантной терапии. В исследовании ATAC анастрозол 1 мг ежедневно в течение 5 лет сравнивали с тамоксифеном 20 мг ежедневно в течение 5 лет при проведении адъювантной терапии у больных операбельным раком молочной железы в постменопаузе с положительными рецепторами стероидных гормонов [6]. При среднем сроке наблюдения 48 месяцев в группе анастрозола достоверно снижена частота прогрессирования от рака молочной железы на 17% по сравнению с тамоксифеном. Это снижение произошло как за счет уменьшения частоты отдаленных метастазов, так и частоты возникновения контрлатерального рака молочной железы. Короткий срок наблюдения не позволяет оценить влияние анастрозола на общую выживаемость.
Другим перспективным подходом является последовательное назначение тамоксифена и ингибиторов ароматазы у больных с отсутствием менструальной функции и положительными рецепторами. В исследовании МА17 больные, закончившие прием тамоксифена в течение 5 лет, рандомизировались в группу плацебо или летрозола в дозе 2,5 мг ежедневно в течение 5 лет [7]. При среднем сроке наблюдения 2,4 года исследование было прекращено в связи с достижением статистически достоверной разницы в 4-летней безрецидивной выживаемости между группами плацебо и летрозола, которая составила 87% и 93% соответственно. На съезде ASCO были представлены последние сведения об отдаленных результатах исследования МА 17 [8]. При сроке наблюдения почти 3 года 5-летняя безрецидивная выживаемость составила 94,7% в группе летрозола и 89,8% в группе плацебо (р.=0.00004). Уменьшение частоты рецидивов наблюдается независимо от наличия или отсутствия метастазов в подмышечные лимфоузлы. При анализе общей выживаемости отмечено достоверное ее улучшение в группе больных с наличием метастазов в подмышечные лимфоузлы. Небольшое число смертельных исходов в группе больных без метастазов в подмышечные лимфоузлы не позволяет проводить сравнение выживаемости.
В итальянском исследовании после 2-3 лет приема тамоксифена больные рандомизировались в группу продолжения приема тамоксифена (общая продолжительность терапии 5 лет) или им назначали анастрозол в дозе 1 мг ежедневно в течение 2-3 лет [9]. Переключение с тамоксифена на анастрозол достоверно улучшило результаты 5-летней безрецидивной выживаемости по сравнению с приемом тамоксифена только. Подобный дизайн исследования был использован для сравнения приема тамоксифена в течение 5 лет и последовательного назначения тамоксифена в течение 2-3 лет и экземестана в дозе 25 мг ежедневно в течение 2-3 лет [10]. В исследование было включено 2362 больные, у которых при сроке наблюдения 30 месяцев отмечено достоверное улучшение 3-летней безрецидивной выживаемости в группе экземестана по сравнению с тамоксифеном: 91,5% и 86,8% соответственно (р.=0.00005). Уменьшение частоты прогрессирования заболевания в группе экземестана произошло как за счет уменьшения частоты отдаленных метастазов, так и возникновения контрлатерального рака молочной железы. Переносимость двух препаратов была хорошей с большей частотой артралгии и диареи в группе экземестана, маточных кровотечений и тромбоэмболий в группе тамоксифена.
Таким образом, складывается впечатление о целесообразности использования ингибиторов ароматазы при проведении адъювантной гормонотерапии у больных операбельным раком молочной железы в постменопаузе с положительными рецепторами стероидных гормонов. Остается непонятным, какая стратегия имеет преимущество: назначение ингибиторов ароматазы только (как в исследовании ATAC) или последовательное назначение тамоксифена с последующим переходом (через 3 года? через 5 лет?) к ингибиторам ароматазы (как долго принимать?). Уже сегодня представляется оправданным всем больным раком молочной железы в постменопаузе, особенно с наличием метастазов в подмышечные лимфоузлы, после 3-5 лет приема тамоксифена рекомендовать прием ингибиторов ароматазы в течение как минимум 2-3 лет.
При длительном назначении больным операбельным раком молочной железы ингибиторов ароматазы должны учитываться отдаленные последствия приема этих препаратов. Ингибиторы ароматазы существенным образом снижают эндогенный уровень эстрогенов в различных тканях, что может способствовать уменьшению плотности костной ткани с развитием остеопороза и увеличению содержания липидов и холестерина в крови с последующим увеличением риска развития атеросклероза, стенокардии и инфарктов миокарда. В исследовании ATAC прием анастрозола сочетался со снижением плотности костной ткани и большой частотой патологических переломов в сравнении с группой тамоксифена [11]. На ASCO были представлены результаты влияния экземестана на плотность костной ткани и уровень липидов в крови по сравнению с больными, получавшими тамоксифен [12, 13]. При наблюдении в течение 2 лет снижение плотности костной ткани на фоне приема экземестана и тамоксифена были одинаковыми, частота патологических переломов костей таза вследствие остеопороза была выше в группе экземестана, частота переломов тел позвонков одинаковой в обеих группах. Прием экземестана приводил к уменьшению содержания липопротеинов высокой плотности и холестерина в крови, не влиял на концентрацию других фракций липидов, параметров свертывающей системы крови и не повышал риск развития сердечно-сосудистых осложнений. Следует продолжить изучение последствий длительного приема ингибиторов ароматазы (создается впечатление, что стероидный ингибитор экземестан в меньшей степени оказывает негативное влияние на плотность костной ткани и концентрацию холестерина в крови, чем нестероидные ингибиторы анастрозол и летрозол), однако результаты проведенных сегодня исследований свидетельствуют, что их частота не является серьезным аргументов против назначения этих препаратов адъювантно.
Ингибиторы ароматазы стали использоваться при проведении предоперационной терапии. Известно, что эффективность предоперационной химиотерапии у больных раком молочной железы в постменопаузе с положительными рецепторами гораздо ниже, чем у больных с отрицательными рецепторами. Так, частота морфологически подтвержденных полных регрессий опухоли после предоперационной химиотерапии среди больных с положительными и отрицательными рецепторами составила 5% и 21% соответственно [14]. Поэтому оправданным выглядит исследование Семиглазова и соавторов, которые рандомизировали больных операбельным раком молочной железы в постменопаузе с положительными рецепторами стероидных гормонов либо в группу химиотерапии комбинацией доксорубицин+паклитаксел 4 курса, либо назначали в течение 3 месяцев анастрозол или экземестан [15]. Результаты исследования представлены в таблице 2.
Таблица 2.
Результаты сравнения химиотерапии и ингибиторов ароматазы в качестве предоперационного лечения
| Химиотерапия | Анастрозол | Экземестан | |
|---|---|---|---|
| Число больных | 62 | 32 | 29 |
| Полная регрессия | 76% | 76% | 81% |
| Морфологически полная регрессия | 7% | 3% | 7% |
Несмотря на высокие цифры клинически полных регрессий при проведении предоперационной химиотерапии, только у 7% больных это подтверждается морфологическим исследованием. Непосредственная противоопухолевая эффективность ингибиторов ароматазы была сопоставимой с эффективностью химиотерапии. При среднем сроке наблюдения 30 месяцев частота местных рецидивов составила 3,2% в группе химиотерапии и 3,4 % в группе гормонотерапии. Поскольку только морфологически полные регрессии опухоли после проведенной предоперационной терапии улучшают прогноз больных, можно сделать вывод о недостаточной эффективности, как предоперационной химиотерапии, так и гормонотерапии у больных в менопаузе с положительными рецепторами. Для них предпочтительнее всего выполнение оперативного вмешательства на первом этапе с последующим проведением адъювантной терапии.
Buzdar и соавторы продемонстрировали, что добавление трастузумаба (Герцептина) при проведении предоперационной химиотерапии у больных с гиперэкспрессией HER2 достоверно увеличивает частоту морфологически полных регрессий [16]. Все больные с гиперэкспрессией получали предоперационную химиотерапию, включающую паклитаксел 225 мг/м² каждые 3 недели 4 курса и комбинацию FEC (500/50/500 мг/м²) каждые 3 недели 4 курса. Часть больных одновременно получала трастузумаб (4 мг/кг 1 неделя, затем 2 мг/кг еженедельно) в течение 24 недель. Частота морфологически полных регрессий в группе химиотерапии составила 25%, в группе химиотерапии+трастузумаб 67% (р.=0.02). Частота кардиотоксичности была одинаковой в обеих группах. Авторы вправе ожидать существенного улучшения отдаленных результатов в группе химиотерапии и трастузумаба после получения столь высокой частоты морфологически полных регрессий.
Таблица 3.
Эффективность трастузумаба у больных с отсутствием гиперэкспресии HER2.
| Паклитакселl | Паклитаксел + трастузумаб | Р. | |
|---|---|---|---|
| Число больных | 111 | 112 | |
| Объективный эффект | 29% | 35% | 0.34 |
| Время до прогрессирования | 6 мес. | 7 мес. | 0.09 |
| Продолжительность жизни | 20 мес. | 22 мес. | 0.67 |
Полученные данные убедительно свидетельствуют еще раз, что больным с отсутствием гиперэкспрессии HER2 назначение трастузумаба не улучшает результаты проводимой химиотерапии. Гемцитабин (Гемзар) зарегистрирован для лечения больных раком молочной железы на основании результатов исследования, представленных Albain и соавторами [18]. В рамках этого исследования 529 больных метастатическим раком молочной железы в качестве первой линии химиотерапии получали только паклитаксел в дозе 175 мг/м² каждые 3 нед. либо комбинацию паклитаксела 175 мг/м² 1 день и гемцитабин 1250 мг/м² 1 и 8 дни каждые 3 нед. до признаков прогрессирования заболевания. Большинство больных ранее получали антрациклины в качестве адъювантной или предоперационной терапии. Результаты исследования представлены в таблице 4 и свидетельствуют, что добавление гемцитабина к паклитакселу при проведении первой линии химиотерапии достоверно удлиняет время до прогрессирования и продолжительность жизни на 2,3 и 2,7 месяцев соответственно.
Таблица 4.
Результаты сравнения паклитаксела и комбинации паклитаксел+гемцитабин у больных метастатическим раком молочной железы.
| Паклитаксел+ гемцитабин | Паклитаксел | |
|---|---|---|
| Число больных | 267 | 262 |
| Объективный эффект | 41% | 22% |
| Время до прогрессирования | 5.2 мес. | 2.9 мес. |
| Продолжительность жизни | 18.5 мес. | 15.8 мес. |
| 1-годичная выживаемость | 71% | 60% |
Принимая во внимание умеренный выигрыш и усиление токсичности от назначения комбинации, представляется более перспективным последовательное назначение двух препаратов.
Выполнение подмышечной лимфаденэктомии сопровождается мучительными для женщин послеоперационными осложнениями: ограничение в подвижности и болезненность при движении в руке на стороне операции, лимфостаз, нарушения кожной чувствительности. Можно ли избежать выполнения лимфаденэктомии у больных с отсутствием увеличенных лимфоузлов в подмышечной области? В исследование включались больные старше 60 лет с операбельным раком молочной железы и отсутствием увеличенных подмышечных лимфоузлов [19]. Удаление опухоли (лампэктомия или мастэктомия) с одновременной подмышечной лимфаденэктомией выполнена 234 больным, у 239 больных проведено только удаление опухоли. Все больные с положительными рецепторами эстрогенов в опухоли получали тамоксифен. Средний возраст больных составил 74 года, у 80% была рецептороположительна. Мастэктомия была выполнена у 45% больных, лампэктомия с последующей лучевой терапией или без нее у 33% и 22% соответственно. При медиане наблюдения 6 лет 5-летняя безрецидивная выживаемость в группе подмышечной лимфаденэктомии составила 71% и 70% без нее, 5-летняя общая выживаемость 78% и 80% соответственно. В группе без выполнения лимфаденэтомии отмечено качество жизни, лучшая подвижность руки со стороны операции, меньшая частота лимфостаза. Авторы делают вывод о возможности отказа от выполнения подмышечной лимфаденэктомии у больных старше 60 лет без увеличения подмышечных лимфоузлов.
1. Nabholtz J.M., Buzdar A., Pollak M. et al. Anastrozole is superior to tamoxifen as first-line therapy for advanced breast cancer in postmenopausal women: results of a North American multicenter randomized trial. Arimidex Study Group. J. Clin. Oncol. 2000, 18: 3758–3767.[Abstract/Free Full Text]
2. Bonneterre J., Thurlimann B., Robertson J.F. et al. Anastrozole versus tamoxifen as first-line therapy for advanced breast cancer in 668 postmenopausal women: results of the Tamoxifen or Arimidex Randomized Group Efficacy and Tolerability study. J. Clin. Oncol. 2000, 18: 3748–3757.[Abstract/Free Full Text]
3. Mouridsen H., Gershanovich M., Sun Y. et al. Superior efficacy of letrozole versus tamoxifen as first-line therapy for postmenopausal women with advanced breast cancer: results of a phase III study of the International Letrozole Breast Cancer Group. J. Clin. Oncol. 2001, 19: 2596–2606.[Abstract/Free Full Text]
5. Cameron D.A., Winer E., Campos S., Guastalla J.P. A comparative study of exemestane versus anastrozole in post-menopausal breast cancer subjects with visceral disease. Proc. ASCO 2004, 23: 34 (abstract 628).
6. Buzdar A. The ATAC (Arimidex, Tamoxifen, Alone or in Combination) trial in postmenopausal women with early breast cancer—updated efficacy results based on a median follow-up of 47 months. ATAC Trialist Group. Presented at the San Antonio Breast Cancer Symposium, San Antonio, Texas, December 2002.
7. Goss P.E., Ingle J.N., Martino S. et al. A randomized trial of letrozole in postmenopausal women after five years of tamoxifen therapy for early-stage breast cancer. N. Engl. J. Med. 2003, 349: 1793–1802.[Abstract/Free Full Text]
8. Goss P.E. NCIC CTG MA.17 final analysis of updated data: a placebo-controlled trial of letrozole following tamoxifen as adjuvant therapy in postmenopausal women with early stage breast cancer. In: Best of Oncology/Society Abstracts. Program and abstracts of the 40th Annual Meeting of the American Society of Clinical Oncology; June 5-8, 2004; New Orleans, Louisiana. Special Session.
9. Boccardo F., Rubagotti A., Amoroso D. et al. Anastrozole appears to be superior totamoxifen in women already receiving adjuvant tamoxifen treatment. Breast Cancer. Res. Treat. 2003, 82: suppl 1:S6.
10. Coombes R.C., Hall E., Gibson L.G. et al. A Randomized trial of exemestane after two to three years of tamoxifen therapy in postmenopausal women with primary breast cancer. N. Engl. J. Med. 2004, 350: 1081-1092.
11. Howell A. on behalf of the ATAC Trialists’ Group. Effect of anastrozole on bone mineral density: 2-year results of the «Arimidex» (anastrozole), tamoxifen, alone or in combination (ATAC) trial. Breast Can. Res. Treat. 2003, 82(suppl 1): S27 (abstract 129).
Аримидекс или анастрозол что лучше
Российский Онкологический Научный Центр им. Н.Н.Блохина
АРИМИДЕКС: результаты исследований по переводу пациентов, уже принимавших в качестве адьювантной терапии тамоксифен на анастразол.
Появление новой генерации ингибиторов ароматазы, направленных на подавление основного пути продукции эстрогенов у женщин в менопаузе при раке молочной железы, предопределило возможное преимущество этого класса соединений над “золотым” стандартом гормонотерапии антиэстрогеном тамоксифеном. После получения положительных результатов терапии распространенных форм заболевания был предпринят ряд работ по изучению эффективности ингибиторов ароматазы в адъювантной терапии. При этом данный класс препаратов использовался в качестве альтернативы тамоксифену, в комбинации с тамоксифеном, а также осуществлялся перевод больных на терапию анастразолом после нескольких лет лечения тамоксифеном в адъювантном режиме.
Франческо Боккардо(2005) [5] с коллегами впервые предложил идею о переводе больных, получавших адъювантную терапию тамоксифеном, на лечение ингибиторами ароматазы. В проведенном рандомизированном исследовании после 2 – 3х летнего лечения тамоксифеном пациенты слепым методом распределялись на 2 группы, на тех кому назначали анастрозол 1 мг в день и тех кому продолжали терапию тамоксифеном 20 мг в сутки. Общая продолжительность лечения составила 5 лет. Показатель безрецидивной выживаемости был основным в анализе эффективности лечения. Также оценивали общую выживаемость и безопасность проводимой терапии.
Все женщины имели эстрогенположительную опухоль. В исследование включено 448 пациенток. Медиана времени наблюдения 52 месяцев. На момент проведения анализа рецидивы заболевания зарегистрированы у 32 больных (14,2%), получавших тамоксифеном и у 12 больных (5,4%) – терапию анастразолом. При использовании тамоксифена по сравнению с анастразолом отмечалось развитие большего числа вторых первичных опухолей (10 и 5 случаев соответственно), включая 5 случаев рака эндометрия, а также смертельных исходов не связанных с рецидивом заболевания. Таким образом, за последующие 36 месяцев, о 45 случаях побочных эффектов сообщили в группе тамоксифена по сравнению с 17 случаями в группе с анастрозолом (P=0.0002). Безрецидивная выживаемость была значительно длиннее в группе анастрозола. Больше случаев, связанных с угрозой жизни или требующих госпитализации отмечено в группе тамоксифена, чем в группе анастрозола (33 из 150 случаев на 28 из 203 случаев, P=0.04)
Раймонд Джейкс и Вальтер Джонат с коллегами (объединенные результаты ABCSG-8 и АRNО 95) (2005) [6] также изучали такой подход в лечении постменопаузальных женщин с гормонозависимым ранним раком молочной железы. Больные распределялись на следующие группы: те, которые, после 2-х летней адъювантной терапии тамоксифеном (20 или 30 мг ежедневно) переводились на ингибитор ароматазы – анастрозол в дозе 1 мг (n=1618), и те, которые продолжали принимать тамоксифен по 20 или 30 мг (n=1606) в адъювантном режиме. В этом исследовании оценивалась безрецидивная выживаемость и число возникновения контралатерального рака молочной железы в группах сравнения.
В исследование было включено 3224 пациентки. Медиана времени наблюдения 28 месяцев. Было отмечено 40%-ое снижение риска рецидива в группе с анастрозолом по сравнению с группой тамоксифена (67 случаев при применении анастрозола против 110 с использованием тамоксифена p=0.0009). Безрецидивная выживаемость спустя 3 года составила 92.7 % для группы, получавшей тамоксифен и 95.8 % для группы, которая была переведена на анастрозол. Оба варианта лечения хорошо переносились. Среди женщин, у которых отмечено прогрессирование болезни, рецидивы в виде отдаленных метастазов составляли 62 %.(n=110). Контралатеральное и развившееся на стороне поражения рецидивирование составило только 16 % (n=28) для группы с анастразолом и 23 % (n=41) в группе тамоксифена. Больше рецидивов заболевания отмечено при лечении тамоксифеном, чем в группе пациенток, получающих анасторозол. Отмечено, что умерли 59 пациентов в группе тамоксифена и 45 в группе анастрозола.
Спустя 3 года общая выживаемость была немного выше у пациентов, которые были переведены на анастрозол (97 %), чем у продолжавших прием тамоксифена (96 %), хотя это различие не существенно (p=0.16).
Отмечалось значительно меньше тромбозов (p=0.034), эмболий (p=0.064) и случаев развития рака эндометрия(p=0.069) у пациенток, лечившихся анастрозолом по сравнению с тамоксифеном. Эти данные демонстрируют целесообразность перехода на использование анастрозола у пациентов, которые в течение 2-х лет получали адъювантную терапию тамоксифеном.
Полученные результаты указывают, что не следует проводить полный 5-летний курс лечения тамоксифеном перед переходом на ингибиторы ароматазы. Кроме того, более высокий уровень рецидивов (особенно в течение 1-3 года), побочных эффектов в группе тамоксифена, еще раз доказывают, что наиболее эффективный и безопасный метод терапии ингибиторами ароматазы должен назначаться на возможно более ранних этапах терапии.
Что лучше: Аримидекс или Анастрозол-Тева
Аримидекс
Анастрозол-Тева
Исходя из данных исследований, Аримидекс лучше, чем Анастрозол-тева. Поэтому мы советуем выбрать его.
Активные вещества одинаковые. Поэтому выбирайте исходя из цены
Сравнение эффективности Аримидекса и Анастрозол-тевы
Эффективность у Аримидекса достотаточно схожа с Анастрозол-тевой – это означает, что способность лекарственного вещества оказывать максимально возможное действие схоже.
Например, если терапевтический эффект у Аримидекса более выраженный, то при применении Анастрозол-тевы даже в больших дозах не получится добиться данного эффекта.
Также скорость терапии – показатель быстроты терапевтического действия у Аримидекса и Анастрозол-тевы примерно одинаковы. А биодоступность, то есть количество лекарственного вещества, доходящее до места его действия в организме, схожа. Чем выше биодоступность, тем меньше его потерь будет при усвоении и использовании организмом.
Сравнение безопасности Аримидекса и Анастрозол-тевы
Безопасность препарата включает множество факторов.
При этом у Аримидекса она достаточно схожа с Анастрозол-тевой. Важно, где метаболизируется препарат: лекарственные вещества выделяются из организма либо в неизмененном виде, либо в виде продуктов их биохимических превращений. Метаболизм протекает спонтанно, но чаще всего задействует основные органы, такие как печень, почки, лёгкие, кожу,